 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Гетероциклічні сполуки
Повне відновлення пірольного циклу відбувається при гідруванні над платиновим або паладієвим каталізатором. Як результат — | утворюється тетрагідропірол (піролідин).
/ \ Щ] (2п + СН3СООН) Ц \\ N11NН Ші 'N11 №і піролін піролідин Піролін і піролідин є циклічними амінами, що істотно відрізняються за хімічними властивостями від піролу. У молекулі піроліну неподілена пара електронів атома Нітрогену не спряжена з п-електронами подвійного зв'язку, тому він виявляє властивості амінів і ненасичених сполук. А піролідин належить до насичених сполук — це типовий представник вторинних циклічних амінів. Піролідиновий цикл входить до складу багатьох природних сполук, таких, як алкалоїди, нікотин, кокаїн, атропін та ін. 4. Реакції окиснення.Фуран і пірол дуже чутливі до дії окисників і окиснюються навіть киснем повітря. При окисненні відбувається розрив гетероциклічного ядра і утворюються полімерні сполуки. Проте пропускання суміші фурану з повітрям над каталізатором У205 при температурі 320 °С приводить до утворення ангідриду малеїнової кислоти.
7 \
о малеїновий ангідрид
При окисненні піролу хромовою кислотою утворюється імід
у \\ [О] н2Сг2о4> о ї н
пірол Тіофен дуже важко піддається окисненню. 5. Взаємні перетворення фурану, піролу та тіофепу.Реакція проходить при температурі 450 °С у присутності каталізатора А1203 (див. розд. 15.4.1). Б. Специфічні хімічні властивості піролу Пірол, будучи слабкою N^1010^010 (рКа ~ 17,5), взаємодіє з металічним калієм, безводним калій гідроксидом, металічним натрієм і літієм у рідкому амоніаку, з калій та натрій амідами, а також магнійорганічними сполуками, утворюючи солі.
•О-
О-
"МІ Н8+
пірол
М§1 піролідмагній йодид Аніон піролу, що входить до складу солей піролу (піролід-ані-он), являє собою доволі стійку частинку внаслідок делокалізації негативного заряду по пірольному ядру. Солі піролу є реакційноздатними речовинами і широко застосовуються в органічному синтезі. Можливості виявлення гетероциклічних сполук за допомогою хімічних методів обмежені. Для ідентифікації піролу та фурану застосовують простий і доступний метод — забарвлення соснової скіпки. Пари піролу забарвлюють соснову скіпку, змочену соляною кислотою, в червоний колір (руггої - червоне масло), а фурану — в інтенсивно-зелений. НАЙВАЖЛИВІШІ ПОХІДНІ ПІРОЛУ Піролідон
-піролідон
+ иНО^СН-~ п
к °
СН=СН2 N-вініл-2-піролідон Глава 15
гетероциклічні сполуки
Низькомолекулярний ПВП (молекулярна маса 12—13 тис.) утворює колоїдні розчини у воді й застосовується для приготування кровозамінника «Гемодезу», середньомолекулярний ПВП (м. м. 35— 40 тис.) використовують у фармацевтичній промисловості як зв'язувальний засіб у виробництві таблеток.
Порфін— кристалічна речовина темно-червоного кольору. За хімічною структурою являє собою макроциклічну спряжену систему, яка складається з пірольного III, піролінового / та двох ізопірольних II, IV ядер, зв'язаних між собою метиновими групами =СН—. Порфін є ароматичною сполукою. Він має площинну будову молекули, містить замкнену спряжену систему з кількістю я-електронів, яка дорівнює 26 (11 л-зв'язків і дві пари неподілених електронів при атомах Нітрогену), що відповідає правилу Хюккеля (4л + 2 при п = 6). Похідні порфіну дістали загальну назву «порфірини». У вигляді комплексів з металами порфірини входять до складу таких важливих природних сполук, як гемоглобін і хлорофіл. Гемоглобін— це барвна речовина крові, що міститься в еритроцитах. Він являє собою складний білок — хромопротеїд, який складається з білка глобіну та забарвленої в червоний колір небіл-кової частини — гему. За хімічною структурою гем є комплексом порфірину з Ре (II). При кислотному гідролізі гемоглобіну вільний гем легко окиснюється на повітрі з утворенням геміну, який має ту ж саму структуру, що й гем, але містить Ре (III).
Будову геміну встановив 1929 року Г. Фішер, тоді ж він здійс- нИВ і синтез геміну. Гем, координаційно сполучений з глобіном, утворює гемоглобін.
оксигемоглобін Деякі речовини, зокрема карбон (II) оксид та солі синильної кислоти, утворюють з гемоглобіном стабільніші комплекси, ніж кисень, і тим самим блокують дію гемоглобіну. Такі сполуки відносять до дихальних отрут. Частково гідрований порфіновий цикл, координаційно зв'язаний з магнієм, входить до складу зеленого пігменту рослин — хлорофілу. Хлорофіл виконує важливу роль у процесі фотосинтезу, перетворюючи світлову енергію сонячного випромінювання на енергію хімічних зв'язків.
де К: -СН2СН2СООН н3с
Поиск по сайту: |

 При конденсації 2-піролідону з ацетиленом утворюється ^вініл-2-піролідон, який легко полімерний • зується, утворюючи полівінілпіролідон (ПВП).
При конденсації 2-піролідону з ацетиленом утворюється ^вініл-2-піролідон, який легко полімерний • зується, утворюючи полівінілпіролідон (ПВП).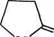

 Гемоглобін в організмі виконує роль носія кисню з легенів У тканини. При цьому молекула кисню зворотньо реагує з гемоглобіном з утворенням оксигемоглобіну за схемою:
Гемоглобін в організмі виконує роль носія кисню з легенів У тканини. При цьому молекула кисню зворотньо реагує з гемоглобіном з утворенням оксигемоглобіну за схемою: