 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
АРОМАТИЧНІСТЬ ГЕТЕРОЦИКЛІВ
Як відомо, ознакою ароматичності сполуки є наявність плоскої циклічної системи, що має замкнутий ланцюг спряження, яка містить (4л+2) я-електронів (див. розд. 13.1.). Ароматичність п'ятичленних гетероциклів з двома я-зв'язками зумовлена тим, що в спряження з я-електронами подвійних зв'язків вступає неподілена пара електронів гетероатома О, N або 8. Глава 15 П,терОЦикліЧНІ СП0ЛУКИ
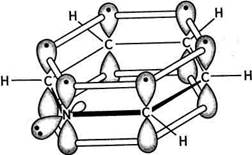
На рис. 15.1 подано електронну будову молекули піролу.У молекулі піролу атоми Карбону та атом Нітрогену знаходяться в стані 5/?2-гібридизації. За рахунок л/^-гібридних орбіталей кожний атом, який входить до складу циклу, утворює три о-зв'язки, розміщені в площині кільця. При цьому в атомів Карбону і атома Нітрогену залишається по одній негібридизованій /ьорбіталі, що розташовані паралельно одна одній у площині, перпендикулярній до площини кільця. Кожна з р-АО атомів Карбону має один електрон, а на /7-орбіталі атома Нітрогену знаходиться неподілена пара електронів. При взаємному перекриванні /ьорбіталей утворюється єдина шестиелектронна хмара, що охоплює всі атоми циклу.
Аналогічно утворюється спряжена система в інших п'ятичленних гетероциклах з двома я-зв'язками, зокрема, в молекулах фуранута тіо-фену.У цих структурах, як і в піролі, гетероатом (О і 8) надає в ароматичний секстет неподілену пару ^-електронів. Аналогічно з піролом гетероатом, який вносить у л-електронну систему два електрони, що займають ^-атомну орбіталь, і який утворює з іншими атомами тільки о-зв'язки, прийнято називати гетероатомом пірольного типу. У ряду шестичленних гетероциклів ароматичні властивості характерні для структур, які являють собою гетероциклічні аналоги бензену. Так, у молекулі піридину(шестичленний гетероцикл з атомом Нітрогену) всі атоми Карбону і атом Нітрогену знаходяться в стані .^-гібридизації. Замкнена шести я-електронна система утворюється п'ятьма /ьорбіталями атомів Карбону (по одній від кожного) та /?-орбіталлю атома Нітрогену. Тобто в молекулі піридину, як і в молекулі бензену, кожний атом циклу надає в ароматич-нйй секстет по одному п-електрону (рис. 15.2).
Неподілена пара електронів атома Нітрогену в молекулі піридину, на відміну від молекули піролу, займає ^-гібридну орбіталь і не бере участі в утворенні ароматичного секстету. Атом Нітрогену в 5р2-гібридизації, що має електронну конфігурацію, в якій неподілена пара електронів займає 5р2-гібридизовану орбіталь і не бере участі в утворенні ароматичного секстету, дістав назву піридинового. Гетероатом такої електронної конфігурації (у цьому випадку атом Нітрогену) ще умовно називають гетероатомом піридинового типу. Гетероатом піридинового типу, маючи більшу електронегатив-ність порівняно з Карбоном, зменшує електронну густину на атомах Карбону ароматичного кільця. Молекули гетероциклів з двома та більше гетероатомами, а також конденсовані гетероциклічні системи можуть включати гетероатоми як пірольного, так і піридинового типу.
Глава £
Гетероцикли, у молекулах яких гетероатом є донор неподіленої пари електронів і, відповідно, збільшує електронну густину на атомах Карбону ароматичного циклу називають я-надлишковими. До них відносять п'ятичленні гетероароматичні сполуки, які містять гетероатоми пірольного типу (фуран, пірол, тіофен та ін.) Гетероцикли, у молекулах яких гетероатом зменшує електронну густину на атомах Карбону ароматичного кільи називають я-дефіцитними. До я-дефіцитних гетероциклічних систем відносять гетероцикли, які містять гетероатоми піридинового типу (піридин, піримі-дин та ін.). При атомі Нітрогену піридинового типу неподілена пара електронів знаходиться на ір2-гібридній орбіталі і не бере участі в утворенні ароматичного секстету. За рахунок цієї електронної пари Нітроген піридинового типу здатний приєднувати протон, тобто виявляти основні властивості (згадайте властивості амоніаку).
Отже, кислотні властивості нітрогеновмісних ароматичних ге-тероциклів зумовлені наявністю в їх структурі атома Нітрогену пірольного типу, а основні — атома Нітрогену піридинового типу. Гетероциклічні сполуки, що містять у своєму складі атоми Нітрогену пірольного та піридинового типів, виявляють амфотерні властивості (імідазол, пурин та ін.).
Кислотні та основні властивості гетероциклічних сполук зумовлені електронною будовою гетероатомів. У молекулі піролу неподілена пара електронів гетероатома, яка
Поряд із цим участь пірольного атома Нітрогену в спряженні сприяє поляризації зв'язку N—Н і тим самим збільшує рухливість атома Гідрогену, що приводить до виявлення в піролу властивостей слабкої >Щ-кислоти. При дії лужних металів і сильних основ (КаОН, №1ЧН2) відбувається заміщення атома Гідрогену при пі-рольному атомі Нітрогену на метал:
№КН2 натрій амід
Поиск по сайту: |

 Утворюється замкнена спряжена система, в якій кількість успільнених л-електронів відповідає правилу Хюккеля (4л+2).
Утворюється замкнена спряжена система, в якій кількість успільнених л-електронів відповідає правилу Хюккеля (4л+2).
 (гетероатом піридинового типу]
(гетероатом піридинового типу] Розподіл гетероатомів на атоми пірольного та піридиновог типів дозволив А. Альберту в 1958 році ввести поняття про л-над лишковістьі я-дефіцитністьгетероароматичних сполук.
Розподіл гетероатомів на атоми пірольного та піридиновог типів дозволив А. Альберту в 1958 році ввести поняття про л-над лишковістьі я-дефіцитністьгетероароматичних сполук.
 15.3. КИСЛОТНО-ОСНбВНІ ВЛАСТИВОСТІ ГЕТЕРОЦИКЛІВ
15.3. КИСЛОТНО-ОСНбВНІ ВЛАСТИВОСТІ ГЕТЕРОЦИКЛІВ