|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
П'єр Ежен Марселен БЕРТЛО (БЕРТЕЛО)
(1827-1907) Французький хімік і державний діяч. Основні сфери наукових досліджень — органічна, аналітична, тер-мо-, біохімія, історія хімії, педагогіка, лінгвістика. Один з основоположників синтетичного напряму в органічній хімії. Уперше синтезував (1851) нафта -лен, бензен і фенол у результаті пірогенетичного розкладання кисневмісних речовин, а також (1854) аналоги стеарину, пальмітину, олеїну та інших жирів. На основі кислотної гідратації етилену здійснив синтез (1854) етилового спирту, який раніше одержували лише бродінням цукристих речовин. Запропонував (1867) метод відновлення органічних речовин з використанням йодистого водню. Увів поняття про ендотермічні й екзотермічні реакції. Досліджував кінетику утворення і розщеплення естерів. Один з перших творців теорії вибухових процесів.
Ма+ Водна фаза
Рис. 37.2. Орієнтація молекул мила на межі розділу водного і повітряного середовищ Глава 37
Аналогічний механізм має процес солюбіліза-ції нерозчинних у воді органічних (у тому числі лікарських) речовин. Більш широке використання мил як мийних засобів обмежене тим, що в «твердій» воді (з підвищеним вмістом іонів Ca2+ і Mg2+) мила утворюють нерозчинні солі Кальцію і Магнію, які осаджуються у вигляді пластівців і забруднюють поверхні, що відмиваються. На утворення цих солей витрачається значна кількість мила. як солі слабких кислот і сильних основ мила внаслідок гідролізу створюють лужне середовище у водних розчинах, яке зумовлює подразнюючу дію мил на слизові оболонки. Зазначені вади мил спричинили створення широкого асортименту більш дешевих і технологічних синтетичних замінників мил — детергентів.
695 Детергенти, або синтетичні мийні засоби, як і мила, належать до ПАР. їх молекули також включають неполярний (гідрофобний) вуглеводневий фрагмент і полярну (гідрофільну) частину, презентовану аніоноїдним або катіоноїдним функціональним угрупованням, зв'язаним з іонами Натрію або мінеральної кислоти відповідно. Полярний кінець молекули детергенту може бути також утворений нейтральним залишком багатоатомного спирту або поліестеру. Залежно від будови полярної частини молекули синтетичні мийні засоби поділяють на аніонні, катіонні та нейтральні.
СН-(СН2) ;СН сн—сн; натрій и-(децил-3)бензенсульфонат У молекулах аніонних детергентів як полярний фрагмент найчастіше міститься бензенсульфонатний залишок. Неполярна частина молекули таких детергентів утворена довголанцюговим алкілом, як правило, вторинним і нерозгалуженої будови. Детергенти з розгалуженими вуглеводневими ланцюжками неприйнятні в екологічному плані, оскільки в процесі очищення стічних вод вони не розкладаються мікроорганізмами, що приводить до накопичення синтетичних мийних речовин у природних водоймах у згубних для їх мешканців концентраціях. До катіонних детергентів належать насамперед четвертинні амонієві солі, наприклад N,N-диметил-N,N-діоктадециламоній хлорид. СН3 (СН2) 17\ + / СН3 СН3-(СН2)/ ЧСН3 сг К,К-диметил-1Ч,]Ч-діоктадециламоній хлорид Прикладами нейтральних (неіоногенних) детергентів можуть слугувати такі сполуки: СН2ОН Л О\о-(сн2)и-сн3 (он Н/ НО-(СН-СН2-О)8-(СН2)И-СН3 НО У^ ^ Н он р-додецилглюкозид О-додецилоктастиленгліколь На відміну від мил, синтетичні мийні засоби не утворюють нерозчинних солей з катіонами Кальцію та Магнію, а їх водні розчини мають нейтральну реакцію, оскільки детергенти є або солями сильних кислот і сильних основ, або не містять груп, здатних гідролізуватися за звичайних умов. Важливою перевагою детергентів перед милами є і те, що їх виробництво не потребує використання як сировини жирів — цінних харчових продуктів. Окиснення жирів. Причиною легкої окиснюваності жирів киснем повітря є наявність подвійних зв'язків у молекулах, що приводить до «гіркнення» жирів. При Глава 37 їх окисненні утворюються альдегіди з короткими вуглецевими ланцюгами, які зумовлюють неприємний запах і смак «згірклих» жирів.
СН2— О—С— (СН2)7— СН СН3—(СН2)7—СН 02
сн2— о—с—(сн2)7— сн—о сн3-(сн2)7-сн-онон о
сн2—о—с—я-
сн2— о—с— (сн2)7— с^
к—с—о—сн сн2—о—с—к( Окиснення ненасичених жирів у м'яких умовах (водним розчином калій перманганату) приводить до утворення гліколів. Наслідком окиснення за більш жорстких умов є розрив вуглецевого скелета з утворенням залишків відповідних карбонових кислот з коротшими вуглецевими ланцюгами. ЇЇ СН2—О—С—(СН2)7—СН— ОН о КМпО4;Н2О Ц СН3—(СН2)7—СН—ОН --------------------------- ► к—с—о-сн ч--------- :тг^---------- 0 л 9,10-дипдроксистеарат
сн2—о—с—(сн2)7—сн СН3—(СН2)7—СН к—с—о—сн
КМпО4; н3о*
СН,—О—С—К'
сн2—о—с—(сн2)7—с—он + ;с—(сн2)7—сн3
к—с—о—сн СН,—О—С—К' 697 При окисненні жирів, у складі яких переважають залишки насичених жирних кислот, характерне утворення кетонів. Гідрогенізація жирів. Гідрогенізації піддаються рослинні олії і жири, які добувають з морських тварин (китовий жир тощо). В основу процесу покладено реакцію приєднання водню за місцем розриву подвійних зв'язків у залишках лінолевої, ліноленової, олеїнової та інших ненасиче-них кислот у присутності нікелевого або платинового каталізаторів при температурі 190—220°С і тиску 0,2—2,0 МПа (каталітичне гідрування). СН3 о сн—сн=сн—сн—сн о СН2— О—С—(СН2)7— СН= СН—СН —СН СН2— О—С—(СН2)п-СН3 О СН-(СН2)-СН 12Н;№; О СН — О—С— (СН2)7— СН= СН— СН — СН 11? IV сн2—о—с—(сн2)—сн= сн—(сн2)—сн3 сн2— о—с—(сн2)^сн3 2-О-лінолеїл-З-О-ліноленоїл-О-олеоїлгліцерин тристеароїлгліцерин (рідкий жир — олія) (твердий жир) Завдяки насиченню вуглець-вуглецевих зв'язків воднем, а також унаслідок ізомеризації залишків олеїнової кислоти (цис-ізомер, т. пл. 13,4 і 16,3 °С) в елаїдинову (транс-ізомер, т. пл. 51,5 °С) під дією нікелевого каталізатора (елаїдування), рослинні олії перетворюються у тверді жири. Промислові жири, здобуті гідрогенізацією рослинних олій, а також жирів, одержаних з морської фауни, називають саломасами. Харчові саломаси (т. пл. 31— 33 °С) використовують у виробництві кондитерських, кулінарних жирів і маргарину. Маргарин — харчовий жир, який є сумішшю гідрогенізованих жирів рослинного і тваринного походження з додаванням вершків, смакових речовин і за-пашників (діацетилу CH3—CO—CO—CH3, ацетоїну CH3—CHOH—CO—CH3 тощо). Технічні саломаси (т. пл. 39—49°С) — сировина для виробництва мила, стеарину тощо. Унаслідок гідрогенізації жирів змінюються не тільки їх фізичні властивості, але завдяки різкому зменшенню кількості подвійних зв'язків у їх молекулах вони набувають стійкості до дії окисників, зокрема кисню повітря, тобто до гіркнення. При цьому вони зберігають високу поживність, характерну для кращих сортів тваринних і рослинних жирів, але на відміну від тваринних жирів продукти гідрогенізації рослинних олій не містять домішки холестеролу, надлишок якого в організмі приводить до атеросклерозу. Кількість грамів водню, необхідна для гідрування 10 кг жиру, є аналітичною характеристикою (число гідрування), яка свідчить про міру ненасиченості жиру. Приєднання галогенів. Реакція приєднання галогенів за місцем розриву подвійних зв'язків у ряду жирів має велике аналітичне значення. Знебарвлення бромної води вказує на вміст залишків ненасичених кислот у молекулі досліджуваного тригліцериду. Кількість грамів йоду, що приєднується до 100 г жиру, названа йодним числом, характеризує міру ненасиченості жирів. Глава 37
О СН3(СН2)7—СН О СН3(СН2)7—СН—І
(СН2)-СН О СН3(СН2)-СН (СН2)-СН О СН3(СН2)-СН (сн2)—сн СН,— О—С (СН2)7—СН—І О СН3(СН2)7—СН—І СН —О—С---- (СН2)7—СН—І
О СН3(СН2)7-СН-І (сн2)7— сн—і
триолеїн три(9,10-дийодостеароїл)глщерин йодне число варіює для рослинних олій у межах 100—200, для тваринних жирів — від 25 (у молочного) до 86 (у кінського), для жирів морських ссавців і риб — від 100 (китовий) до 193 (тюленячий). воски. твши Воски — естери вищих карбонових кислот і високомолекулярних спиртів, які містять парну кількість атомів Карбону в кислотних і спиртових залишках. Здебільшого воски — насичені сполуки. Найчастіше до складу восків входять цетиловий C16H33OH та мірициловий C30H61OH спирти. Воски поділяють на тваринні (спермацет, бджолиний віск, ланолін тощо) і рослинні (карнаубський віск). Воском прийнято вважати також озокерит (гірський віск) — мінеральний викопний продукт (т. пл. 58—100°С), який є сумішшю переважно насичених вуглеводнів, здебільшого з розгалуженими ланцюгами. Використовують озокерит у медицині (озокеритолікування), у виготовленні мастил, кремів, гідрофобізації матеріалів і т. ін. Воски бувають м 'які і тверді, тому що їх температура плавлення підвищується з подовженням вуглецевого ланцюга молекул. До м'яких восків належать ланолін і спермацет. Ланолін добувають шляхом очищення шерстяного (вовняного) воску, який є сумішшю естерів ланолінового спирту C12H23OH, діестерів а,|3-алкандіолів (гліколів), вищих жирних кислот (C18—C24), з високим вмістом вільних вищих спиртів і кислот (до 45%), вуглеводнів (до 18%) і стеринів (до 10%). шерстяний віск продукується шкірними залозами овець і у великій кількості (5—16%) міститься на овечій вовні, з якої його змивають на шерстемийних фабриках органічними розчинниками. ланолін (т. пл. 36—42°С) нерозчинний у воді, але, на відміну від інших восків, здатний утворювати стійкі емульсії навіть з подвійною за масою кількістю води. Остання властивість дозволяє використовувати ланолін як мазеву основу для введення до складу мазі водорозчинних лікарських речовин. Спермацет, який на 98% складається з цетину C15H31COOC16H33, виморожують зі спермацетового масла, добутого витоплюванням зі спермацетового мішка голови кашалота. Спермацет використовується у фармації як основа для мазей, кремів, а також при виробництві мила, свічок тощо. Гідруванням спермацетового масла одержують цетилпальмітат — віск, більш стійкий до окиснення, ніж спермацет. Карнаубський віск є твердим воском (покриває листя бразильської воскової пальми). Він містить більше 80% естерів вищих жирних кислот і вищих спиртів. Основна складова частина — HOCH2(CH2)nCOOCH2(CH2)mCH3, де n = 16—28, 699 т = 30 і 32. Карнаубський віск застосовують як компонент полірувальних паст, при виробленні шкіри, у виробництві копіювального паперу. Бджолиний віск містить 72% естерів вищих жирних кислот і вищих спиртів (33% мірицилпальмітату C15H31COOC30H61), до 13,5 % вільних кислот і 12—12,5 % вуглеводнів. Температура плавлення бджолиного воску 62—70°С. Добувають його з бджолиних стільників, використовують для виготовлення штучної вощини, як компонент для полірувальних паст і мазей, косметичних препаратів і т. ін. твіни— синтетичні продукти, близькі за будовою до гліцеридів. Вони є неповними етерами шестиатомного спирту сорбіту і поліетиленгліколю, в яких вільні гідроксильні групи в залишку сорбіту естерифіковані вищими жирними кислотами.
Виснаження нафтових запасів і ріст цін на енергоносії обумовили інтенсивний пошук альтернативних джерел енергії. Одними з перспективних видів пального є біоетанол і біодизель. Біоетанолможна виробляти з біомаси (рослинних і тваринних матеріалів). Він має високе октанове число. «Газоголь» (бензинова суміш, що містить 10 % біоетанолу) вже набуває розповсюдження на американському континенті. Зокрема, у Бразилії використовується велика кількість етаноловмісного пального. Автомобіль не потребує спеціального переобладнання, хоча і відчувається деяке зниження потужності його двигуна. У багатьох країнах єС вміст етанолу в моторному пальному обмежується 5 %. Біодизель— пальне, отримане на основі жирів, частіше рослинного походження. Біодизель — не що інше, як естери карбонових кислот, що мають властивості пального матеріалу і одержані з жиру в результаті реакції переестерифікації. Основна сировинна база пального — рослина ріпак (Вгашса париз L.). яскраво-жовті квітки цієї невибагливої рослини можна зустріти повсюди на полях європи. Виділену ріпакову олію піддають обробці метанолом у присутності основного каталізатора.
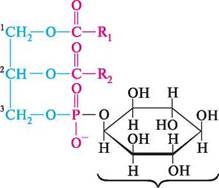
н2с—он не—он + з к—с—осн, н2с-он тригліцерид гліцерин біодизель Вміст метилових естерів після проходження реакції переестерифікації має бути вище 96%. Біодизель «біологічно нешкідливий»: мікроорганізми за 28 днів утилізують до 99 % біо-дизеля, що потрапив у ґрунт або воду. При згорянні дає меншу кількість викидів вуглекислого газу в атмосферу порівняно з іншими видами пального. є відносно безпечним пальним (точка займання перевищує 100 °С). Ринок біодизеля розвивається швидкими темпами. Глава 37 СКЛАДНІ ЛІПІДИ До складних ліпідів належать фосфоліпіди і гліколіпіди (див. с. 688). ФОСФОЛІПІДИ Фосфоліпідами називають фосфорильовані ліпіди. Унаслідок гідролізу фосфоліпідів утворюються вищі жирні кислоти (ВЖК), спирт — гліцерин або сфінгозин, фосфатна кислота Н3РО4, часто — нітрогено-вмісні основи (аміноспирти — коламін, холін, амінокислота — серин) тощо. Фосфоліпіди залежно від природи спирту, що входить до складу молекули, поділяють на дві групи: гліцерофосфоліпіди та сфінгомієліни. /-1ТТ ҐҐ^ТІ \ ХТ З 2 12\с/ сн2-он н^ ^сн—он сн-он сн- сн2— он сн2— он гліцерин сфінгозин Гліцерофосфоліпіди— це похідні фосфатидної кислоти: О СН2— О—С—К: — залишок насиченої ВЖК;О СН — О—С—К^ — залишок ненасиченої ВЖК;О СН2—О—Р—ОН — залишок фосфатної кислоти ОН фосфатидна кислота; діацилгліцерилфосфат Одна з гідроксильних груп фосфатидних кислот, як правило, естерифікована нітрогеновмісною сполукою: аміноспиртом (коламіном, холіном), амінокислотою (серином) або циклічним шестиатомним спиртом інозитолом тощо. н2м—сн—сн2—он
(СН3)3К—СН— СН2— ОН холін (триметильована похідна етаноламіну) ЛІПІДи о сн2—о—с—кх о Загальна формула гліцерофосфоліпідів СН — О—С—К2 , О сн2—о—р—ок3 О" де К: R2 — залишки ВЖК; R3 — залишок нітрогеновмісної сполуки (коламіну, холіну, серину) або інозитолу. У ряду гліцерофосфоліпідів виділяють фосфатидилетаноламіни (кефаліни), фосфатидилхоліни (лецитини), фосфатидилсерини, фосфатидилінозитоли тощо. Фосфатидилетаноламіни (кефаліни) Фосфатидилхоліни (лецитини) О ? \— п—г—р сн2—о—с—кх
я-о-с-н,
фрагмент етаноламіну 3-фосфатидилетаноламін; кефалін фрагмент холіну З -фосфатидилхолін; лецитин Кефаліни та лецитини метаболічно зв'язані один з одним і є головними ліпідними компонентами клітин. Дипальмітиллецитин знижує поверхневий натяг і тим самим перешкоджає злипанню внутрішніх поверхонь дихальних шляхів у легенях. його відсутність у легенях недоношених немовлят призводить до розвитку синдрому дихальної недостатності. Фосфатидилсерини. Слід зазначити, що були також виділені фосфоліпіди, які містять залишок треоніну (див. с. 662). О г-О—С—ЕЦО СН —О—С—К, О СОО" Зсн2— о—р—о—сн—сн—]чн3 І _ V О фрагмент серину З -фосфатидилсерин Глава 37 Фосфатидилінозитоли. Досить широко розповсюджені в природі. Виявлені у тварин, рослинах і мікроорганізмах. У тваринному організмі знайдені в мозку, печінці і легенях.
Поиск по сайту: |


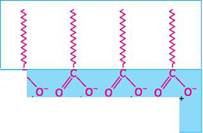
 Рис. 37.1. Будова міцели мила у воді
Рис. 37.1. Будова міцели мила у воді молекули мила зчеплюються з гідрофобними частинками забруднень своїми вуглеводневими «хвостами», утворюючи навколо таких частинок щільну ізолювальну плівку (рис. 37.3), уклинюються між забруднювальною частинкою і очищуваною поверхнею і нарешті відривають цю частинку, переводячи її в завислий стан у товщі водного середовища.
молекули мила зчеплюються з гідрофобними частинками забруднень своїми вуглеводневими «хвостами», утворюючи навколо таких частинок щільну ізолювальну плівку (рис. 37.3), уклинюються між забруднювальною частинкою і очищуваною поверхнею і нарешті відривають цю частинку, переводячи її в завислий стан у товщі водного середовища.

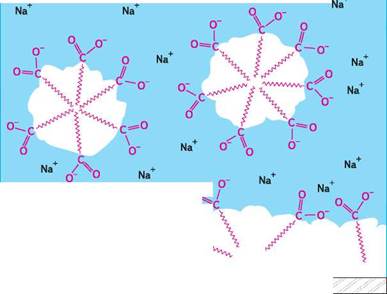 Водна фаза
Водна фаза Рис. 37.3. Схема мийної дії мила
Рис. 37.3. Схема мийної дії мила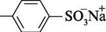


 альтернативне пальне
альтернативне пальне

 V , її
V , її