 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
ГаЛОГенОПОхІДнІ ВУГЛеВОДнІВ
нуклеофільність реагентів
Розчинник, молекули якого містять атом Гідрогену, здатний до утворення водневого зв 'язку або до взаємодії з основою, називають протонним. Протонні полярні розчинники (вода, спирти, мурашина кислота, оцтова кислота тощо) добре сольватують як катіони, так і аніони. Сольватуючи нуклеофіл, вони знижують його реакційну здатність і, отже, сповільнюють реакції, що йдуть за механізмом SN2. Розчинник, молекули якого не містять атом Гідрогену, здатний до утворення водневого зв 'язку або до взаємодії з основою, називають апротонним. Апротонні полярні розчинники (диметилформамід HCON(CH3)2, диметил-сульфоксид (CH3)2SO, ацетон CH3COCH3, ацетонітрил CH3—C3N тощо) сольватують тільки катіони, тому швидкість реакцій SN2 у них суттєво підвищується. механізм SN1 (мономолекулярне нуклеофільне заміщення).На відміну від механізму SN2, де розрив зв'язку C—Hal і утворення зв'язку С—Nu відбувається синхронно, у механізмі SN1 розрив зв'язку C—Hal передує утворенню зв'язку С—Ми. За механізмом SN1 реакція перебігає через дві стадії: Стадія І — С—Наї карбокатіон Стадія II -С+ + №Г На стадії I відбувається іонізація молекули галогеналкану з утворенням карбо-катіона і галогенід-іона. Процес іонізації проходить повільно, а тому він визначає швидкість усієї реакції. Іонізації галогеналкану сприяє розчинник. На стадії II катіон, що утворився, швидко взаємодіє з нуклеофільним реагентом, утворюючи кінцевий продукт реакції. Механізм нуклеофільного заміщення, який здійснюється за розглянутою схемою, називають мономолекулярним, оскільки на стадії, яка визначає швидкість усього процесу (стадія I), бере участь молекула лише одного реагенту — галогеналкану. Такий механізм позначають SN1. швидкість реакцій, які перебігають за механізмом SN1, залежить лише від концентрації галогеналкану та описується кінетичним рівнянням першого порядку: V = k[R— Hal]. Оптично активні третинні галогеналкани, в яких атом галогену зв'язаний з асиметричним атомом Карбону, у реакціях SN1 здебільшого утворюють раце- Глава 18 мічні форми. це зв'язано з тим, що утворений на стадії I реакції карбокатіон має площинну конфігурацію (катіонний центр перебуває в sp2-гібридизації) і може бути атакований нуклеофільним реагентом з однаковою імовірністю з обох боків площини. А це приводить до утворення рівних кількостей двох стереоізомерів, тобто до рацемізації:
К' К X—Наї К' К
К' к С— N11 Указані експериментальні дані підтверджують механізм SN1. Чинники, що сприяють перебігу реакцій за механізмом SN1. Проходженню реакцій за механізмом SN1 сприяють такі чинники: > просторові перешкоди для атаки нуклеофілом електронодефіцитного атома > здатність сполук утворювати дуже стійкі карбокатіони; > висока іонізуюча і сольватуюча здатність розчинника. За механізмом SN1 відбувається нуклеофільне заміщення в третинних і за певних умов — у вторинних галогеналканах.
У молекулі третинного галогеналкану трет-бутилброміду (CH3)3C—Br три метильні групи створюють просторову перешкоду для підступу нуклеофілу до електрофільного центру, і, отже, його атака з тилу стає неможливою. Разом з тим третинні галогеналкани в сильнополярних середовищах здатні до іонізації:
СН3 СН,— С — Вг
Сн, 1_п Ч^ІІО
як відомо, іонізація сполуки тим легша, чим стабільніші іони, що утворюються. Стійкість алкільных карбокатіонів зумовлена делокалізацією позитивного заряду за рахунок +I-ефекту алкільних груп:
СН,
сн3—сн Відносна стабільність карбокатіонів
Вплив розчинника на перебіг реакцій за механізмом SN1 зумовлений ефектом сольватації. Протонні полярні розчинники, такі як вода, спирти, мурашина
Поиск по сайту: |
 На нуклеофільність реагенту впливають замісники, зв'язані з нуклеофільним центром. електронодонорні замісники підвищують електронну густину в нуклео-фільному центрі і приводять до збільшення нуклеофільності, а електроноакцеп-торні, навпаки, знижують нуклеофільність:
На нуклеофільність реагенту впливають замісники, зв'язані з нуклеофільним центром. електронодонорні замісники підвищують електронну густину в нуклео-фільному центрі і приводять до збільшення нуклеофільності, а електроноакцеп-торні, навпаки, знижують нуклеофільність: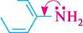 >
>
 Вплив розчинника на нуклеофільність визначається ефектом сольватації.
Вплив розчинника на нуклеофільність визначається ефектом сольватації.
 Тому утворення третинного карбокатіона для молекули енергетично вигідніше, ніж вторинного, і тим більше — первинного. Звідси третинні галогеналкани легше піддаються іонізації, ніж вторинні та первинні, і тому найбільше реакційноздатні в реакціях, які проходять за механізмом SN1.
Тому утворення третинного карбокатіона для молекули енергетично вигідніше, ніж вторинного, і тим більше — первинного. Звідси третинні галогеналкани легше піддаються іонізації, ніж вторинні та первинні, і тому найбільше реакційноздатні в реакціях, які проходять за механізмом SN1.