 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
БаГатОяДернІ арени З КОнДенСОВаними БенЗенОВими ЦиКЛами
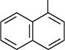
Сульфування.Нафтален піддається сульфуванню при дії концентрованої сульфатної кислоти. Суттєво впливає на напрям реакції сульфування температура реакційного середовища. Залежно від температури реакція сульфування може перебігати переважно в а- або В-положенні. Так, сульфування нафталену при температурі 80 °С призводить до утворення а-нафталенсульфокислоти, а при 160°С — переважно В-нафталенсульфокислоти:
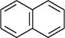
5О3Н Н2О Р -нафталенсульфокислота При нагріванні до температури 160 °С а-ізомер перетворюється в В-ізомер. У присутності 20%-вого олеуму при 40°С а-нафталенсульфокислота сульфу-ється далі, утворюючи суміш 1,5- і 1,6-нафталендисульфокислот. Галогенування.Нафтален хлорується при температурі 90—110°С в присутності ферум(III) хлориду з утворенням переважно а-хлоронафталену. Бромування нафталену в а-положення проходить легко за відсутності каталізатора:
С12; РеС13
Вг2; СС14;
а-хлоронафтален Вг
а-бромонафтален алкілювання та ацилювання.У присутності кислот льюїса (AlCl3, SnCl4 тощо) нафтален взаємодіє з галогеналканами і галогенангідридами карбонових кислот з утворенням суміші а- і В-заміщених ізомерів. РЕАКЦІЇ ПРИЄДНАННЯ Нафтален значно легше, ніж бензен, вступає в реакції приєднання, тому що зв'язки між а- і В-атомами Карбону в молекулі нафталену мають більшу ненаси-ченість, ніж зв'язки СС у бензені. Так, при звичайній або пониженій температурі за відсутності каталізатора нафтален приєднує молекулу хлору з утворенням продукту 1,4-приєднання: Глава 15
Н' СІ 1,4-дигідро-1,4-дихлоронафтален Розглянута раніше (див. с. 219) реакція бромування нафталену відбувається за схемою приєднання—відщеплення, тобто спочатку бром приєднується в положення 1 і 4, а потім продукт приєднання при нагріванні відщеплює бромоводень, утворюючи а-бромонафтален:
Вг Н Вг
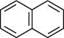
Вг2 Ґ^\ґ\\ Н Вг 1,4-дибром-1,4-дигідронафтален а-бромонафтален У присутності каталізатора М нафтален значно легше, ніж бензен, приєднує водень. Процес гідрування нафталену проходить ступінчасто. Спочатку при температурі 150°С утворюється 1,2,3,4-тетрагідронафтален (тетралін), який при 200°С гідрується далі з утворенням декагідронафталену (декаліну):
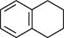
; 150 °С Н/ЇЧі; 200 °С
тетралін декалін ОКИСНЕННЯ Нафтален окиснюється набагато легше, ніж бензен. Залежно від умов окис-нювання утворюються різні продукти. При окисненні нафталену киснем повітря в присутності каталізатора V2O5 утворюється ангідрид фталевої кислоти. Дією хром(VI) оксиду в оцтовій кислоті нафтален окиснюється до 1,4-нафтохінону:
фталевий ангідрид 1,4-нафтохінон Слід зазначити, що при окисненні гомологів нафталену, на відміну від гомологів бензену, більш чутливе до дії окисників нафталенове ядро:
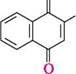
СгО3; СН3СООН р -метилнафтален 2-метил-1,4-нафтохінон БаГатОяДернІарени З КОнДенСОВаними БенЗенОВими ЦиКЛами
Поиск по сайту: |
 8О3Н
8О3Н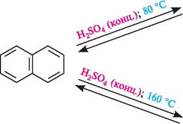 Н2О
Н2О

 -на
-на
 -НВг
-НВг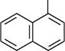
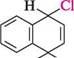 + Сі,
+ Сі,


 О
О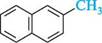
 О
О