|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
БаГатОяДернІ арени З ІЗОЛЬОВаними БенЗенОВими ЦиКЛами
N81411,
трифенілметилнатрій
С12
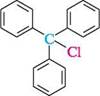
трифенілхлорометан
[ ] трифенілметанол Трифенілметилнатрій має іонну будову. його молекула складається з катіона Натрію і трифенілметил-аніона. етерові розчини трифенілметилнатрію проводять електричний струм. Атом галогену в молекулі трифенілхлорометану і гідроксильна група в молекулі трифенілметанолу під впливом електроноакцепторних властивостей трьох бензе-нових кілець виявляють високу рухливість (активність). Так, трифенілхлорометан у рідкому SO2 (розчинник з високою діелектричною сталою) у присутності AlCl3 піддається іонізації з утворенням трифенілметил-катіона. Аналогічно відбувається іонізація трифенілметанолу в концентрованій сульфатній кислоті:
трифенілхлорометан
8О2 (рідк.) + А1С1, Н28О4 (конц.) + аісі; Н8О Н2О трифенілметанол Глава 16 Здатність трифенілметильної групи утворювати стійкі карбокатіони і карб-аніони зумовлена участю бензенових циклів у делокалізації позитивного або негативного заряду іона за рахунок кон'югації:
трифенілметил-катіон трифенілметил-аніон Однак, незважаючи на те що центральний атом Карбону в трифенілметил-катіоні і трифенілметил-аніоні перебуває в sp2 -гібридизованому стані, зазначені іони мають не площинну, а пропелероподібну структуру, в якій бензенові цикли вивернуті з площини на 30—40°. Таке розміщення бензенових кілець у просторі пов'язане зі стеричною взаємодією атомів Гідрогену в орто-положеннях (рис. 16.1).
Рис. 16.1. Просторова будова: а — трифенілметил-катіона; б — трифенілметил-аніона Саме тому кон'югація центрального атома Карбону з кожним ядром дещо менша, ніж можна було б очікувати при площинній структурі. При обробці трифенілхлорометану цинком, натрієм або тонкоздрібленим сріблом у бензеновому розчині утворюється вільний трифенілметильний радикал, що знаходиться в рівновазі зі своїм димером:
трифеніл-хлорометан трифенілметил-радикал похідна цикпогексадієну Уперше вільний трифенілметил-радикал було отримано 1900 року американським хіміком Мозесом Гомбергом при вивченні хімічних властивостей трифеніл- БаГатОяДернІ арени З ІЗОЛЬОВаними БенЗенОВими ЦиКЛами хлорометану. це був перший з радикалів, виділений у вільному вигляді. Причина такої високої стійкості трифенілметил-радикала порівняно з алкільними радикалами полягає в значній делокалізації неспареного електрона по всіх бензенових ядрах.
Трифенілметил-радикал дуже реакційноздатна речовина: на повітрі легко окиснюється, утворюючи трифенілметил пероксид (C6H5)3C—O—O—C(C6H5)3, з металічним натрієм — трифенілметилнатрій (С6Н5)3СГІчГа+, з йодом — йодотри-фенілметан (C6H5)3C—І. Трифенілметильний катіон, аніон і радикал мають характерне забарвлення: трифенілметил-катіон — червоно-оранжеве, трифенілметил-аніон — червоне, а вільний трифенілметил-радикал — жовте. Появу забарвлення в зазначених іонах і вільному радикалі зумовлює наявність в їхній структурі довгої кон'югованої системи (хромофору), що включає три бензенових цикли. Похідні трифенілметану знайшли широке практичне застосування як барвники і лікарські препарати.
Поиск по сайту: |

 -гш.
-гш.

 -неї
-неї