|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
ГетерОФУнКЦІОнаЛЬнІ КарБОнОВІ КиСЛОти. з утворенням ацетондикарбонової і мурашиної кислот
сн2— соон но—с— соон сн2— соон Н28О4 (конц.); і сн2—соон
+ нсоон сн2— соон
Н2О сн3—с —сн3 о Солі та естери лимонної кислоти називають цитратами. ОН ЙаООС — СН2—С—СН2— СО(Ша+ СО(Жа+ натрій цитрат Тринатрієву сіль лимонної кислоти (натрій цитрат) використовують у медицині для консервування донорської крові. ФЕНОЛОКИСЛОТИ Фенолокислотами називають похідні аренкарбонових кислот, в яких один або кілька атомів Гідрогену в ароматичному кільці заміщені на гідроксильні групи. Найбільш важливі представники фенолокислот:
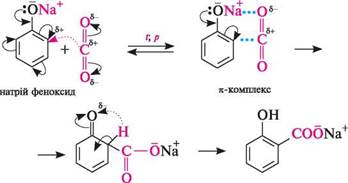
СПОСОБИ ДОБУВАННЯ Багато фенолокислот містяться у вільному стані або у вигляді естерів у рослинах, з яких їх можна виділити індивідуально. Галову кислоту одержують у результаті гідролізу дубильних речовин. Синтетичні методи добування фенолокислот ґрунтуються на введенні в структуру фенолів карбоксильної групи (карбоксилювання фенолів) або введенні в молекулу аренкарбонової кислоти фенольного гідроксилу (гідроксилювання ароматичних кислот). Карбоксилювання фенолів карбон(IV) оксидом(реакція Кольбе—Шмітта). При дії карбон(IV) оксиду на натрій феноксид при температурі 120—140 °С і тиску 5 атм утворюється натрій саліцилат, який потім переводять у саліцилову кислоту: Глава 27
СО2; ґ, р ОН он СООН
натрій феноксид натрій салііщлат саліцилова кислота Реакція перебігає за механізмом SЕ. Оскільки карбон(IV) оксид виявляє слабкі електрофільні властивості, у реакції використовують не сам фенол, а натрій феноксид, в якому за рахунок +М-ефекту з боку негативно зарядженого атома Оксигену бензенове кільце в реакціях SE більш активне, ніж у фенолу.
он СООН
п-комгшекс натрій саліцилат саліцилова кислота При більш високих температурах, і особливо якщо використовувати калій феноксид як основний продукт реакції, утворюється 4-гідроксибензойна кислота. Гідроксилювання аренкарбонових кислот. При нагризанні основних мідних солей ароматичних карбонових кислот відбувається гідроксилювання ароматичного ядра в орто-положенні:
Си(ОН)2 -NаОН саліцилова кислота Сплавлення сульфобензойних кислот з лугами. При сплавленні сульфобензойних кислот з лугами сульфогрупа заміщується на гідроксильну групу:
КОН (сплавлення) соок ОК н+ СООН Н
л-сульфобензойна кислота ж-гідроксибензойна кислота ГетерОФУнКЦІОнаЛЬнІ КарБОнОВІ КиСЛОти ХІМІЧНІ ВЛАСТИВОСТІ Реакційна здатність гідроксикислот зумовлена наявністю в їх структурі карбоксильної групи, фенольного гідроксилу та ароматичного ядра. За участі карбоксильної групи гідроксикислоти утворюють різні функціональні похідні — солі, галогенангідриди, естери тощо. Так, аналогічно аренкарбоновим кислотам при дії на гідроксикислоти лугів, гідрокарбонатів або карбонатів лужних металів утворюються солі. При цьому з гідрокарбонатами або карбонатами лужних металів у реакцію вступає тільки карбоксильна група. Фенольний гідроксил, маючи слабші кислотні властивості, ніж карбонатна кислота, не здатний витісняти її із солей: соон
он саліцилова кислота + соо
ОН натрій саліцилат СО2! + Н2О При дії на фенолокислоти лугів утворюються солі як по карбоксильній групі, так і по фенольному гідроксилу (феноляти):
ОН + 2Ш0Н СОО + 2Н2О
саліцилова кислота динатрієва сіль саліцилової кислоти При взаємодії фенолокислот зі спиртами утворюються естери, з галогенуючими реагентами (PCl5, POCl3, SOCl2) — галогенангідриди:
мегилсаліцилат он хлорангідрид саліцилової кислоти Завдяки фенольному гідроксилу фенолокислоти здатні утворювати етери та естери. При ацетилюванні саліцилової кислоти оцтовим ангідридом утворюється ацетилсаліцилова кислота (аспірин):
он + (СН3СО)2О ацетилсаліцилова кислота Подібно до фенолів фенолокислоти утворюють із ферум(III) хлоридом фіолетове забарвлення. Глава 27 476 Г Фенолокислоти подібно до аренів вступають у реакції електрофільного заміщення по ароматичному ядру. При нітруванні саліцилової кислоти нітруючою сумішшю за м'яких умов утворюється 2-гідрокси-5-нітробензойна кислота:
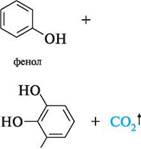
(конц.); Н25О4 (конц.) ^ -Н2О ОН ^ "ОН 2-гідрокси-5-нітробензойна кислота При нагріванні фенолокислоти досить легко піддаються декарбоксилюванню:
но но галова кислота пірогалол ОКРЕМІ ПРЕДСТАВНИКИ. ВИКОРИСТАННЯ Саліцилова (о-гідроксибензойна) кислота. Біла кристалічна речовина (т. пл. 159°С), легко сублімується, при сильному швидкому нагріванні декарбоксилю-ється, розчинна в гарячій воді. хоон
он Саліцилова кислота виявляє вищу кислотність (рКa = 2,98), ніж бензойна кислота (рKa = 4,17), а також мета- або пара-гідроксибензойні кислоти. Підвищена кислотність саліцилової кислоти зумовлена додатковою стабілізацією аніона завдяки утворенню внутрішньомолекулярного водневого зв'язку:
Саліцилова кислота використовується в медицині у вигляді спиртових розчинів та мазей як антисептичний лікарський засіб. Вона також слугує сировиною для синтезу інших лікарських засобів, таких як натрій саліцилат, метилсалі-цилат, фенілсаліцилат (салол), саліциламід, оксафенамід, ацетилсаліцилова кислота (аспірин). Хімічні перетворення, пов'язані із синтезом цих лікарських препаратів, зображено на схемі:
Поиск по сайту: |


 .он А. ^ он
.он А. ^ он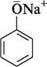

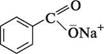

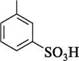
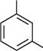
 СООН
СООН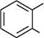

 СООН
СООН
 он
он
 СООН
СООН СООН О21Чк ^ ХООН
СООН О21Чк ^ ХООН
 хоон
хоон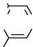 СО2І
СО2І