 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
НОМЕНКЛАТУРА. ІЗОМЕРІЯ. За замісною номенклатурою ШРАСназви первинних амінів утворюють шляхом додавання до
За замісною номенклатурою ШРАСназви первинних амінів утворюють шляхом додавання до назви вуглеводню суфікса -амін, указуючи положення аміногрупи у вуглецевому ланцюзі. При складанні назв вторинних і третинних амінів їх розглядають як похідні первинного аміну з замісниками при атомі Нітрогену. За вихідний первинний амін у цьому випадку приймають зв'язаний з атомом Нітрогену найбільш складний за структурою радикал. Інші вуглеводневі замісники при атомі Нітрогену перелічують за алфавітним порядком із зазначенням локанта N-: сн3— сн — сн3 сн3— ічн— с2н5 сн3— N — сн2— сн2— сн3 2-пропанамін К-метилетанамін М-етил-ІМ-метил-і-пропанамін якщо сполука містить дві або три аміногрупи, то в назві їх позначають множними префіксами ді- або три-, які ставлять перед суфіксом -амін: н2к—сн2—сн2— сн2— сн2— *щ2 1,4-бутандіамін Найпростіші аміни найчастіше називають за радикало-функціональною номенклатурою. За цією номенклатурою назви амінів утворюють з назв вуглеводневих радикалів, які перелічують за алфавітним порядком, і суфікса -амін: АмІни с2н5 С2Н5— СН3— N11—С2Н5 С2Н5—К—С2Н5 СН3—СН2—СН—СН3
етилметиламш сн3— сн—сн2— сн3 сн3 ізобутиламін яі/>ет-бутиламін
кн втор- бутиламш сн2—
анілін толуїдини (о-, м-, п-) анізидини (о-, м-, п-) фенетидини (о-, л*-, п-) фенілендіаміни (о-, м-, п-)
бензидин Назви первинних ароматичних амінів, а також змішаних амінів зазвичай утворюють на основі назви представника родоначальної структури — аніліну. У разі змішаних амінів положення замісників при атомі Нітрогену позначають за допомогою локанта N-:
сн,
Вторинні і третинні ароматичні аміни, як правило, називають за радикало-функціональною номенклатурою:
дифеніламін трифеніламін Ізомерія амінів зумовлена різною структурою вуглеводневих радикалів, різним положенням аміногрупи і метамерією. Суть метамерії полягає в тому, що аміни з однією і тією ж брутто-формулою можуть бути первинними, вторинними і третинними. Наведені нижче сполуки є метамерами:
^з сн3—кн—сн2—сн3 етилметиламш Глава 20 20.2. АЛКІЛ аміНИ Алкіламінами називають продукти заміщення одного, двох або трьох атомів Гідрогену в амоніаку алкільними групами. СПОСОБИ ДОБУВАННЯ Взаємодія галогеналканів з амоніаком(реакція Гофмана).При нагріванні спиртового розчину амоніаку з галогеналканами утворюється суміш первинного, вторинного та третинного амінів і сіль четвертинної амонієвої основи. цю реакцію відкрив 1850 року німецький хімік Август Вільгельм Гофман. Спочатку амоніак з галогеналканом утворює сіль алкіламонію, яка в надлишку амоніаку перетворюється в первинний алкіламін: _ СН3І+ 1ЧН3 ------*► [СН3ЇЧН3]І метиламоній йодид метиламін Первинний амін, що утворився, реагує з наступною молекулою галогеналкану і т. д. У результаті утворюється вторинний амін, потім третинний і сіль четвертинної амонієвої основи:
СН3І СН3І [(СН3)2КН2]Г диметиламоній йодид [(СН3)3КН]Г триметиламоній йодид [(СН3)4А]Г тетраметиламоній йодид ТШ триметиламін При значному надлишку амоніаку збільшується вихід первинного аміну, у разі надлишку галогеналкану в суміші переважає сіль четвертинної амонієвої основи. Утворену суміш первинних, вторинних і третинних амінів розділяють фракційною перегонкою. Синтез Габріеля.Метод дозволяє одержати первинні алкіламіни. Він ґрунтується на взаємодії калій фталіміду з галогеналканами і подальшим гідролізом утвореного N-алкіл фталіміду:
]Ч-етилфталімід хоон СООН фталева кислота Відновлення нітроалканів і нітрилів.При відновленні нітроалканів і нітрилів утворюються первинні аміни. Відновлення проводять воднем у присутності каталізатора (Ni, Pd, Pt) або воднем у момент виділення. амІни
2Н2О
СН3—К02 + ЗН2
нітрометан
4-^ХІ.т \_^---------- 14 ацєтонітрил розщеплення незаміщених амідів карбонових кислот натрій гіпобромітом (перегрупування Гофмана). При обробці незаміщених амідів карбонових кислот натрій гіпобромітом (або сумішшю брому і натрій гідроксиду) утворюються первинні аміни, в яких на один атом Карбону менше, ніж у вихідному аміді:
амід протеїнової кислоти
—*- сн3—сн2—
Поиск по сайту: |




 Деякі аміни зберігають тривіальні назви:
Деякі аміни зберігають тривіальні назви:



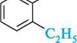 /снз
/снз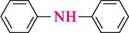

 сн3і
сн3і

