 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
МЕЗОМЕРНИЙ ЕФЕКТ (ЕФЕКТ КОН'ЮГАЦІЇ)
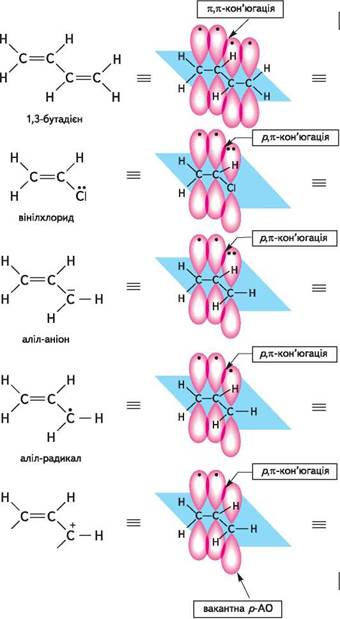
Більш ефективно відбувається передача електронного впливу замісника по кон'югованій (спряженій) системі. Кон'югованою називають систему, що складається з простих і кратних зв'язків, які чергуються, або ж коли поруч з атомом Карбону, що утворює кратний зв'язок, знаходиться атом, р-АО якого заповнена одним, двома електронами або вакантна. Кон'юговані системи поділяються на системи з відкритим і замкненим ланцюгами: н2с=сн—сн=сн2 н2с=сн—с=сн н2с=сн—с=к 1,3 -бутадієн вінілацетилен акрилонітрил
н2с=сн—сі н2с=сн—о—сн=сн2 бензен вінілхлорид дивініловий етер н2с=сн—сн2 н2с=сн—сн2 н2с=сн—сн2 аліл-аніон аліл-радикал аліл-катіон У кон'югованих системах має місце кон'югація (спряження) зв'язків — додаткове перекривання п- або р-орбіталей замісника з п-орбіталями зв'язків вуглецевого ланцюга або ароматичного кільця. Кон'югація зв'язків зумовлює утворення єдиної делокалізованої електронної хмари. ВЗаЄмниЙ ВПЛиВ атОмІВ В ОрГанІЧних СПОЛУКах Розрізняють (рис. 4.1) я,я-кон'югацію (перекривання двох я-орбіталей) і ^,я-кон'югацію (перекривання р- з я-орбіталлю). Кон'югація можлива лише у випадку паралельності осей симетрії (компланарності) взаємодіючих орбіталей.
делокалізована я-система
Рис. 4.1. Кон'юговані системи 1,3-бутадієну, вінілхлориду й алільного аніона, радикала та катіона Кон'югація для молекули — це енергетично вигідний процес. Вона супроводжується зменшенням енергії системи і приводить до підвищення термодинамічної стійкості молекули. Глава 4 Процес передачі електронного впливу замісника по кон'югованій системі п-зв'язків називають мезомерним ефектом (М), або ефектом кон'югації. Мезомерний ефект виявляється лише в тому випадку, якщо замісник входить у кон 'юговану систему молекули. У молекулі аніліну аміногрупа входить у кон'юговану систему і виявляє мезомерний ефект. У молекулі бензиламіну аміногрупа ізольована від кон'югованої системи ароматичного кільця двома 5-зв'язками і не виявляє мезомерного ефекту.
анілін бензиламін Мезомерний ефект позначають символом М, а зміщення електронної густини в кон'югованій системі — вигнутою стрілкою (). Початок стрілки вказує, які саме електрони зміщуються, а кінець стрілки — зв'язок або атом, до яких спрямоване зміщення. Розрізняють позитивний (+М) і негативний (-М) мезомерні ефекти. Позитивний мезомерний ефект виявляють замісники, які надають електрони в кон'юговану систему. +М-ефект виявляють атоми, що містять неподілені пари електронів або несуть негативний заряд, а також атомні групи, які мають на першому атомі неподілені електронні пари або негативний заряд. Негативний мезомерний ефект виявляють замісники, які зміщують на себе електронну густину кон'югованої системи. —М-ефект виявляють замісники, перший атом яких несе позитивний заряд, а також атомні групи, в яких перший атом пов'язаний з більш електронегативним атомом кратним зв'язком. Нижче наведені деякі замісники, розташовані за порядком зменшення +М- або -М- ефектів.
І і
група А виявляє —М-ефект група В виявляє +М-ефект
— N1^ , — С=ічГ, ч
>гі=п —г^ — о
Максимальний негативний мезомерний ефект виявляють замісники, що несуть позитивний заряд. -М-ефект ненасичених угруповань тим більший, чим більша різниця електронегативностей атомів, сполучених кратним зв'язком. Максимальний позитивний мезомерний ефект мають атоми, які несуть негативний заряд. +М-ефект замісників, що містять атоми з неподіленими парами ВЗаЄмниЙ ВПЛиВ атОмІВ В ОрГанІЧних СПОЛУКах
—іїн2 > —он > — р У межах групи періодичної системи +М- ефект замісників слабшає зверху вниз (—F > —Сl > —Br), що пояснюється більшою енергетичною вигідністю при перекриванні близьких за розмірами р-орбіталей. Розрізняють чотири основних типи виявлення мезомерного ефекту в органічних сполуках. 1. Взаємодія замісника, щовиявляє +М-ефект, з %-електронною системою молекули: С Н2С—С +М-ефект \^ +М-ефект вінілметиловий етер фенол 2. Взаємодія замісника, що виявляє —М-ефект, з и-електронною системою молекули:
—М-ефект —М-ефект
3. Взаємодія двох замісників з +М- і —М-ефектом, безпосередньо зв'язаних \Х>: -М-ефект '•■ ІОНІ +М-ефект оцтова кислота 4. Взаємодія замісників, що виявляють +М- і —М-ефект, через п-електронну систему молекули:
4-амінобензальдегід На відміну від індуктивного ефекту передача електронного впливу замісника в кон'югованій системі відбувається на значно більшу відстань, практично не згасаючи.
Поиск по сайту: |



 делокалізована я-система
делокалізована я-система




 електронів, тим більший, чим менша в межах періоду електронегативність атома, який несе неподілену електронну пару:
електронів, тим більший, чим менша в межах періоду електронегативність атома, який несе неподілену електронну пару: нос=0:н—Е=ічІ
нос=0:н—Е=ічІ акрилонітрил нітробензен
акрилонітрил нітробензен


 +М-ефект —М-ефект
+М-ефект —М-ефект