 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Формули Коллі—Толленса
СН2ОН напшацетальнии гідроксил (глікозидний) Формули Хеуорса
І І.НО|-С—Н
-он о -он СН7ОН р-Х)-глюкофураноза Аналогічно зображують за допомогою формул Хеуорса піра-нозні та фуранозні форми кетогексоз:
а-/>-фруктопіраноза При зображенні суміші а- і Р-аномерів у формулі Хеуорса символ атома Гідрогену в глікозидного атома Карбону випускають, а розміщення гідроксильної групи позначають хвилястою лінією: Їуглеводи
он но н он і)-глкжопіраноза Таутомерія.Моносахариди є таутомерними речовинами. У кристалічному стані вони мають циклічну будову. Так, І)-глюкоза, одержана дробною кристалізацією з етилового спирту або води, знаходиться у формі а-і)-глюкопіранози. У водному розчині циклічна форма під дією розчинника перетворюється через відкриту оксоформу на інші циклічні форми — піранозні та фуранозні з а- і ^-конфігурацією аномерного центру. Тому у водному розчині моносахариди існують у вигляді п'яти таутомерних форм — відкритої, а- та (3-піранозних і а- та 3-фуранозних.
і>-глкжоза н он н он р-Х>-глюкофураноза р-і)-глюкопіраноза Такий вид таутомерії називається цикло-оксо-таутомерією, або кільчасто-ланцюговою таутомерією. Перехід однієї форми в інші відбувається безперервно. Згодом у розчині встановлюється рухома (динамічна) рівновага, за якої кількість усіх форм залишається постійною. У рівноважній суміші таутомерів альдогексоз переважають піранозні форми. Наприклад, рівноважна система І)-глюкози складається з 64 % р-2)-глюкопі-ранози і близько 36 % — а-І>-глюкопіранози. Фуранозні та відкрита форми присутні в дуже малих кількостях. Аналогічні таутомерні перетворення відбуваються у водних розчинах кетоз. Нижче наведено схему г<и/о20-<жс0-таутомерії 2?-фруктози. Глава 22
он н
а-І>-фруктофураноза
он н р-.0-фруктофураноза
У рівноважній системі таутомеріє І>-фруктози переважають фуранозні форми. Здатність моносахаридів до цикло-оксо-таутомерп пояснює виявлене задовго до встановлення їхньої будови явище мутаротації. Мутаротація (від лат. тиіо — змінюю і гоїаііо — обертання) — тимчасова зміна величини оптичного обертання свіжоприготованих розчинів оптично активних сполук. Наприклад, у свіжоприготованому водному розчині глюкози спостерігається зменшення кута оптичного обертання від +113° до постійного значення +52,5°. Хімічною основою цього процесу є цикло-оксо-гаутомерїя. Конформації'моносахаридів.Фуранозні форми моносахаридів мають практично плоску просторову будову, а тому замісники в п'ятичленному циклі змушені знаходитися в нестійкій заслоненій конформації. Для піранозних циклів найвигіднішою формою, що відповідає мінімуму енергії, є форма крісла, в якої замісники знаходяться в конформації, близькій до загальмованої. Тому фуранозні форми моносахаридів термодинамічно менш вигідні, ніж піранозні.
НО форма крісла форма крісла Вуглеводи -------------------------------------------------------------------------------------------------- 405 СПОСОБИ ДОБУВАННЯ Вуглеводи дуже поширені в природі. Вони утворюються в зелених частинах рослин з вуглекислого газу та води в процесі фотосинтезу. «со2 + «н2о мороф1л ■ №Д + «о2 Найважливішим способом здобування моносахаридів є кислотний гідроліз природних ди- і полісахаридів. Так, /)-глюкозу добувають гідролізом крохмалю, суміш І)-глкжози з і)-фруктозою — гідролізом сахарози і т. д. Синтетичні методи застосовують звичайно для здобування малодоступних моносахаридів. У більшості випадків ці методи ґрунтуються на перетворенні моносахаридів, які легко виділяються з природних джерел (2)-глюкоза, £>-галактоза, і)-маноза та інші), на інші моносахариди шляхом скорочення або подовження карбонового ланцюга. Альдольна конденсація формальдегіду.В 1861 році О. М. Бутлеров здійснив перший синтез цукристої речовини, коли пропустив формальдегід крізь розчин вапняного молока: їгіл п Са(ОНЬ , г но ФІЗИЧНІ ВЛАСТИВОСТІ Моносахариди — тверді гігроскопічні речовини, легко розчинні у воді, важко розчинні в етанолі та практично нерозчинні в діетиловому етері, бензені, діоксані. Значна частина моносахаридів — кристалічні речовини. Водні розчини моносахаридів мають, як правило, солодкий смак і нейтральну реакцію. У розчинах молекули моносахаридів сильно сольватовані, що приводить до утворення в'язких «сиропів», в яких процес кристалізації значною мірою уповільнюється. Кристали багатьох моносахаридів складаються з молекул у пі-ранозній формі. Розчини моносахаридів оптично активні. ХІМІЧНІ ВЛАСТИВОСТІ Будучи полігідроксикарбонільними сполуками, моносахариди виявляють хімічні властивості карбонільних сполук, багатоатомних спиртів, а також циклічних напівацеталів. Глава 22
Хімічні перетворення в ряду моносахаридів можна умовно поділити на дві групи: реакції з участю відкритих форм моносахаридів і реакції з участю циклічних форм. А. Реакції з участю відкритих форм Відновлення.При відновленні моносахаридів воднем у присутності каталізатора (нікель, паладій) утворюються багатоатомні спирти. З Х)-глюкози при цьому утворюється спирт — £)-сорбіт, з £-манози — /)-маніт, з /)-ксилози — і)-ксиліт і т. д.
Н\^о
н- но- н- СН2ОН Х>-ксилоза [Н] СН2ОН -он -н -он сн2он .0-ксиліт нХ(/о -он -н -он -он сн2он .0-глюкоза [Н] СН2ОН -ОН -н -он -он СН2ОН .О-сорбіт і)-Ксиліт і і)-сорбіт — кристалічні речовини, солодкі на смак, їх вживають при цукровому діабеті як замінники цукру. і)-Сорбіт є проміжним продуктом у промисловому синтезі аскорбінової кислоти з 2)-глюкози. При відновленні І)-фруктози утворюється суміш /)-сорбіту та /)-маніту.
СН2ОН =0 -н -он -он сн2он .0-фруктоза [Н] СН2ОН -ОН -Н -ОН -он СН2ОН #-сорбіт СН2ОН -н -н -он -он сн2он /)-маніт Окиснення.Моносахариди легко окиснюються, проте, залежно від природи окисника та умов окиснення, утворюють різні продукти. У кислому та нейтральному середовищі окиснення відбувається без руйнування карбонового ланцюга молекули, а в лужному середовищі звичайно воно супроводжується розщепленням карбонового скелета. Окиснення в кислому і нейтральному середовищі.При використанні слабких окисників, наприклад бромної води або розведеної
Вуглеводи нітратної кислоти, альдози окиснюються з утворенням однооснов-них поліоксикислот, які дістали загальну назву альдонові кислоти. І>-Глюкоза за цих умов дає /)-глюконову кислоту, ^-галактоза — /)-галактонову кислоту і т. д.
•V0 -он -н -он -он СН2ОН .0-глюкоза . НВЮ (Вг2 + Н2Р) но\^°
-он -н -он -он СН2ОН
СОО- іСа2+
ОН Н ОН ОН ■ СН2ОНІ2 кальцій глюконат Сильні окисникі, наприклад концентрована НNОз, окисню-ють у молекулі альдоз альдегідну і первинну спиртову групи з утворенням дикарбонових кислот, які дістали загальну назву альдаро-ві, або цукрові кислоти. Так, 2>-глюкоза окиснюється в і>-глюкарову кислоту: Н\^о
Н- но-н-н- сн2он />-глкжоза конц. НМ03
соон он н он он соон Х>-глюкарова кислота, />-цукрова кислота При окисненні кетоз за аналогічних умов відбувається розрив карбонового ланцюга за місцем карбонільної групи з утворенням дикарбонової кислоти.
сн,он с=о -н -он -он СН2ОН /)-фруктоза конц. НNОз -со,
соон -н -он -он соон />-арабінарова кислота Глава 22
Окиснення в лужному середовищі. Подібно до альдегідів моносахариди окиснюються амонііачним розчином аргентум (І) оксиду і купрум (II) гідроксидом у лужному розчині. У ці реакції вступають як альдози, так і кетози, тому що в лужному середовищі кетози ізомеризуються в альдози. У першому випадку відбувається реакція «срібного дзеркала». У другому — утворюється купрум (І) оксид оранжевого кольору. Моносахариди при окисненні в лужному середовищі розщеплюються до суміші продуктів окиснення. Ці реакції є якісними на альдози і кетози:
К—С—Н + [Ав(Ш3)2]ОН альдоза д„і + продукти окиснення
о К—С—Н + Си (комплекс) Си20| + продукти окиснення Спрощено цей процес можна зобразити так: І (СНОН)4 + А§20 >ш, Чс/он (СНОН)4 + 2А§
СН2ОН глюкоза СН2ОН глкжонова кислота
І (СНОН)4 + Си(ОН)2 ОН',? °С чс/он І (СНОН)4 + СиОН
СН2ОН СН2ОН
2СиОН і °С - Си20 +Н20 Вуглеводи
Поиск по сайту: |
 нашвацетальний гідроксил
нашвацетальний гідроксил
 )Н Н
)Н Н

 сн2он
сн2он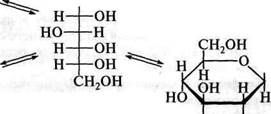
 V
V
 НОН2С
НОН2С
 НОН2С
НОН2С