 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
КЛАСИФІКАЦІЯ ТА НОМЕНКЛАТУРА. Моносахариди класифікують, зважаючи на дві ознаки: характер оксогрупи (альдегідна
Моносахариди класифікують, зважаючи на дві ознаки: характер оксогрупи (альдегідна або кетонна) і довжину карбонового ланцюга. Залежно від наявності в структурі моносахаридів альдегідної або кетонної групи їх поділяють на альдози і кетози. За кількістю атомів Карбону в молекулі моносахариди класифікують на триози (С3), тетрози (С4), пентози (С5), гексози (С6) і т. д. Моносахариди, до складу яких входить понад шість атомів Карбону, називають вищими цукрами. Більшість природних моносахаридів є пентозами і гексозами. Звичайно при класифікації зважають вод- Глава 22 ночас на обидві класифікаційні ознаки, наприклад, альдопентоза, альдогексоза, кетопентоза, кетогексоза.
■
•с^° НОН нон 4СНОН 5СН2ОН альдопентоза н. 2) 2СНОН 3СНОН 4СНОН 5СНОН 6СН2ОН альдогексоза 6СН2ОН кетогексоза У назвах моносахаридів, як правило, користуються тривіальною номенклатурою. Усі тривіальні назви мають закінчення -оза, наприклад, глюкоза, фруктоза, галактоза, рибоза та ін. Номенклатуру ШРАС до назв вуглеводів практично не застосовують. СТЕРЕОІЗОМЕРІЯ Молекули моносахаридів містять декілька асиметричних атомів Карбону, і тому вони існують у вигляді різних просторових ізомерів. Наприклад, альдопентоза має 3 асиметричні атоми Карбону, тому тій же самій структурній формулі відповідає вісім стереоізомерів (23), альдогексоза містить 4 асиметричні атоми Карбону і може існувати у вигляді 24 = 16 стереоізомерів (N=2", де п — кількість асиметричних атомів Карбону). Для зображення стереоізомерів на площині користуються проекційною формулою Фішера. Усі ізомери моносахаридів поділяють на і)- і ^-стереохімічні ряди, належність до яких визначається конфігурацією асиметричного атома Карбону, максимально віддаленого від карбонільної групи (для пентоз — С4, для гексоз — С5). Якщо конфігурація цього хірального атома Карбону збігається з конфігурацією ^-гліцеринового альдегіду, то моносахарид відносять до .О-ряду, якщо ж із конфігурацією £-гліце-ринового альдегіду, — то до І-ряду, наприклад:
Вуглеводи Н. •4* н. -^
-—ОН: СН2ОН 2>-гліцериновий альдегід -—он; СН2ОН і-гліцериновий альдегід
&
Н^ но-^ н^ 6СН2ОН Д-глюкоза СН2ОН =0 -н -он -он 6СН2ОН £>-фруктоза ь<
н-но-но- СН20Н І-арабіноза СН2ОН
н4 іно-^ 6сн2он і-сорбоза Так, із 16 стереоізомерів альдогексози 8 належать до 2)-ряду, а 8 — до і-ряду. Представники 2)-ряду є оптичними антиподами Х-ряду, тобто альдогексоза існує у вигляді 8 пар енантіомерів. Наприклад, енантіомерами є О-глюкоза і і-глюкоза.
^ ■^
н- но- н- н- СН2ОН .О-глюкоза но- н- но- но- сн2он і-глюкоза Переважна більшість природних моносахаридів належать до -О-ряду. Найважливішими природними моносахаридами є:
^ -он -он -он сн2он 2>-рибоза
а.
н- но- н- сн2он />-ксилоза
в.
н-но-но- сн2он І-арабіоза
Глава 22 СН2ОН
І 2 с=о Но—І—н
н—^он
Н-4-ОН СН2ОН
/)-фруктоза Просторові ізомери моносахаридів, які відрізняються конфігурацією одного або декількох атомів Карбону і не належать до дзеркальних ізомерів (енантіомерів), називаються діастереомерами. Так, 2)-глюкоза і />-галактоза, £-маноза і 5-глюкоза, 2?-маноза і 2?-га-лактоза складають пари діастереомерів. Діастереомери, що відрізняються конфігурацією тільки одного асиметричного атома Карбону, називають епімерами. Наприклад, І)-глюкоза і /^-галактоза, а також І>-глюкоза і І>-маноза складають пари епімерів. Отже, епімерія є окремим випадком діастереомери. Найважливішою властивістю речовин, молекули яких мають асиметричний атом Карбону або асиметричні в цілому, є їх здатність обертати площину поляризованого променя світла (див. розд. 20.2.2). Тому моносахариди виявляють оптичну активність. Обертання площини поляризованого світла вправо позначають знаком (+), а вліво — знаком (-). Однак слід пам'ятати, що напрямок обертання визначається експериментально і зовсім не пов'язаний з конфігурацією, тобто належністю до 2>- або Х-ряду.Так, форма 2)-глюкози, яка зустрічається в природі, є правообертальною, а природна форма £>-фруктози — лівообертальною. БУДОВА МОНОСАХАРИДІВ Тривалий час у науці панувала думка, нібито моносахариди є сполуками з відкритим карбоновим ланцюгом, містять у своєму складі альдегідну або кетонну групу і кілька спиртових гідроксилів. Однак при подальшому вивченні їх будови було встановлено, що деякі властивості моносахаридів не узгоджуються з цими твердженнями. Так, виявилося, що моносахариди, будучи альдегідами, не дають деяких реакцій на альдегідну групу. Зокрема, вони не утворюють за звичайних умов гідросульфітні похідні, не дають забарвлення з фуксинсульфітною кислотою. При нагріванні мо- Вуглеводи носахаридів зі спиртами в присутності сухого хлороводню в реакцію вступає тільки одна гідроксильна група вуглеводу, хоча, виходячи з лінійної структури, за цих умов має утворитися сполука типу етеру по всіх гідроксильних групах. Не мало пояснення і характерне для моносахаридів явище мутаротації (від лат. тиіо — змінюю, гоіаііо — обертання) — зміна величини оптичного обертання свіжоприготованих розчинів. На пояснення цих фактів російський хімік А. А. Коллі (1870 р.), а потім німецький Б. Толленс (1883 р.) висловили припущення про циклічну будову моносахаридів. Як відомо, альдегіди реагують зі спиртами з утворенням напів-ацеталів (див. розд. 17.4): к—сг + к—он Ті г
н напівацеталь
Аналогічно моносахариди, будучи полігідроксіальдегідами або полігідроксикетонами, утворюють циклічні напівацеталі внаслідок внутрішньомолекулярної взаємодії карбонільної та просторово зближеної з нею спиртової груп. Причому, за теорією напруження циклів найбільш сприятливою є взаємодія, якщо вона приводить до утворення п'яти- або шестичленних циклів. Шестичленний цикл утворюється при взаємодії ок-согрупи з гідроксильною групою при С5 альдогексоз або С6 кетогексоз. Він називається піранозним (від шестичленного гетероциклу пірану). Цей процес можна зобразити так:
_,-Р°л В Г« 1—с—он-"" < 5^0 -сн Внутрішньомолекулярне утворення напівацеталю приводить до того, що атом Карбону карбонільної групи перетворюється на аси- Глава 22 метричний. Цей новий хіральний центр називається аномерним, а відповідні йому два нові стереоізомери — а- і (}-аномерами. Гідроксильна група, утворена в процесі циклізації моносахариду при аномерному центрі, називається напівацетальною, або глікозидною.
СН2ОН Р-£>-глюкопіраноза ,аномернии центр СН2ОН Д-глюкоза глікозидний гідроксил СН2ОН а-Л-глюкопіраноза
гідроксил
аномернии центр
глікозидний гідроксил
Л_ Л-гЬтлг-тпіпянтя П- іЬп л/^гт я п- П-гЬпл/ь-тлпіпяі-іп'їя
о фуран При взаємодії оксогрупи з гідроксильною групою при С4 альдогексоз або С5 кетогексоз утворюється п'ятичлен-ний цикл, який називають фуранозним (від п'ятичленно-го гетероциклу фурану). Вуглеводи
СН2ОН 3-/>-глюкофураноза глікозидний гідроксил
і_ноічс?-сн2он -он -н СН2ОН р-О-фруктофураноза аномерний центр СН2ОН
,0-глюкоза аномерний центр
глікозидний гідроксил СН2ОН а--0-глюкофураноза глікозидний гідроксил Наведені вище зображення циклічних форм моносахаридів називаються формулами Коллі—Толленса. Оскільки формули Коллі—Толленса громіздкі й незручні для зображення циклічних структур, англійський хімік-органік X. Хеуорс у 20-ті роки XX століття запропонував зображувати циклічні форми моносахаридів у вигляді плоских багатокутників, розміщених перпендикулярно до площини креслення. Хімічні зв'язки циклу, що знаходяться над площиною, зображують жирними лініями, а зв'язки, розміщені за площиною,— звичайними лініями. Атом Оксигену в циклі розміщується за площиною рисунка, причому, у піранозному циклі — у правому куті, у фуранозному — вгорі. Символи атомів Карбону в циклі не зображують.
піранозний цикл фуранозний цикл Замісники, які знаходяться у формулі Коллі—Толленса зліва від вертикалі, розміщують над площиною циклу, а ті що справа,— Глава 22 під площиною. У моносахаридах 2)-ряду група 6СН2ОН знаходиться над площиною циклу, а в моносахаридах Х-ряду — під площиною.
2 ---------
-он -н -он СН2ОН * а-і)-глюкошраноза
Поиск по сайту: |




 глікозидний гідроксил
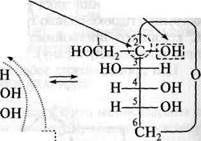
глікозидний гідроксил В ос-аномеру розміщення напівацетального гідроксилу таке ж саме, як і гідроксилу «кінцевого» хірального центру (асиметричного атома Карбону, що визначає належність до В- або 1-ряду). Тому в проекційних формулах моносахаридів І)-ряду глікозидний гідроксил в ос-аномеру розміщений справа від вертикальної лінії карбонового ланцюга, а у Р-аномеру — зліва.
В ос-аномеру розміщення напівацетального гідроксилу таке ж саме, як і гідроксилу «кінцевого» хірального центру (асиметричного атома Карбону, що визначає належність до В- або 1-ряду). Тому в проекційних формулах моносахаридів І)-ряду глікозидний гідроксил в ос-аномеру розміщений справа від вертикальної лінії карбонового ланцюга, а у Р-аномеру — зліва.
 ГЛІКОЗИДНИЙ
ГЛІКОЗИДНИЙ

 глікозидний гідроксил
глікозидний гідроксил

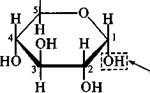 -с—юн:
-с—юн: