 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
ОКРЕМІ ПРЕДСТАВНИКИ. ВИКОРИСТАННЯ
етилен Н2С=СН2. Безбарвний газ з дуже слабким запахом, малорозчинний у воді, горить яскравим коптячим полум'ям, з повітрям утворює вибухові суміші. У промисловості слугує сировиною для виробництва етанолу, етиленгліколю, ацетальдегіду, поліетилену тощо. Використовується як речовина, що сприяє до-зріванню овочів і фруктів. ПропіленН2C=CH—CH3. Безбарвний газ зі слабким запахом. широко вживається в промисловому органічному синтезі для одержання ізопропілового спирту, гліцерину, ацетону, поліпропілену та інших цінних органічних сполук. Глава 11 аЛКадіЄНИ Алкадієнами називають аліфатичні вуглеводні, що містять два подвійні вуглець -вуглецеві зв 'язки. Загальна формула алкадієнів СиН2и_2. Залежно від розташування подвійних зв'язків у молекулі розрізняють три основних типи алкадієнів: > алкадієни з кумульованими подвійними зв 'язками (подвійні зв'язки розташовані біля одного атома Карбону) С—С—С . Такі сполуки називають аленами (за тривіальною назвою найпростішого представника цього ряду — алена Н2С—С—СН2); > алкадієни з кон 'югованими подвійними зв'язками (подвійні зв'язки розділені од > алкадієни з ізольованими подвійними зв 'язками (подвійні зв'язки розділені одним НОМЕНКЛАТУРА Назви алкадієнів за номенклатурою ШРАС утворюють аналогічно алкенам. Наявність двох подвійних зв'язків позначають суфіксом -дієн з указівкою положення кожного з них у головному вуглецевому ланцюзі: сн3—сн=сн—сн=сн2 сн3—сн=с=сн2 н2с=с—сн=сн2 сн3 1,3-пентадієн 1,2-бутадієн 2-метил-1,3-бутадієн Для деяких алкадієнів використовують тривіальні і раціональні назви: н2с=с—сн=сн2 н2с=сн—сн=сн2 н2с=сн—сн2—сн=сн2 сн3 ізопрен дивініл дивінілметан БУДОВА АЛКАДІЄНІВ У молекулі алкадієнів з кумульованою системою подвійних зв'язків атом Карбону, що утворює два подвійні зв'язки, знаходиться в стані sp-гібридизації, а сусідні з ним атоми Карбону — у sp2-гібридизації (рис. 11.1, а). ці три атоми Карбону Глава 11 розташовані в просторі лінійно, а я-зв язки знаходяться у двох взаємно перпендикулярних площинах. Чотири замісники при вуглецевих атомах у sp2-гібридизації теж розташовані у двох взаємно перпендикулярних площинах (рис. 11.1, б).
зр зр2 ЧН :с=с=с^ н сГ ,н А б Рис. 11.1. Схема просторової будови аленів Унаслідок такої просторової будови молекули аленів, в яких при кожному з атомів Карбону в sp2-гібридизації знаходяться різні замісники, є хіральними, а отже, для них можлива оптична ізомерія: н\ НзС^ енантіомери 1,3 -диметилалену Н якщо подвійні зв'язки в молекулі розділені одним вуглець-вуглецевим о-зв'язком (алкадієни з кон 'югованими зв'язками), відбувається додаткове перекривання р-електронних хмар сусідніх я-зв'язкш (я,я-кон'югація) і утворюється єдина я-електронна система, в якій я-електрони вже не належать окремим зв'язкам, а делокалізовані по всій системі (див. рис. 11.2).
^ Н /0,134 нм\ А б Рис. 11.2. Схематичне зображення кон'югованої системи 1,3-бутадієну: а — геометрія молекули; б — перекривання p-АО; в — делокалізована її-МО Перерозподіл електронної густини в молекулі приводить до укорочення о-зв'язку, розташованого між етиленовими групами, і супроводжується виділенням енергії, що сприяє підвищенню стабільності системи. цю енергію називають енергією резонансу. Так, у молекулі 1,3-бутадієну довжина зв'язку С-2—С-3 становить 0,148 нм, тоді як довжина зв'язку С—С в етані дорівнює 0,154 нм. енергія резонансу 1,3-бутадієну складає приблизно 15 кДж/моль. За допомогою методу електронографії встановлено, що алкадієни з кон'юго-ваними зв'язками мають переважно трансоїдну конформацію (транс-розташування подвійних зв'язків відносно одинарного): аЛКаДІЄни
Н н
0,134 мм н
н 122° н Алкадієни з ізольованими подвійними зв'язками побудовані аналогічно алкенам. Особливості будови алкадієнів різних типів позначаються на їх реакційній здатності. Зокрема, алкадієни з кумульованими та ізольованими зв'язками за хімічними властивостями в багатьох випадках нагадують алкени. Вони легко вступають у численні реакції приєднання, тільки в них бере участь не один, а два подвійні зв'язки. Алкадієни з кон'югованими подвійними зв'язками виявляють специфічні хімічні властивості.
Поиск по сайту: |

 Н
Н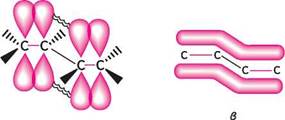 Н 0,134 нм.Н
Н 0,134 нм.Н