 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
АРОМАТИЧНІ ДИКАРБОНОВІ КИСЛОТИ
хоон ^/соон
хюон ноос^ Фталева ізофталева, терефталева, и-бенївдикарбонова 1,3-бензендикарбонова М-бензевди^карбонова кислота кислота - - ' Головним способом добування арендикарбонових кислот є каталітичне окиснення ксиленів киснем повітря; наприклад, при окисненні и-ксилену утворюється терефталева кислота: ,соон 02; і °С; кат.
Адипінова кислота НООС—(СН2)4—СООН.Біла кристалічна речовина (т. пл. 152 °С), малорозчинна у воді. Солі адипінової кислоти називають адипінатами. Застосовується переважно у вй- н,с и-ксилен
НООС"
Карбонові кислоти. Глава и При окисненні о-ксилену спочатку утворюється фталевий ангідрид, який у присутності води перетворюється на фталеву кислоту:
О,; / °С; У,0
фталевий ангідрид ^^.соон
хюон фталева кислота
У промисловості фталеву кислоту здобувають окисненням на-фталену киснем повітря в присутності каталізатора. Фталевий ан гідрид, що утворюється в процесі окиснення, гідролізують:
О,; х °С; У,0
І^онокарбонові кислоти лієї або двох карбоксильних груп утворюють солі, естери та аміди. Ґалогенангідриди утворюються тільки з участю двох карбоксильних груп. Моногалогенангідриди фталевих кислот під час реакції внутрішньомолекулярно реагують з карбоксильною групою, утворюючи ангідриди або полімерні речовини.
ге -н2о со-4он При конденсації фталевого ангідриду з фенолом утворюється фенолфталеїн. Реакція відбувається при нагріванні, у присутності водовіднімальних засобів (Н2$04): ОН н25Р4; '°С; н2о
Фізичні та хімічні властивості.Фталеві кислоти — це білі кристалічні речовини з високими температурами плавлення. Фталева та терефталева кислоти малорозчинні у воді, ізофталева кислота легко розчинна у воді. Фталеві кислоти виявляють більшу кислотність, ніж бензойна кислота. За хімічними властивостями арендикарбонові кислоти майже не відрізняються від ароматичних монокарбонових. З участю оД" фенолфталеїн (безбарвна форма) Фенолфталеїн являє собою білу кристалічну речовину, практично нерозчинну у воді, добре розчинну в етанолі (т. пл. 259— 263 °С). У кислому та нейтральному середовищі він перебуває в безбарвній формі, у лужному середовищі (при рН = 8,2... 10,0) набуває малиново-червоного забарвлення внаслідок утворення хіноїдної структури:
фенолфталеїн (малинове забарвлення)
У сильнолужному середовищі (рН > 12) малиново-червоне барвлення фенолфталеїну зникає внаслідок утворення солі бензс їдної структури:
Монокарбонові кислоти фенолфталеїн застосовується в аналітичній практиці як кис-дотно-оснбвний індикатор, у медицині — як проносний засіб. Препарат випускають у таблетках під назвою «Пурген». Ідентифікація дикарбонових кислот.При ідентифікації дикарбонових кислот беруть до уваги їх фізико-хімічні властивості. Здебільшого це кристалічні речовини з певними температурами плавлення, розчинні у воді. Як і монокарбонові кислоти, вони утворюють солі, естери, аміди. Для визначення деяких дикарбонових кислот існують також специфічні методи. Наприклад, сплав щавлевої кислоти та дифеніламіну забарвлює краплю етилового спирту в синій колір за рахунок утворення барвника — анілінового синього.
.
№0Н на
О забарвлена форма ЙаО. ОН
,014а
безбарвна форма ■ :■ ■ нкціональні похідні карбонових кислот ------ 315
ГЛАВА Ш) ГЛАВА
,о н3с—сн2—сн2—с XI
Поиск по сайту: |
 Ароматичними дикарбоновими (арендикарбоновими) кислотами називаються похідні ароматичних вуглеводнів, які містять дві карбоксильні групи, безпосередньо сполучені з ароматичним ядром. Найважливішими представниками є фталева, ізофталева і те-рефталева кислоти:
Ароматичними дикарбоновими (арендикарбоновими) кислотами називаються похідні ароматичних вуглеводнів, які містять дві карбоксильні групи, безпосередньо сполучені з ароматичним ядром. Найважливішими представниками є фталева, ізофталева і те-рефталева кислоти:


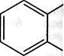
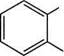 .СНз
.СНз

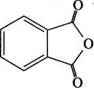
 Фталева кислота відрізняється від інших ізомерів здатністю легко перетворюватись при нагріванні на ангідрид:
Фталева кислота відрізняється від інших ізомерів здатністю легко перетворюватись при нагріванні на ангідрид: СООі^Н
СООі^Н
 Карбонові кислоти. Глава ід
Карбонові кислоти. Глава ід



 ,<Жа
,<Жа
