 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Строение атома и Периодическая система химических элементовСтр 1 из 11Следующая ⇒
НЕОРГАНИЧЕСКАЯ ХИМИЯ БИОГЕННЫХ ЭЛЕМЕНТОВ Методические указания и контрольные задания для студентов технологических специальностей заочной формы обучения
Могилёв 2012 УДК 546
Рассмотрено и рекомендовано к изданию на заседании кафедры химии Протокол № 1 от 30.08.2012 г.
Составители: Огородников В.А. Супонева Т.М.
Рецензент кандидат химических наук, доцент А.В. Оботуров
В пособии представлены контрольные задания по курсу общей химии для студентов технологических специальностей заочной формы обучения и указания к решению типовых задач.
УДК 546
© Учреждение образования «Могилёвский государственный университет продовольствия», 2012
Содержание
Введение
Дисциплина «Неорганическая химия биогенных элементов» относится к циклу фундаментальных химических дисциплин и представляет собой теоретическую основу современных технологий пищевой промышленности. Кроме того, химическая культура технолога пищевой промышленности является необходимым элементом правильного понимания экологических вопросов, связанных с контролем качества продуктов питания, переработкой сырья, рациональным природопользованием. В настоящем пособии представлены 8 заданий по наиболее важным темам, понимание которых необходимо для успешного освоения студентами-технологами других химических дисциплин, таких как аналитическая химия, физическая и коллоидная химия, биохимия, а также специальных дисциплин по технологии отрасли. Эти задания включают следующие разделы курса: – Периодическая система, строение атома; – прогнозирование свойств элементов и их соединений; – комплексные соединения; – окислительно-восстановительные реакции; – расчёт концентраций ионов в растворах соединений биогенных элементов; – расчёт pH в растворах электролитов и расчёт концентраций электролитов по заданной величине pH.
Каждое задание включает в себя 35 вариантов задач; номер варианта соответствует порядковому номеру студента в списке группы. Из 8 заданий –
Для получения по контрольной работе оценки «зачтено» достаточно выполнить задания № 1; 2а; 3–5; 8 (предполагается, что при выполнении этих заданий студент осваивает учебный материал, знание которого соответствует удовлетворительной оценке на экзамене). Студенты, претендующие на хорошие и отличные оценки, должны выполнить все задания.
1 Понятие о биогенных элементах. Прогноз свойств химических
Биогенные элементы Биогенные элементы – это химические элементы, постоянно входящие в состав организмов и выполняющие определенные биологические функции. Биогенные элементы необходимы для существования и жизнедеятельности живых организмов. Основу живых систем составляют шесть элементов: углерод, водород, кислород, азот, фосфор, сера. Эти элементы называют органогенами; их суммарное содержание в живых организмах превышает 97 % (по массе). Однако перечень биогенных элементов не исчерпывается лишь органогенами. К числу важнейших биогенных элементов относятся также хлор, калий, натрий, магний, кальций, железо, цинк, медь, марганец, ванадий, молибден, бор, кремний, селен, фтор, бром, йод и некоторые другие элементы. По количественному содержанию в организме биогенные элементы делятся на макро-, микро- и ультрамикроэлементы. Макроэлементы – это элементы, массовая доля которых в живых организмах превышает 0,01 % (кислород, углерод, водород, азот, фосфор, сера, кальций, магний, натрий, хлор). Содержание микроэлементов в организме составляет 10–5–10–3 масс. %; микроэлементами являются фтор, бром, йод, мышьяк, стронций, барий, медь, кобальт. Элементы, массовая доля которых в организме менее 10–5 %, называют ультрамикроэлементами (ртуть, золото, уран, торий, радий и др.). Часто микроэлементы и ультрамикроэлементы объединяют в одну группу. В таблице 1.1 приведены данные о содержании ряда химических элементов в организме человека [1, с.210].
Таблица 1.1 – содержание некоторых химических элементов в организме человека
Недостаток данной классификации заключается в том, что она отражает лишь содержание элементов в живых организмах, но не указывает на биологическое значение того или иного элемента. По значимости для жизнедеятельности организма химические элементы можно разделить на 3 группы [1, с.211]: 1 – жизненно необходимые (незаменимые) элементы – постоянно содержатся в организме человека и животных, входят в состав ферментов, гормонов и витаминов (C; H; O; N; P; S; Cl; I; K; Na; Mg; Ca; Mn; Fe; Co; Cu; Zn; Mo; V). Их дефицит приводит к нарушению нормального функционирования организма. 2–примесные элементы, постоянно находящиеся в организме; эти элементы постоянно содержатся в организме человека и животных (Ga; Sb; Sr; Br; F; B; Be; Li; Si; Sn; Cs; Al; Ba; Ge; As; Rb; Pb; Ra; Bi; Cd; Cr; Ni; Ti; Ag; Th; Hg; U; Se), однако их биологическая роль малоизучена или неизвестна. 3 – примесные элементы, обнаруживаемые в организме (микропримесные элементы) – данные о содержании этих элементов (Sc; Tl; In; La; Pr; Sm; W; Re; Tb и др.) и их биологической роли в настоящее время отсутствуют. Как следует из вышеизложенного, перечислить точно все биогенные элементы невозможно из-за сложности определения очень маленьких концентраций микроэлементов и выяснения их биологических функций. В настоящее время известно, что в организме человека и животных обнаруживается свыше 70 элементов таблицы Д.И. Менделеева; около 50 из них присутствуют постоянно, т.е. являются биогенными. Развитие аналитической химии и, в частности, спектрального анализа позволяет расширить перечень биогенных элементов и установить биологическое значение многих из них.
Строение атома и Периодическая система химических элементов Согласно современным представлениям атом представляет собой сложную микросистему, состоящую из положительно заряженного ядра и отрицательно заряженных электронов, движущихся вокруг этого ядра. Заряд ядра Zравен порядковому номеру элемента в Периодической системе химических элементов. Например, заряд ядра атома водорода равен +1, поэтому водород – первый элемент Периодической системы; заряд ядра атома углерода равен +6 (углерод – шестой по счёту элемент в периодической системе). Химический элемент– этовид атомов, характеризующийся определённым зарядом ядра. Ядра всех атомов данного элемента имеют один и тот же заряд. Поскольку атом электронейтрален, то число электронов (отрицательных частиц) в атоме равно положительному заряду ядра: в атоме водорода (Z = +1) содержится только один электрон, в атоме углерода (Z = +6) – шесть электронов, в атоме железа (Z = +28) – двадцать восемь электронов. Электроны в многоэлектронных атомах располагаются на нескольких электронных слоях (уровнях), находящихся на различных расстояниях от ядра атома. Чем больше энергия электрона, тем дальше он находится от ядра. Если несколько электронов имеют близкие значения энергии, то они (электроны) находятся на приблизительно одинаковом расстоянии от ядра. Так образуются электронные оболочки, состоящие из электронов с приблизительно одинаковой энергией. Можно также сказать, что электроны с близкими значениями энергии образуют электронный слой, или, как часто говорят, энергетический уровень. Число электронных слоёв в атоме данного элемента равно номеру периода, в котором находится элемент. Например, кремний (Z = +14) – элемент третьего периода; все 14 электронов, содержащиеся в атоме кремния, располагаются на трёх энергетических уровнях: на первом энергетическом уровне (n = 1) – 2 электрона, на втором (n = 2) – 8 электронов, на третьем – 4 электрона (рисунок 1.1).
Рисунок 1.1 – Строение атома кремния
Рисунок 1.2 – Формы и обозначения атомных орбиталей
На одной орбитали может находиться не более двух электронов, причём спины этих электронов должны быть противоположны. Первый энергетический уровень любого атома образован одной s-орбиталью
Рисунок 1.3 – Расположение p-электронных облаков в пространстве
В пределах одного и того же энергетического уровня p-орбитали имеют несколько более высокую энергию, чем s-обитали. Поэтому p-орбитали показывают чуть выше s-орбиталей. На четырёх орбиталях второго энергетического уровня может разместиться не более 8 электронов, поэтому максимальное число электронов на втором энергетическом уровне любого атома равно 8.
Поиск по сайту: |

 Атомной орбиталью называют область пространства вокруг ядра атома, в которой наиболее вероятно нахождение электрона (иногда вместо термина «атомная орбиталь» используют термин «электронное облако»). Орбитали в зависимости от энергии электронов имеют различные формы и размеры (рисунок 1.2):
Атомной орбиталью называют область пространства вокруг ядра атома, в которой наиболее вероятно нахождение электрона (иногда вместо термина «атомная орбиталь» используют термин «электронное облако»). Орбитали в зависимости от энергии электронов имеют различные формы и размеры (рисунок 1.2):

 Графически орбиталь изображают в виде клеточки, а электрон – в виде стрелки. Орбиталь атома водорода с его единственным электроном:
Графически орбиталь изображают в виде клеточки, а электрон – в виде стрелки. Орбиталь атома водорода с его единственным электроном: Кроме движения вокруг ядра каждый электрон обладает собственным движением. Это собственное движение электрона (аналогия из классической механики – вращение частицы вокруг своей оси) характеризуют с помощью понятия спин (обозначение спина: или ¯).
Кроме движения вокруг ядра каждый электрон обладает собственным движением. Это собственное движение электрона (аналогия из классической механики – вращение частицы вокруг своей оси) характеризуют с помощью понятия спин (обозначение спина: или ¯). . Т.к. на одной орбитали может разместиться максимум
. Т.к. на одной орбитали может разместиться максимум 
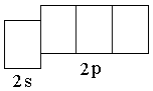 Второй энергетический уровень любого атома состоит из одной 2s-орбитали, образующей s-подуровень и трёх 2p-орбиталей, образующих p-подуровень; три p-электронных облака расположены в пространстве перпендикулярно друг другу (рисунок 1.3).
Второй энергетический уровень любого атома состоит из одной 2s-орбитали, образующей s-подуровень и трёх 2p-орбиталей, образующих p-подуровень; три p-электронных облака расположены в пространстве перпендикулярно друг другу (рисунок 1.3).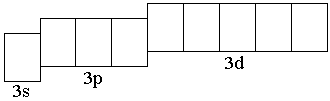 Третий энергетический уровень образован одной
Третий энергетический уровень образован одной