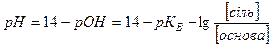|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Гідроліз солей. Ступінь та константа гідролізу
ГІДРОЛІЗ СОЛЕЙ Більшість реакцій гідролізу – оборотні: Pb(NO3)2 + H2O → Pb(OH)(NO3) + HNO3 Na2HPO4 + H2O →NaH2PO4 + NaOH У результаті гідролізу в розчинах багатьох солей утворюється кисле або лужне середовище. Деякі солі повністю розкладаються у воді, тобто повністю гідролізують і не можуть існувати у вигляді розчинів. В таблиці розчинності солей вони позначені знаком ( þ Реакція ГІДРОЛІЗУ
Ця реакція є зворотною до реакції утворення солей.
þ Реакція НЕЙТРАЛІЗАЦІЇ
Основи і кислоти можуть бути сильними і слабкими, тому солі можна розділити на чотири типи. þ ТИПИ СОЛЕЙ
Розглянемо реакції гідролізу цих типів солей. 1. Солі, утворені сильними основами і слабкими кислотами, гідролізують за аніоном,їх розчини мають лужне середовище (рН >7). Приклади солей: Na2CO3; CH3COONa; KCN; Na2S; K2SiO3 Приклад рівняння гідролізу: K2SiO3 +2H2O = 2КОН + H2SiO3 2K+ + SiO32 SiO32 Висновок: 1. В реакції гідролізу бере участь АНІОН солі. 2. рН>7, середовище розчину солі стає лужним. ü Якщо ліки гідролізують за аніоном і утворюють лужне середовище, приймати їх треба перед їжею, інакше вони нейтралізуються шлунковим соком. 2.Солі, утворені слабкими основами і сильними кислотами гідролізують за катіоном,їх розчини мають кисле середовище, рН<7. Приклади солей: A12(SO4)3; FeCl3; CuBr2; NH4C1; Zn(NO3)2; (NН4)2Cr2O7. Приклад рівняння реакції гідролізу: FeCl3 + 3Н2О = Fe(OH)3 + 3НCl Fe3+ + 3Сl Fe3++ 3H2O = Fe(OH)3¯ + 3H+ Висновок: 1. В реакції гідролізу бере участь КАТІОН солі 2. рH<7, середовище розчину солі стає кислим. ü Ліки, які гідролізуютьза катіоном і утворюють кисле середовище приймати треба після їжі, щоб не викликати подразнення слизової шлунку. 3. Солі, утворені слабкими основами і слабкими кислотамигідролізують за катіоном і аніоном,розчини цих солей мають нейтральне, слабокисле або слаболужне середовище, рН≈7. Приклади солей: A12S3; Cr2S3; CH3COONH4; (NH4)2CO3. Приклад реакції гідролізу: (NН4)2СО3 + 2Н2О = 2NH4OH + Н2СО3 2NH4+ + СO32 Висновок: 1. В реакції гідролізу бере участь КАТІОН і АНІОН солі 2. рН = 7. розчин має нейтральне середовище. Якщо утворюється два слабкі електроліти, то гідроліз протікає необоротно. A12S3 + 6H2O = 2А1(ОН)3¯ + 3H2S Тому сульфід алюмінію не може існувати у вигляді водних розчинів, може бути одержаний тільки "сухим способом", наприклад, взаємодією елементів при високій температурі: 2A1 + 3S = A12S3 і повинен зберігатись в герметичних посудинах, в які не потрапляє волога. ü Якщо ліки піддаються повному гідролізу, вони вміщуються в капсули, які повинні розчинитися у визначеному місці шлунково-кишкового тракту. 4. Якщо сіль утворена сильною основою і сильною кислотою гідроліз не відбувається,середовище завжди (!) нейтральне, рН=7. Наприклад в розчинах NaCl, K2SO4, К2Сr2О7, Ba(NO3)2 гідроліз не відбувається. NaCl + Н2О = NaOH + HC1 Na+ + Сl Н2О = Н+ + ОН ü Якщо лікарські речовини не гідролізують, їх можна приймати у будь-який час і вводити у вигляді ін'єкцій безпосередньо в кров. Буферні розчини. Буферними називають розчини, які здатні зберігати значення рН при розведенні або при додаванні невеликих кількостей кислоти чи лугу, а також при їх концентруванні. До таких розчинів належать: 1) розчини, що містять слабку кислоту і сіль цієї кислоти з сильною основою: СН3СООН + СН3СООNa- ацетатний буфер рН (3,72-5,57) (4,65) 2) розчини, що містять слабку основу і сіль цієї основи з сильною кислотою NН40Н + NH4Cl - аміачний буфер pН (8,43-10,28) (9,37) 3) розчини, що містять солі багатоосновних слабких кислот Nа2НР04 + NаН2P04 - фосфатний буфер pН( 5,91-7,73) (6,81) рН для даного складу буферу є величина постійна, однак змінюючи співвідношення в концентрації кислоти і солі можна одержувати в кожному випадку інше значення pН буферної системи, яка може бути в деяких певних границях. Механізм дії буферних розчинів. В ацетатному буфері кислота і сіль піддаються дисоціації
СНзСООNа СНзСОО- + Nа+ Якщо до такого розчину додати кислоту, яка в розчині протолізується НСІ + Н2О = СІ- + Н3О+ то в розчині буде проходити реакція нейтралізації.
Отже, H+ сильної кислоти зв’язуються з аніонами слабкої кислоти, яка є малодисоційованою і тому реакція середовища майже не змінюється. Якщо ж до цього самого розчину додати сильну основу NаОН, то будуть відбуватись такі процеси: електролітична дисоціація NаОН = Na+ + ОН- протоліз СНзСООН+Н2О = СН3СОО- +Н3О+ нейтралізація Н3О++ ОН- = 2Н2О Отже, реакція середовища майже не змінюється. Для розрахунку pН кислотного буферного розчину використовують формулу:
а для основних буферів рівняння Гендерсона-Гассельбаха:
Здатність буферних розчинів протидіяти зміні pН називають буферною дією. Межі, в яких проявляється ця дія називається буферною ємністю. Буферна ємність - це розрахункова величина, яка визначається кількістю еквівалентів сильної кислоти п (1/1 НСІ) або п(1/2 Н2S04) або сильної основи п (1/1 NаОН), п(1/2 Вa(ОН)2) що треба додати до 1 л. буферного розчину, щоб pН змінився на одиницю. Якщо В - буферна ємність, а п (Н3О+) і п (ОН-) — молярні концентрації еквівалентів відповідно кислоти і основи, то
Із досліджувальної пари співвідношення концентрацій кислоти до солі =1 : 10 pН = pКA ± 1 Якщо С солі = С кислоти, то pН = pКA
Поиск по сайту: |



 СН3СОО- + Н3О+ СН3СООН + Н2О
СН3СОО- + Н3О+ СН3СООН + Н2О звідси
звідси або
або 
 або
або