 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Вчення про розчини. Кислотно-основна рівновага біологічних рідин в організмі
Розчин – це гомогенна (однорідна) система, яка складається з розчинника, розчинених речовин і продуктів їх взаємодії. За агрегатним станом розчини поділяються на рідкі і тверді (деякі мінерали, металічні сплави, пластмаси). За співвідношенням між розчинником і розчиненою речовиною розрізняють розчини ненасичені, насичені і перенасичені, а також розведені та концентровані. Розчин у якому речовина більше не розчиняється за даної температури, називається насиченим. Наприклад у воді масою 100 г при t=20 0С розчиняється хлорид натрію масою 36 г. Більше хлориду натрію в цьому розчині розчинитися не може, тобто маємо насичений розчин. Розчин у якому речовина ще може розчинитися за даної температури називається ненасиченим. Пересичені розчини– це нестабільні системи. Їх одержують шляхом повільного охолоджування насичених при більш високій температурі розчинів. Здатність речовин, змішуючись з іншою речовиною, утворювати гомогенні системи називається розчинністю. Основні поняття: Моль (ν) - кількість речовини, що містить стільки певних структурних частинок, скільки атомів міститься в 12 г С12 ( Це число 6,02 • 1023). Молярна маса (М)- це маса 1 моля речовини.
ν - кількість молів речовини, m – маса речовини. На практиці молярну масу визначають виходячи із молекулярної формули речовини, як суму мас всіх атомів, які входять до складу молекули. Наприклад М(H2SO4) = 2*1+32+4*16=98 г/моль. Еквівалент (Е) в кислотно-основних реакціях - це умовна частина, яка може приєднати, заміщати чи якимось іншим способом взаємодіяти з одним молем йонів водню. Еквівалент в реакціях окиснення - відновлення - умовна частина, яка може приєднати чи віддавати один електрон. Число еквівалентності (z) - число, яке показує з кількома йонами водню може взаємодіяти дана речовина в кислотно-основних реакціях; або кількість прийнятих чи відданих електронів в окисно-відновних реакціях. Фактор еквівалентності (f) - число, яке показує, яка частка умовної частини речовини еквівалентна або реагує з одним йоном водню в даній кислотно- оcновній реакції чи з одним електроном в даній окисно-відновній реакції. Молярна маса еквівалента (МE) - це маса одного моля еквівалентів даної речовини яку можна визначити як добуток фактора еквівалентності на молярну масу.
Для елементів z - валентність елементу M E = f .M = Наприклад для А1: M( Для кислот: z - основність кислоти (кількість Н+, які заміщуються в даній реакції)
Для Н2SO4 : М( Для основ: z - кислотність основи ( кількість ОН- )
Для Са(ОН)2 : М( Для солей: z - добуток кількості атомів металу на їх валентність
Для Al2 (SO4)3: Концентрації розчинів можна виражати як через масу, так і за кількістю молів розчиненої речовини. Розрізняють такі основні способи вираження концентрації: 1). Масова частка (ω) - величина, що показує скільки грам розчиненої речовини міститься в 100 г розчину і виражається як відношення маси розчиненої речовини до маси розчину: m розчину = m розч.реч. + m розчинника
Виражають в безрозмірних одиницях, частках одиниці або у відсотках:
Для розчинів, які містять дуже мало розчиненої речовини можна виразити масову частку в проміле ( ‰ ) - тисячна частка цілого 1 ‰ = 0,1% 2). Молярна концентрація (См) – величина, що показує скільки молів розчиненої речовини знаходиться в 1 л розчину. Визначається як відношення кількості речовини (ν) до об’єму розчину:
визначається в моль/л чи моль/дм3 (в системі СI використовують розмірність моль/м3) враховуючичи, що
або якщо V вимірюється в мл, то 3). В об’ємних методах аналізу при титруванні, а також в науковій літературі використовують спосіб вираження концентрації – молярна концентрація еквівалентів, який в застарілій літературі зустрічається як нормальність (N). Молярна концентрація еквівалентів (СЕ) - це величина, що показує скільки еквівалентів розчиненої речовини міститься в 1 л розчину. Визначається як відношення кількості еквівалентів речовини до об’єму розчину. або де V- об’єм розчину, мл m- маса розчиненої речовини, г. Виражають молярну концентрацію еквівалентів розчину в моль-екв./л, або в моль/л чи моль/дм3 .
Поиск по сайту: |
 ,
, 

 [г/моль]
[г/моль] . М
. М Аl)=
Аl)= 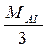 =
=  =9 г/моль
=9 г/моль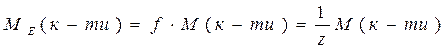



 Са(ОН)2)=
Са(ОН)2)=  =
=  =37 г/моль
=37 г/моль
 = 57 г/моль
= 57 г/моль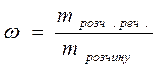
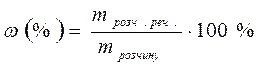






 M(x) - молярна маса еквівалентів речовини х
M(x) - молярна маса еквівалентів речовини х