 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Самостійна робота на занятті
Виконати лабораторні роботи: 1. Визначити константу електродної посудини. 2. Визначити електропровідність розчинів слабих електролітів. 3. Визначити ступінь і константу дисоціації досліджуваних електролітів Методика виконання роботи Робота 1. Визначення константи електродної посудини. Визначення константи електродної посудини проводять за допомогою розчину електроліту, для якого відоме значення питомої електропровідності. З цією метою використовують, як правило, 0,01 М розчин Ксl, для якого при 20 0С В посудину для визначення електропровідності наливають такий об’єм 0,01 М розчину Ксl , щоб електроди були повністю занурені в розчин. За допомогою омметра замірюють опір розчину в посудині і за формулою К = R× Робота 2. Визначення електропровідності розчинів слабих електролітів та біологічних рідин. Визначивши постійну (константу) електродної посудини, останню старанно промивають дистильованою водою, наливають в неї відповідний досліджуваний розчин слабкого електроліту і вимірюють опір. Одержані дані заносять у таблицю:
Використовуючи знайдені величини опору досліджуваних розчинів і постійну електродної посудини (K) розраховують питому електропровідність :
і молярну електропровідність :
С - молярна концентрація V – розведення, Для розчинів слабких електролітів розрахувати також граничну молярну електричну провідність, використовуючи дані довідника про електролітичну рухливість відповідних іонів :
Результати занести в таблицю і зробити висновок. Робота 3.Порівняння сили електролітів на основі електропровідності їх розчинів. Використовуючи дані із роботи № 2 про молярну електропровідність і граничну електропровідність відповідних розчинів електролітів, розраховують ступінь і константу дисоціації.
Дані занести у таблицю і зробити висновок про силу різних електролітів і як впливає введення хлору в радикал кислоти на її силу.
ЗАНЯТТЯ №14 Тема: Електродні потенціали та механізм їх виникнення. Потенціометрія Актуальність теми:Потенціометричний метод дозволяє визначити концентрацію йонів водню в розчинах і різних біологічних рідинах. Наявність доступних вимірювальних приладів робить цей метод широко використовуваним на практиці. Знання закономірностей виникнення електродних потенціалів, будови електродів, вимірювання рН середовища дає в руки медиків інструмент для діагностики і коректування важливого показника різних рідин внутрішнього середовища організму. Навчальні цілі: Знати: суть методу потенціометрії, який дозволяє визначити концентрацію йонів в різних середовищах, будову електродів, принцип вимірювання за допомогою потенціометра. Вміти: підготувати прилад до роботи, вимірювати рН різних розчинів і біологічних рідин, провести потенціометричне титрування і визначити концентрацію досліджуваного розчину. Самостійна позааудиторна робота студентів. 1. Механізм виникнення подвійного електричного шару. 2. Електродний потенціал, фактори від яких залежить його значення. 3. Рівняння Нернста для окисно-відновних систем. 4. Стандартні електродні потенціали. 5. Класифікація електродів. 6. Електроди визначення. Скляний електрод, йонселективні електроди. 7. Електроди порівняння. Водневий електрод. Хлорсрібний електрод. 8. Суть потенціометричного методу визначення рН розчинів і біологічних рідин. 9. Потенціометричне титрування. Які електроди при цьому застосовуються? 10. Криві потенціометричного титрування. Визначення точки еквівалентності графічним методом. 11. Застосування методу потенціометрії в медицині. 12. Зубні протези в стоматології. Проблеми гальванозу. 13. При потенціометричному титруванні до 20 мл розчину NaOH додавали по 1 мл розчину HCl C(HCl) = 0,15 моль /л. При цьому рН розчину змінювалось дуже повільно і до досягнення рН 9,7 було витрачено 14 мл розчину HCl. Після цього розчин HCl стали додавати порціями по 0,1 мл і при додаванні 0,4 розчину HCl рН різко змінився до 4,3. Розрахувати молярну концентрацію еквівалентів NaOH .
Контрольні питання. 1. Електродні потенціали, причини виникнення. 2. Рівняння Нернста. 3. Електроди 1 і 2-го роду. 4. Що таке стандартні електродні потенціали? 5. Будова і принцип дії водневого електроду. 6. Будова і принцип дії електроду порівняння. 7. Будова і принцип дії скляного електроду. 8. Будова і принцип дії мембранного електроду. 9. Як визначають стандартні електродні потенціали? 10. Що таке потенціометричне титрування? 11. Які складові необхідні для визначення рН розчину? 12. Як визначити точку еквівалентності при потенціометричному титруванні? 13. Що таке йонселективний електрод?
Поиск по сайту: |
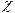 = 1,25 × 10-3 См/м.
= 1,25 × 10-3 См/м.




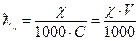 де:
де:  - питома електропровідність
- питома електропровідність

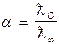 ; К=
; К= 
 a
a