|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Индикаторы, которые применяются в редоксиметрии.
В отдельных методах (случаях) редоксиметрии можно титровать без индикаторов. Примером безиндикаторного титрования может быть окисление разных восстановителей перманганатом, особенно в кислой среде. Без индикатора можно также титровать восстановители раствором І2, поскольку присущая йоду темно-бурая окраска исчезает в результате восстановления І2 до І-; раствором соли Се (IV), так как он окрашен в желто-оранжевый цвет, а Се (ІІІ) – бесцветный. Однако результаты титрования во всех перечисленных случаях получаются менее точными по сравнению с перманганатом, потому что окраска перечисленных веществ менее интенсивна, чем окраска КMnO4. Поэтому в редоксиметрическом титровании, как правило, применяют индикаторы. Индикаторы, для редоксиметрических титрований по их действию можно разделить на две группы: 1) Индикаторы, которые вступают в специфическую реакцию с окислителем или восстановителем. Например: Ø SCN- является индикатором на Fe3+, так как образует с ним окрашенные в красный цвет комплексные соединения типа [Fe(SCN)]2+, [Fe(SCN)2]+ и т.д.; Ø Крахмал является прекрасным индикатором на І2, так как образует с йодом смешанные адсорбционные и комплексные соединения ярко-синего цвета. 2) Индикаторы, у которых изменение окраски не зависит от специфических свойств окислителя или восстановителя, реагирующих между собой при титровании, а связана с достижением титруемым раствором определенного окислительно-восстановительного потенциала. Такие индикаторы называют окислительно-восстановительными или редокс-индикаторами. Из сказанного ясно, что окислительно-восстановительные индикаторы представляют собой вещества, способные обратимо окисляться или восстанавливаться, причем окисленная и восстановленная формы их имеют разную окраску. Если обозначить эти формы схематически через Indox и Indred, то взаимопревращение их можно представить уравнением: Indox + ne = Indred. Очевидно, система, состоящая из Indox и Indred, представляет собой окислительно-восстановительную пару. Применяя к ней уравнение Нернста, получим:
где Ео – стандартный потенциал данной пары. Если к раствору кого-либо восстановителя (или окислителя) прибавить 1-2 капли раствора того или другого окислительно-восстановительного индикатора, то установится соответствующее потенциалу раствора отношение между концентрациями окисленной и восстановленной форм индикатора. При этом раствор приобретет соответствующую данному отношению окраску. Если такой раствор титровать каким-либо окислителем (или восстановителем), то величина потенциала Е будет изменяться. Соответственно будет меняться также соотношение
Следовательно, интервал перехода индикатора записывается уравнением:
Таким образом, интервал перехода индикатора лежит между значениями двух потенциалов, один из которых на 0,059/n больше, другой на 0,059/n меньше, чем его стандартный потенциал. Приведем несколько примеров редокс-индикаторов.
Поиск по сайту: |
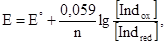
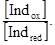 Однако, как и для индикаторов метода кислотно-основного титрования, не всякое изменение этого отношения воспринимает наш глаз как изменение окраски. Если принять, что присутствие одной из окрашенных форм индикатора глаз перестает замечать при десятикратном избытке другой формы, то для области перехода окислительно-восстановительного индикатора получим следующие границы значений потенциала Е:
Однако, как и для индикаторов метода кислотно-основного титрования, не всякое изменение этого отношения воспринимает наш глаз как изменение окраски. Если принять, что присутствие одной из окрашенных форм индикатора глаз перестает замечать при десятикратном избытке другой формы, то для области перехода окислительно-восстановительного индикатора получим следующие границы значений потенциала Е: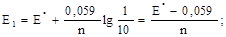 (окраска Indred);
(окраска Indred); (окраска Indox).
(окраска Indox).