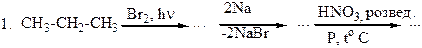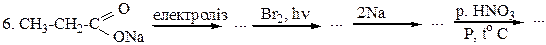|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Експериментальна частинаСтр 1 из 9Следующая ⇒
Техніка безпеки 1. Дослід 2 виконувати у витяжній шафі в захисних окулярах при опущеному захисному склі. 2. При попаданні фільтрату (дослід 2) на шкіру, уражене місце промити великою кількістю води та нейтралізувати 1 %-им розчином оцтової кислоти, оскільки фільт-рат має лужне середовище. Контрольні запитання та завдання
1. Які елементи входять до складу більшості органічних речовин? 2. На яких реакціях грунтується якісний аналіз органічних речовин? 3. Як визначають карбон та гідроген в органічних сполуках? 4. Як визначають сірку в органічних сполуках? 5. Як визначають нітроген в органічних сполуках? 6. Як визначають галогени в органічних сполуках? Лабораторна робота 2
Тема: Методи добування та хімічні властивості алканів Мета роботи:Вивчити методи добування та хімічні властивості алканів, провести відповідні досліди. Тривалість виконання:4 год.
Теоретична частина
Насичені вуглеводні (алкани) об’єднані в гомологічний ряд загальної формули СnH2n+2, містять sp3-гібридизований атом карбону. Усі ковалентні зв’язки у алканах – σ-зв’язки. Алкани мало реакційноздатні сполуки, вступають в реакції заміщення гідрогену та реакції розщеплення молекули з руйнуванням С–С-зв’язків. Для алканів найхарактерніші реакції замі-щення, що відбуваються за радикальним ланцюговим механізмом (гало-генування, нітрування, сульфохлорування та ін.). Для проходженя цих реакцій потрібно опромінення або нагрівання. Не всі реакції заміщення є селективними. Наприклад, бромування відбувається селективно, а при хлоруванні утворюється суміш усіх можливих продуктів заміщення. Алкани окиснюються важко, як правило, при високих температурах. Це екзотермічний і малокерований процес, тому окиснення проводять киснем повітря при невисоких температурах (150 оС) при наявності каталізатора, утворюються гідропероксиди і продукти подальшого їх розкладу. Розчини перманганату калію алкани не окиснюють. Слід пам’ятати, що суміш метану з повітрям у співвідношенні 1:10 вибухонебезпечна. Алкани поширені серед природних сполук (нафта, газ та ін.), тому основні промислові методи добування алканів – це виділення у вигляді сумішей. Лабораторні методи добування алканів (реакція Вюрца, електроліз солей карбонових кислот (реакція Кольбе), декарбоксилювання карбонових кислот, гідрування алкенів та ін.) дозволяють отримати індивідуальні алкани [1, с.203-228]. Експериментальна частина
Дослід 1. Добування метану (Дослід проводити у витяжній шафі в захисних окулярах при опущеному захисному склі.) Для проведення досліду збирають прилад, який зображений на рис.2. Пробірку 1 на 1/5 заповнюють сумішшю, яка складається з однієї частини безводного ацетату натрію та двох частин твердого лугу. Далі пробірку за-
Спостереження:
Рівняння реакції:
Дослід 2. Відношення газоподібних алканів до бромної води Газ, який виділяється у досліді 1, пропускають у пробірку з бромною водою.
Спостереження:
Дослід 3. Відношення газоподібних алканів до розчину перман-ганату калію Газ, який виділяється у досліді 1, пропускають у пробірку з 0,5 %-им розчином перманганату калію.
Спостереження: Дослід 4. Відношення рідких алканів до бромної води До 2 мл розчину бромної води додають 1 мл рідкого алкану (наприк-лад, гексану) суміш енергійно струшують.
Спостереження:
Дослід 5. Відношення рідких алканів до розчину перманганату калію До 2 мл 0,5%-го розчину перманганату калію додають 1 мл рідкого насиченого вуглеводню (наприклад, гексану), суміш енергійно струшують.
Спостереження:
Дослід 6. Взаємодія метану з киснем Товстостінну пляшку об’ємом 250 мл заповнюють із газометрів методом витіснення сумішшю рівних кількостей метану та кисню. Пляшку обгортають рушником і закривають корком. Перевертають пляшку в горизонтальне положення, відкривають корок і підносять до отвору палаючу скіпку.
Спостереження:
Рівняння реакції:
Висновок: Техніка безпеки
1. Дослід з твердим лугом проводити у витяжній шафі в захисних окулярах при опу-щеному захисному склі. Твердий луг брати шпателем або пінцетом. При попаданні лугу на шкіру промити уражене місце великою кількістю води та нейтралізувати 1 %-им розчином оцтової кислоти 2. Досліди з бромною водою проводити у витяжній шафі. При попаданні бромної во-ди на шкіру уражене місце промити водним розчином аміаку. Після проведення дос-ліду реакційну суміш вилити у спеціальний посуд, що стоїть у витяжній шафі. 3. Дослід 6 виконує лаборант.
Контрольні запитання та завдання 1. Що таке sp3 – гібридизація ? Яку гібридизацію мають атоми вуглецю в алканах? 2. Наведіть механізм взаємодії 2-метилпентану з бромом. 3. Запропонуйте методи добування 2,3-диметилгексану, застосовуючи реакції Вюрца, Кольбе, Дюма. 4. Які реакції характерні для насичених вуглеводнів? 5. Наведіть рівняння реакцій хлорування, нітрування, сульфохлорування алканів на прикладі 2-метилбутану. 6. Які продукти утворяться при дії оксигену на 2-метилбутан при температурі 150оС ( у присутності каталізатора) ? Завдання до самостійної роботи Здійснити перетворення:
Перетворити в декілька стадій:
Виконати завдання:
[2], № 1.1.3, 5, 7, 10, 12,13,19, 20, 21, 22, 24, 25, 26,27, 36 . Лабораторна робота 3
Поиск по сайту: |
 Рис.2.
Рис.2.