 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
ВИВЧЕННЯ КІНЕТИКИ НІТРОЗУВАННЯ ТРОПЕОЛІНУ
Мета роботи: визначити порядок реакції нітрозування тропеоліну за азотистою кислотою; знайти каталітичну константу швидкості реакції. Тропеолін 00 – натрієва сіль 4-феніламіноазобензол-4-сульфокисло-ти – кислотно-основний індікатор. Кислі розчини (pH < 3) тропеоліну 00 мають червоно-фіолетове забарвлення, обумовлене існуванням його у вигляді амфііону. Реакція нітрозування тропеоліну в цих умовах оборотна і проходить за рівнянням:
При введенні у розчин соляної кислоти або її солей реакція значно прискорюється. Припускається, що хлорид-іони утворюють з азотистою кислотою більш активний нітрозуючий агент – активну проміжну сполуку. Механізм їхньої взаємодії такий:
Якщо врахувати, що в початковий момент реакція практично необоротна, швидкість каталітичної реакції wk утворення нітрозотропеоліну (RNNO) буде Вважаючи, що рівновага утворення NOCl за першою стадією (3.2) встановлюється дуже швидко, визначаємо концентрацію проміжної сполуки: де K – константа рівноваги реакції утворення NOCl. Приймаючи до уваги оборотну хімічну реакцію Підставивши (3.5) і (3.6) у рівняння (3.4), дістанемо:
де Оскільки швидкості каталітичної та некаталітичної реакцій сумірні, сумарна швидкість нітрозування тропеоліну 00 у присутності Cl--іонів: де k0, k – константи швидкості відповідно некаталітичної реакції й реакції у присутності каталізатора. За ходом реакції спостерігають по змінюванню забарвлення розчину фотоколориметричним методом (див. "Загальні відомості"). Необхідне обладнання: 1. Фотоелектроколориметр. 2. Кювети колориметричні з товщиною світлопоглинаючого шару 30 мм – 2 штуки (поводитись із кюветами дуже обережно!). 3. Секундомір. 4. Папір фільтрувальний для протирання кювет. 5. Колба мірна об'ємом 25 або 50 мл для приготування еталонних розчинів – 1 шт. 6. Колби для еталонних розчинів об'ємом 50-100 мл – 6 шт. 7. Бюретки на 25 мл – 2 шт. (для розчинів тропеоліну № 1 і № 2, та для розчину 0,4 н. H2SO4). 8. Циліндр мірний об'ємом 10 або 25 мл – 2 шт. 9. Склянка об'ємом 50 мл для приготування реакційної суміші – 2 шт. 10. Лійки для бюреток – 2 шт. 11. Олівець по склу (маркер). 12. Посудина для зливання відпрацьованих розчинів. Реактиви: 1. Розчин 1×10-5 моль/дм3 тропеоліну у 0,4 н. H2SO4 (Розчин № 1). 2. Розчин 1×10-5 моль/дм3 тропеоліну у 0, 4 н. H2SO4 з 0,6 моль/дм3 хлориду натрію (Розчин № 2). 3. Кислота сірчана, 0,4 н. розчин. 4. Розчин нітриту натрію 3×10-5 моль/дм3. 5. Розчин нітриту натрію 6×10-5 моль/дм3.
Поиск по сайту: |

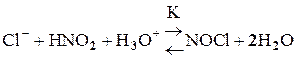 (швидко), (3.2)
(швидко), (3.2) (3.3)
(3.3) , (3.4)
, (3.4) , (3.5)
, (3.5) , де Kд – константа дисоціації протонованої форми тропеоліну, знаходимо:
, де Kд – константа дисоціації протонованої форми тропеоліну, знаходимо: . (3.6)
. (3.6) , (3.7)
, (3.7)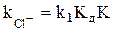 – каталітична константа.
– каталітична константа. (3.8)
(3.8)