 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Вивчення кінетики реакції гідролізу оцтово-етилового ефіру у присутності каталізатора (іони гідроксонію)
Мета роботи: визначити порядок і константу швидкості реакції гідролізу оцтово-етилового ефіру у присутності соляної кислоти при різних температурах; обчислити енергію активації реакції. У водному розчині гідроліз оцтово-етилового ефіру за рівнянням
проходить практично повністю, але дуже повільно. Реакція значно прискорюється у присутності каталізатора – соляної кислоти, яка вводиться в реакційну систему у надлишку. За її відсутності процес перебігав би автокаталітично, бо оцтова кислота, що утворюється, дисоціює з утворенням іонів гідроксонію. У присутності надлишку HCl ступінь дисоціації оцтової кислоти дуже мала, і концентрація іонів гідроксонію у розчині залишається сталою. У реакції кислотного гідролізу складних ефірів виявляється специфічний кислотний каталіз, бо каталізатором є іони гідроксонію, і реакційноздатною є протонована форма вихідної речовини (субстрат S). Стадії процесу:
Лімітуючою стадією кислотно-каталітичного процесу є перетворення реакційноздатної проміжної протонованої форми у продукти реакції. Отже, швидкість реакції гідролізу етилацетату дорівнює швидкості другої стадії:
де
тобто швидкість реакції гідролізу етилацетату підкоряється кінетичному рівнянню першого (псевдопершого) порядку, у якому константа швидкості, що спостерігається, дорівнює Кінетику реакції вивчають за зміною у часі концентрації оцтової кислоти шляхом титрування проб, що відбираються з реакційної суміші через певні проміжки часу. Необхідне обладнання: 1. Колби об'ємом 100 см3 із притертими пробками – 2 шт. 2. Циліндр мірний об'ємом 50-100 см3 – 1 шт. 3. Піпетки на 2-5 см3 із поділками (для ефіру та проб реакційної суміші) – 2 шт. 4. Колби для титрування – 2 шт. 5. Колба для води об'ємом 250-300 см3 – 1 шт. 6. Бюретка об'ємом 25 см3 – 2 шт. 7. Термостат. 8. Годинник. Реактиви: 1. Етилацетат. 2. Розчин HCl 0,5 M. 3. Розчин NaOH 0,1 н. 4. Розчин фенолфталеїну 1%-ий.
Поиск по сайту: |
 (1.1)
(1.1)
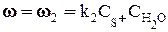 , (1.5)
, (1.5)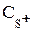 – концентрація протонованої форми ефіру, що складає деяку долю aвід концентрації етилацетату Cеф, тобто:
– концентрація протонованої форми ефіру, що складає деяку долю aвід концентрації етилацетату Cеф, тобто: 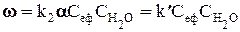 . У цім рівнянні k¢ = k2a – ефективна константа швидкості реакції. Коефіцієнт a не залежить від концентрації ефіру і визначається лише кислотністю середовища. Таким чином, концентрація H3O+ входить у величину k¢ в неявній формі. Оскільки реакцію проводять при невеликій концентрації ефіру у водному розчині, то концентрація води протягом усього експерименту практично не змінюється, і можна записати
. У цім рівнянні k¢ = k2a – ефективна константа швидкості реакції. Коефіцієнт a не залежить від концентрації ефіру і визначається лише кислотністю середовища. Таким чином, концентрація H3O+ входить у величину k¢ в неявній формі. Оскільки реакцію проводять при невеликій концентрації ефіру у водному розчині, то концентрація води протягом усього експерименту практично не змінюється, і можна записати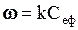 , (1.6)
, (1.6)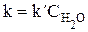 .
.