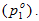|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Давление насыщенного пара над раствором, эбулиоскопия, криоскопия, осмос и осмотическое давление.
Давление насыщенного пара над раствором равно произведению его давления над чистым растворителем на его мольную долю. (Закон Рауля). Между жидкостью и ее насыщенным паром существует динамическое равновесие жидкость↔ насыщенный пар, т.е. число молекул жидкости, испаряющихся с поверхности, равно числу конденсирующихся молекул. Этому равновесию соответствует давление насыщенного пара растворителя над чистым растворителем Нижний индекс (1) обозначает то, что свойство относится к растворителю; (2) – к растворенному веществу, а верхний индекс (о) указывает на то, что это свойство вещества в чистом состоянии; в данном случае это свойство чистого растворителя. В 1882 г. французский ученый Рауль сформулировал закон, названный его именем: давление насыщенного пара растворителя над раствором пропорционально молярной доле растворителя:
Выражение для молярной массы растворенного вещества
Следовательно, измеряя экспериментально давление насыщенного пара растворителя над раствором можно определить молярную массу растворенного вещества. Эбулиоскопия (от лат. ebulio — вскипаю) — метод исследования растворов, основанный на измерении повышения их температуры кипения по сравнению с чистым растворителем. Используется для определения молекулярной массы растворенного вещества, активности растворителя, степени диссоциации (или изотонического коэффициента). Температура кипения жидкости — такая температура, при которой давление пара над жидкостью равно внешнему давлению. В то же время давление пара над раствором нелетучего вещества практически полностью определяется давлением пара растворителя и, в соответствии с законом Рауля, может быть выражено уравнением:
где x1 — мольная доля растворителя. Видно, что при повышении концентрации растворенного вещества давление пара над раствором будет снижаться, а следовательно, при неизменном внешнем давлении, будет расти температура кипения. С учетом уравнения Клапейрона — Клаузиуса можно показать[1], что изменение температуры кипения раствора (ΔTboil) может быть рассчитано по формуле:
где ΔHboil — энтальпия испарения; M1 — молярная масса растворителя; n2 — моляльная концентрация растворенного вещества. Криоскопия (от греч. κρύο — холод и греч. σκοπέω смотрю) — метод исследования растворов, в основе которого лежит измерение понижения температуры замерзания раствора по сравнению с температурой замерзания чистого растворителя. Был предложен Ф. Раулем в 1882 году. Давление пара над раствором нелетучего вещества практически полностью определяется давлением пара растворителя и может быть выражено уравнением (согласно закону Рауля):
где x1 — мольная доля растворителя. Видно, что оно ниже, чем давление пара над чистым растворителем, и снижается с ростом концентрации растворенного вещества. О́смос (от греч. ὄσμος — толчок, давление) - самопроизвольный процесс перехода растворителя через полупроницаемую перегородку (мембрану) из растворителя в раствор или из менее концентрированного раствора в более концентрированный. Осмотическим давлением называется величина, измеряемая минимальным гидравлическим давле–нием, которое нужно приложить к раствору, чтобы осмос прекратился. Законы осмотического давления. Вант-Гофф предложил эмпирическое уравнение для расчета осмотического давления разбавленных раст–воров неэлектролитов: π = С(Х)RT, где π – осмотическое давление, кПа; С(Х) – молярная концентрация, моль/л; R – универсальная газовая постоянная, равная 8,31 кПа – л/(моль – К); Т – абсолютная температура, К. Хотя закон Вант—Гоффа был установлен на основе экспериментальных данных, он может быть выведен из условий термодинамического равновесия при ΔG = 0. Поэтому этот закон следует рассматривать как следст–вие второго начала термодинамики. Выражение в вышеуказанной форме аналогично уравнению Клапейрона—Менделеева для идеальных газов, однако эти уравнения описывают разные про–цессы.
Поиск по сайту: |