 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Природа химической связи
Химическая связь – взаимодействие атомов, обуславливающее их соединение в молекулы и кристаллы. В 1807 г. Дэви предположил, что молекулы образуются благодаря электрическому притяжению разноименно заряженных атомов. Берцелиус развил эту идею и в 1812-1818 гг. создал электрохимическую теорию химической связи. Согласно теории любой атом обладает как положительным, так и отрицательным полюсами. Атомы с преобладанием положительного полюса притягиваются к атомам с преобладанием отрицательного. Получившаяся молекула может также обладать избыточным зарядом, положительным или отрицательным, и притягиваться к другой молекуле. Например: Са+ + О– → СаО+ ; СаО+ + CO2– → CaCO3 . Однако теория Дэви-Берцелиуса не могла объяснить существование ряда молекул, например, H2, Cl2, O2, образованных одинаковыми атомами. В 1860-е годы Бутлеров разработал теорию химического строения, в которой выдвинул следующее положение: Атомы в молекулах соединены друг с другом в определенной последовательности в соответствии с их валентностью, и от этой последовательности зависят свойства вещества. Валентность – это свойство атома соединяться с некоторым числом других атомов. Бутлеров предложил изображать внутреннюю структуру молекул в виде формул вида: Н – Cl ; H – O – Cl ;
После открытия электрона и строения атома валентность стали связывать с числом электронов на периферии атома. В 1916 году Льюис предположил, что ковалентная химическая связь возникает путем образования электронной пары, общей двум атомам, и поэтому молекула является более устойчивой системой, чем отдельные атомы. H • + H • → H : Н (образование молекулы Н2). В том же году Кóссель высказал подобную идею об образовании ионной связи. Однако, в этом случае, один из атомов полностью отдает валентный электрон другому атому. Устойчивость соединения обеспечивается электрическим притяжением образовавшихся ионов. Na • + • Если ввести понятие энергии химической связи, как энергии, необходимой для ее разрыва, то закон сохранения энергии приводит к выводу о том, что устойчивая молекула может образоваться только при уменьшении потенциальной энергии взаимодействия электронов и ядер исходных атомов. В рамках квантовой механики это взаимодействие микрочастиц в молекуле в принципе может быть описано теоретически путем решения уравнения Шрёдингера для системы электронов и ядер при наименьшем значении потенциальной энергии. Однако, для многоэлектронных систем точное решение получить не удается ввиду математических трудностей, и поэтому в практических расчетах используют приближенные решения, которые согласуются с экспериментальными данными об энергиях связи и межъядерных расстояниях в молекулах. Впервые такой расчет был проведен в 1927 г. для молекулы Н2 (Гейтлер, Лондон). Взаимодействие электрона с ядром в каждом атоме Н они считали основным взаимодействием, а взаимодействия между электронами и ядрами разных атомов Н учли в виде малых поправок к основному взаимодействию. В результате решения уравнения Шрёдингера удалось получить зависимость энергии (W) системы от расстояния между ядрами r. Оказалось, что существует определенное расстояние r0, соответствующее минимуму W. В дальнейшем Пóлинг распространил метод Гейтлера-Лондона на другие молекулы с ковалентной связью, а потом различные методы квантовой механики были применены также к другим типам химической связи. Параллельно проводились экспериментальные исследования молекулярных структур. Таким образом, начиная с 1930-х гг. можно говорить о появлении квантовой химии, как раздела теоретической химии, рассматривающей химические явления с точки зрения квантовых представлений о веществе. В настоящее время считается, что: 1) любая химическая связь есть вид электромагнитного взаимодействия электронов и ядер атомов в молекулах; 2) ее образование сопровождается перестройкой электронной структуры атомов; 3) положение электронов относительно ядер определяет тип химической связи; 4) современная теория химической связи должна использовать квантовую механику.
Происхождение жизни Биология – наука, изучающая живые организмы. Исторически в биологии имели место два подхода: 1) редукционистский (направленный на изучение структурно-функциональных особенностей отдельных организмов); 2) виталистический (направленный на изучение жизни в целом, как уникального явления, не сводимого только к физическим или химическим закономерностям). Основная задача биологии – истолковывать все явления живой природы, исходя из научных законов, не забывая при этом, что организму как целому присущи свойства, отличные от свойств его частей. Например: сознание возникает в результате коллективной работы миллионов нейронов. Хотя работу отдельного нейрона можно описать языком физики и химии, феномен сознания в целом так описать нельзя. Поэтому нет представления о возникновении мысли и ее химических основах. В рамках современной науки жизни нельзя дать строгого определения, а можно только перечислить признаки, отличающие живой объект: 1) питание (создание живым организмом своих органических веществ): - автотрофное: а) фотосинтез органики из СО2, Н2О под действием света; б) хемосинтез органики из неорганических веществ в ходе химических реакций; - гетеротрофное (органические вещества синтезируются в результате химических превращений органики, созданной автотрофамисинтезируются в результате химических превращений ств)ственной проблемы, а не отдельной узкой задачиь, шуманизируетго применени); 2) дыхание (окисление веществ с целью получения энергии для процессов жизнедеятельности): - аэробное (с участием О2); - анаэробное (без участия О2); 3) раздражимость (реакция на изменение внешней и внутренней среды); 4) подвижность (характерна для животных, менее заметна у растений); 5) выделение (продуктов обмена веществ); 6) размножение (воспроизведение себе подобных, обеспечивающее непрерывность и преемственность жизни): - половое (развитие организма в результате слияния половых клеток); - бесполое (без участия половых клеток); - вегетативное (развитие нового организма из части материнского); 7) рост (живых организмов изнутри за счет питательных веществ, в отличие от неживых объектов, присоединяющих вещество к наружной поверхности). Эти семь главных признаков любого живого организма характеризуют его как систему саморегуляции (устойчивую). Нельзя также сказать, как и когда возникла жизнь на Земле, т.к. воспроизвести эти события в наглядном виде невозможно. Поэтому любые теории происхождения жизни в настоящий момент могут быть только совокупностью гипотез, в той или иной мере поддающихся проверке. Рассмотрим эти теории. 1. Теория креационизма предполагает, что жизнь создана сверхъестественным образом в определенное время. Эта идея присутствует почти во всех религиозных учениях. Процесс сотворения имел место только один раз и поэтому недоступен наблюдению. Следовательно, наука не может ни доказать, ни опровергнуть концепцию креационизма. 2. Теория самопроизвольного зарождения жизни считает, что жизнь возникала неоднократно из неживого вещества. Эта теория существовала еще в Китае, Вавилоне и Египте как альтернатива креационизму. Аристотель на основе собственных наблюдений составил лестницу природы – ряд организмов от неживых до живых существ – и тем самым выделил предмет биологии. Он считал, что есть частицы вещества, содержащие активное начало, которое при подходящих условиях может создавать живой организм. Теория зарождения была опровергнута только микробиологическими исследованиями Пастера в XIX веке. Пастер доказал справедливость концепции биогенеза, т.е. то, что жизнь может возникнуть только из ранее существовавшей жизни. 3. Теория стационарного состояния – жизнь существовала всегда. Земля тоже существовала всегда и всегда была способна поддерживать жизнь. Аргументы этой теории, как правило, связаны с неясностями в экспериментальных данных. Например, для возраста Земли даются все более высокие оценки (4,5-5)·109 лет. Или обнаруживаются ископаемые остатки вида, считавшегося вымершим. 4. Теория панспермии (Рихтер, 1865 г.; Аррениус, 1895 г.) – жизнь занесена на Землю извне. Т.к. по данным космической разведки в Солнечной системе обнаружены только некоторые органические соединения, утверждается, что жизнь могла возникнуть в разное время в разных частях Вселенной. Тем самым проблема ее возникновения просто туда переносится. 5. Теория биохимической эволюции утверждает, что жизнь возникла в результате процессов, подчиняющихся физическим и химическим законам. В 1871 году Дарвин высказал следующую идею. Условия первичного возникновения жизни, вероятно, отличались от современных условий на Земле хотя бы потому, что они должны были обеспечить накопление органического материала в течение длительного времени. В 1923 году Опарин разработал теорию, в которой предполагалось, что такие условия появились на Земле после образования ее внешних оболочек. Атмосфера содержала Н2О, NН3, СН4, Н2, в ней не было О2. Органические вещества образовались в океане под воздействием ультрафиолетового излучения Солнца. Затем образовались коацерваты – сгустки белковых молекул и молекул Н2О, способные избирательно накапливать различные соединения, и из них – примитивные клетки. Несмотря на экспериментальное подтверждение возможности синтеза первичного органического материала Миллером (1953), Орджелом и другими, эта теория содержит ряд темных мест, например, о переходе от коацерватов к клеткам, появлении у них способности к самовоспроизведению.
Поиск по сайту: |
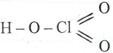 , где черточка обозначает химическую связь между атомами.
, где черточка обозначает химическую связь между атомами.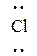 : → Na+ Cl– (образование соединения NaCl).
: → Na+ Cl– (образование соединения NaCl).