 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Второй закон термодинамики
Формулировки: Р. Клаузиус: Невозможен процесс, единственным результатом которогоявляется переход теплоты от более холодного тела к более горячему У. Томсон: Теплота наиболее холодного из участвующих процессе тел неможет служить источником работы Существует функция состояния системы (энтропия), определяющаянаправление самопроизвольного процесса: в изолированной системесамопроизвольно могут протекать только те процессы, при которыхпроисходит увеличение энтропии. Энтропия
Физический смысл энтропии: мера беспорядка в системе Энтропия - функция состояния системы. В термодинамике - это величина, определяемая соотношением: где S- энтропия. Т.е. изменение энтропии равно количеству теплоты, переданному в процессе, к температуре, при которой происходил этот процесс. В этом смысле адиабатный процесс - это изоэнтропийный процесс. Из первого закона термодинамики:
- основное уравнение термодинамики. Из теоремы Карно следует: Следовательно: Второй закон термодинамики объясняет направление протекания процессов и вводит понятие энтропии ΔS=Q/T. ---Критерием самопроизвольного протекания процесса в изолированной системе является ΔS>0, равновесия – ΔS=0. --- Энтропия является функцией состояния и ее смысл расшифровывается в статистической термодинамики как мера беспорядка системы. Чем больше беспорядок, тем больше энтропия. Ряд последовательных термодинамических процессов, представляющих собой один замкнутый, называется круговым термодинамическим процессом или циклом. В рассмотренных ранее политропных процессах изучались вопросы получения работы вследствие подведенной теплоты, изменения внутренней энергии рабочего тела или вследствие того и другого. При однократном расширении газа в цилиндре можно получить лишь ограниченное количество работы, так как при любом процессе расширения все же наступит момент, когда температура и давление рабочего тела станут равными температуре и давлению окружающей среды и на этом прекратится получение работы. Для повторного получения работы необходимо осуществить процесс сжатия и возвратить рабочее тело в первоначальное состояние. Таким образом, для непрерывного производства работы рабочее тело должно участвовать в круговом термодинамическом процессе (рис.1).
Рис. 1
Циклы могут быть обратимыми, состоящими из обратимых процессов, и необратимыми. В основе анализа эффективности современных тепловых машин лежат обратимые циклы, т.е. идеальные циклы, не учитывающие потери на трение и т.д. Циклы подразделяются на прямые и обратные. Прямыми называются циклы, в которых теплота преобразуется в работу, обратными – в которых теплота передается от более холодного тела к более нагретому. При изображении циклов на термодинамических диаграммах последовательный обход процессов в прямом цикле происходит по часовой стрелке (см. рис.1), в обратном цикле – против часовой стрелки. Для всех циклов очевидным является условие: так как цикл начинается и заканчивается в одной точке. Тогда первый закон термодинамики для цикла запишется следующим образом: где Qц – теплота, участвующая в цикле, равная алгебраической сумме количеств теплоты для каждого процесса; Lц – работа цикла (цикловая работа), равная соответственно алгебраической сумме работ в каждом процессе.
Прямой цикл.Прямой цикл – это цикл двигателя. В этом цикле происходит преобразование теплоты в механическую работу (рис.2).
Рис.2
В процессе 1а2 к рабочему телу от горячего источника температурой Т1 подводится теплота Q1 и совершается положительная работа. В процессе 2b1 от рабочего тела к холодному источнику температурой Т2 отводится количество теплоты Q2 и совершается отрицательная работа. Количество работы в процессе расширения L1a2 , больше, чем работа сжатия L2b1 , и цикловая работа будет положительна и равна: На рисунке работа цикла изображается площадью фигуры пл.1-а-2-b-1. В соответствии с первым законом термодинамики для цикла: Для оценки эффективности преобразования теплоты в работу в прямом цикле используют термический коэффициент полезного действия (КПД), под которым понимают отношение работы, полученной в цикле, к затраченной теплоте: Таким образом, термический КПД показывает какая часть теплоты, подведенной к циклу от нагревателя, превращена в полезную работу. Согласно второму закону термодинамики эта величина всегда меньше единицы (<100%). Обратный цикл. Обратный цикл служат для производства холода или теплоты. В нем рабочее тело переносит теплоту от холодного источника к горячему. Для совершения такого несамопроизвольного процесса затрачивается работа цикла. Обратные циклы реализуются в холодильных машинах и тепловых насосах (рис.3).
Рис.3 В процессе расширения 1а2 температура рабочего тела ниже Т2,в результате чего от холодного источника к рабочему телу передаётся количество теплоты Q2. В процессе сжатия 2в1 температура рабочего тела выше Т1 и горячему источнику от рабочего тела передаётся количество теплоты Q1. Так как на процесс сжатия работы затрачивается больше и она отрицательна, работа цикла будет равна: Первый закон термодинамики имеет вид: Для оценки работы холодильных машин применяется так называемый холодильный коэффициент, определяемый отношением полезной теплоты Q2, отнятой от холодного источника ограниченной емкости, к затраченной работе: В холодильной машине теплота Q1 выбрасывается в окружающую среду – источник неограниченной емкости. Машины, основным продуктом производства которых является теплота Q1, передаваемая в источник ограниченной емкости, называются тепловыми насосами. Эффективность работы в этом случае оценивается отопительным коэффициентом, представляющим собой отношение теплоты Q1, переданной потребителю, к затраченной работе: В цикле теплового насоса теплота Q2 отбирается от источника неограниченной емкости (например, атмосфера). Значения холодильного и отопительного коэффициентов могут изменяться в широких пределах 0 ≤ ε,φ< ∞.
Цикл Карно и максимальный КПД тепловой машины
Цикл Карно в координатах T и S Представим себе следующий цикл: Фаза А→Б. Рабочее тело с температурой, равной температуре нагревателя, приводится в контакт с нагревателем. Нагреватель сообщает рабочему телу Фаза Б→В. Рабочее тело отсоединяется от нагревателя и продолжает расширяться адиабатически (без теплообмена с окружающей средой). При этом его температура уменьшается до температуры холодильника. Фаза В→Г. Рабочее тело приводится в контакт с холодильником и передает ему Фаза Г→А. Рабочее тело адиабатически сжимается до исходного размера, и его температура увеличивается до температуры нагревателя. Его КПД равен, таким образом,
то есть, зависит только от температур холодильника и нагревателя. Видно, что 100%-ный КПД можно получить только в том случае, если температура холодильника есть абсолютный нуль, что недостижимо. Можно показать, что КПД тепловой машины Карно максимален в том смысле, что никакая тепловая машина с теми же температурами нагревателя и холодильника не может обладать бо́льшим КПД. Заметим, что мощность тепловой машины Карно равна нулю, так как передача тепла в отсутствие разности температур идёт бесконечно медленно.
Поиск по сайту: |
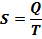
 ,
,
 .
. или
или 

 ,
, ,
,
 .
. .
. .
. 

 .
. .
. .
. .
.

 тепла в изотермическом процессе (при постоянной температуре), при этом объём рабочего тела увеличивается.
тепла в изотермическом процессе (при постоянной температуре), при этом объём рабочего тела увеличивается. тепла в изотермическом процессе. При этом объём рабочего тела уменьшается.
тепла в изотермическом процессе. При этом объём рабочего тела уменьшается. ,
,