 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Место фотохимии в колориметрии
В заключение уместно обсудить, неустойчивость органических пигментов, как общий закон природы. Многие объекты экспертизы (см. 6.3) выстроены сложными органическими (углеводородными) молекулами, происходящими из окружающего растительного и животного мира. К таким материалам относят бумагу, дерево, ткани, лаки, масла, и т.д., и т.п., каждый из которых имеет характерную пигментацию. Очевидно, в силу закона сохранения вещества все сложные углеводороды рано или поздно разложатся на элементарные (С; О2; Н2О; СО2 и др.), которые унаследуют новый цикл превращений, … – человек может только отслеживать этапы этого бесконечного процесса. Но если историку суждено хронографировать, то эксперту дано еще и анализировать его. И здесь термодинамические законы служат фундаментальной основой для такого анализа. Спонтанность фотохимических реакций есть следствие 2-го закона термодинамики и фотоиндуцированное разложение углеводородов, хоть и протекает с малой скоростью, идет в природе спонтанно. Очевидно, термодинамически благоприятными являются процессы, сопровождающиеся уменьшением свободной энергии
где T – температура, Рассмотрим ∆G = – Fnn∆E (4) где F=9,64846×104 Дж×(В×моль)–1 – число Фарадея (по химической шкале), n – количество вещества-реагента, n – число перенесенных в реакции электронов, ∆E – разность электрохимических потенциалов реагента и продукта. Не повторяясь в вопросе о химических механизмах разрушения (см. Приложение В), для всех реакций обратим внимание на электрохимические потенциалы основных реагентов и продуктов разрушения органических веществ. На рис. 6.4 показан график зависимости Е от степени окисления углерода для ряда его соединений. Любопытно, что практически все природные
углеводороды концентрируются на одной прямой, т.к. у них степень окисления углерода незначительно варьируется вблизи нуля. Анализ закономерности рис. 6.4 позволяет сформулировать следующие обобщения: 1. Превалирующая стойкость элементарного углерода над углеводородами с той же степенью окисления (целлюлозой, формальдегидом, глюкозой, etc.) обуславливает приоритетное разрушение этих углеводородов, ибо последнее становится термодинамически благоприятным процессом. 2. Максимум, лежащий на кривой между высшей и низшей возможными степенями окисления, говорит о том, что углеводороды со степенями окисления интервале [–4;+4], – нестойкие в сравнении с СО2 и СН4. Иначе говоря, все сложные углеводороды с близкой к нулю степенью окисления энергетически богаты и термодинамически неустойчивы по отношению к разрушающим реакциям окисления до CO2 и восстановления до СH4. Сказанное в равной степени относится и к природным, и к искусственным органическим материалам – всем им присуще неизбежное разрушение, безразлично, при окислении или при восстановлении до наиболее стабильных элементарных соединений. В свою очередь, сказанное справедливо и для всех органических пигментов, обуславливающих окраску – предмет выцветает. Нарушений законов термодинамики науке пока не известно. Как показано выше, из второго закона термодинамики следует, что определяющие цвет молекулы сложных углеводородов будут в конце концов разрушены. Независимо от того, какие меры противодействия предприняты, это разрушение приведет к необратимому изменению цвета объекта. Посему этот закон можно считать хорошим подспорьем для экспертов-хронологов. И хотя некоторые возможности искусственно замедлять процессы разрушения и сводить к минимуму их действие имеются, полностью прекратить их нельзя никогда. Завершая раздел, попробуем очертить место колориметрии со вспомогательной фотохимической реакцией среди направлений экспертной деятельности. Учитывая вышеизложенные перспективы в области технической экспертизы документов, первоочередного раскрытия заслуживает сфера искусствоведческих приложений этого метода (применительно к криминалистике – это, в первую очередь, экспертиза антиквариата). Подробное освещение этой темы в наиболее сложном аспекте органической химии (динамика цветности лака, покрывающего, например, иконопись; …) отнесено к Приложению В, а более тривиальные вопросы неорганической химии (к примеру, цвет патины на бронзе; закристаллизованного стекла; ...) оставлены для самостоятельной проработки [1.16 и др.]. Здесь мы подчеркнем только, что основной вопрос при экспертизе антиквариата очевиден – это установление времени создания предмета старины. И эта задача адекватно решается либо непосредственным измерением цвета, либо методами анализа. Так сравнительная колориметрия фрагментов, выполненных неорганическими и органическими пигментами, приводит не только к понятию, но и к технологии колориметрической датировки произведений искусства.
Поиск по сайту: |
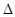 G<0. Если в 0<
G<0. Если в 0< 