 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Аргентометрическим методом
Метод основан на способности азотнокислого серебра в нейтральных растворах образовывать с хлористым натрием белый осадок хлористого серебра, а с хромовокислым калием темно-красный осадок хромовокислого серебра. Растворимость хлористого серебра меньше, чем хромовокислого серебра, поэтому вначале образуется белый осадок хлористого серебра по реакции
NaCl + AgNO3 = NaNO3 + AgCl↓
После связывания всего хлора азотнокислое серебро начинает реагировать с хромовокислым калием с образованием красного осадка по уравнению AgNO3 + K2CrO4 = Ag2CrО4↓ + 2KNО3 Аппаратура, материалы, реактивы: весы AR2140; бюретка; колбы мерные на 250 см3; стакан; палочки стеклянные; фильтры бумажные; пипетки вместимостью 10, 25 см3; Реактивы: гидроокись натрия 0,1 моль/дм3 (0,1 н. раствор); серебро азотнокислое 0,05 моль/дм3 (0,05 н. раствор); калий хромовокислый 100 г/дм3 (10 % -ный раствор); фенолфталеин 10 г/дм3 (1,0 %-ный спиртовой раствор). Проведение испытания. В стакан на 100 см3 взвешивают с точностью 0,01 г 5 г пробы и количественно переносят дистиллированной водой с температурой 60 оС (2/3 объема) в мерную колбу вместимостью 200-250 см3, и настаиваю в течение 30 мин, охлаждают и холодным дистиллятом доводят до метки. Содержимое мерной колбы фильтруют через сухой бумажный фильтр, первые 20-30 см3 фильтрата отбрасывают. Отбирают пипеткой 25 см3 фильтрата и титруют 0,05 н раствором азотнокислого серебра в присутствии 3-4 капель раствора хромовокислого калия до получения неисчезающего красновато-бурого окрашивания.
Массовую долю поваренной соли (Х) в процентах определяют по формуле:
где V - объем жидкости в мерной колбе, см³; V2 - объем 0,05 н. раствора азотнокислого серебра, пошедший на титрование испытуемого раствора, см³; V1 - объем водной вытяжки, взятой на титровании, см³; m - масса навески муки, г; 0,00295 - количество хлористого натрия, соответствующее 1 см³ 0,05 н. раствора азотнокислого серебра; К - поправочный коэффициент к 0,05 н. раствору азотнокислого серебра. За окончательный результат принимают среднее арифметическое значение результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,2%. Вычисление проводят до второго десятичного знака.
1.3.5 Определение кислотности. Метод основан на нейтрализации свободных жирных кислот, содержащихся в изделии, раствором гидроокиси натрия в присутствии фенолфталеина. Титруемая кислотность выражается в градусах. Градусом кислотности называют объем 1 моль/дм3 (1н щелочи), идущей на нейтрализацию кислот, содержащихся в 100 г продукта. Оборудование, материалы:весы лабораторные общего назначения, с допустимой погрешностью 0,01г, колбы конические с пробкой, вместимостью 500 см3, колбы мерные, вместимостью 250 см3, пипетки вместимостью 25 см3; стеклянная палочка с резиновым наконечником; капельница; бюретка со штативом. Реактивы: натрия гидроокись, раствор 0,1 моль/дм3 (0,1 н); фенолфталеин, спиртовой раствор10 г/дм3 (1,0 %-й). Проведения испытания. В коническую колбу вместимостью 500 см3 отвешивают 25 г пробы с погрешностью ± 0,01 г Мерную колбу, вместимостью 250 см3 наполняют до метки дистиллированной водой температурой от 18 до 25 оС. Около 100 см3 дистиллированной воды отливают в колбу с навеской, быстро растирают пробу толстой стеклянной палочкой с резиновым наконечником до однородной массы. К полученной массе добавляют из мерной колбы всю оставшуюся дистиллированной воду, колбу закрывают пробкой и интенсивно встряхивают 3 мин. После встряхивания дают смеси отстояться в течение 8 мин, жидкость осторожно сливают через сито или марлю в сухой стакан. Из стакана в две конические колбы отбирают по 50 см3 раствора, добавляют три капли раствора фенолфталеина и после тщательного перемешивания титруют 0,1 н раствором гидроокиси натрия до появления слабо-розовой окраски, не исчезающей в течение 1 мин. Кислотность х , град определяют по формуле:
где V1—объем раствора молярной концентрации 0,1 моль/дм3 гидроокиси натрия или гидроокиси калия, израсходованный на титрование, см3; V – объем дистиллированной воды, взятый для извлечения кислот, см3; m— навеска, г; V2 – объем исследуемого раствора, взятого на титрование, см3; К - поправочный коэффициент приведения используемого раствора гидроокиси натрия или гидроокиси калия к раствору точно молярной концентрации 0,1 моль/дм3 , 10 – коэффициент пересчета раствора гидроокиси натрия, молярной концентрации 0,1 моль/дм3 к 1 моль/дм3;а – коэффициент пересчета на 100 г навески.
Поиск по сайту: |
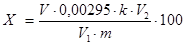 (1.15)
(1.15) (1.16)
(1.16)