 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Йодометрическим методом
Метод основан на окислении альдегидной группы сахаров (глюкозы, лактозы) йодом в щелочной среде. Массовую долю сахарозы определяют по разности между количеством взятого и неизрасходованного йода, определяемого титрованием тиосульфата натрия. СН2ОН-(СНОН)4-СНО + I2+ 3NaOH = CH2OH-(CHOH)4-COONa +2H2O + 2NaI I2 + 2 Na2S2O3 = NaI + Na2S4O6 Для протекания реакции необходимо чтобы йода было в 2-3 раза было больше, чем требуется для окисления глюкозы, щелочи должно быть в полтора раза больше по объему, чем раствора йода. Массу навески М в граммах рассчитывают по формуле: M = где V – вместимость мерной колбы, см3; Р – предполагаемая массовая доля редуцирующих веществ в исследуемом изделии, %; С – оптимальное содержание редуцирующих веществ в 100 см3 раствора навески, г. Принимаем С = 4 мг/см3. Реактивы: натрия гидроксид, 0,1 моль/ дм3 (0,1 н) и 1 моль/ дм3 (1 н); раствор 100 г/дм3 (10 %-ый); железистосинеродистый калий, раствор 150 г/дм3 (15 %-ый); сульфата цинка, раствор 300 г/дм3 (30 %-ый); соляная кислота раствор 200 г/дм3 (20 %-ый), 0,5 моль/ дм3 (0,5н); йод, 0,1н раствор; тиосульфат натрия, 0,1 н раствор, крахмал, раствор 10 г/дм3 (1 %-ый); метиловый красный, раствор 0,2 г/ дм3 (0,02 %-ный); Материалы, оборудование: электрическая водяная баня; термометр ртутный стеклянный с пределом измерения 150 оС; мерные колбы вместимостью на 100 и 250 см3; фарфоровая ступка с пестиком; пипетка вместимостью 5,10, 50 см3, конические колбы вместимостью 100, 250 см3; мерный цилиндр вместимостью 10 см3. Проведение анализа. Из подготовленной пробы взвешивают навеску, рассчитанную по формуле, с точностью до 0,01 г, растирают ее в ступке с помощью 100-120 см3 дистиллированной воды, прибавляя ее порциями. Затем содержимое ступки количественно переносят в мерную колбу вместимостью 250 см3. Колбу с содержимым нагревают на водяной бане при температуре не выше 60 оС в течение 15 мин при частом взбалтывании, затем содержимое колбы охлаждают до комнатной температуры. К охлажденному раствору прибавляют по 2 см3 15% -ого раствора железисто-синеродистого калия и 30 % -ого сернокислого цинка. Содержимое тщательно перемешивают и через 10-15 мин доводят до метки дистиллированной водой и фильтруют содержимое колбы в сухую колбу через бумажный фильтр. 10 см3 фильтрата используют для определения редуцирующих сахаров йодометрическим методом, 50 см3 фильтрата используют для гидролиза сахаров. Гидролиз дисахаридов. 50 см3 фильтрата переносят в мерную колбу на 100 см3. Туда же приливают 5 см3 20 %-ой соляной кислоты и помещают колбу на 8 мин в водяную баню, нагретую до 70 °С. Затем колбу быстро охлаждают до комнатной температуры, нейтрализуют содержимое 10 % раствором гидроокиси натрия (или калия) в присутствии метилового красного до появления желто-розового окрашивания, доводят водой до метки. Фильтрат используют для определения редуцирующих сахаров после гидролиза. В одну коническую колбу на 200 см3 помещают 10 см3 фильтрата до гидролиза, во вторую 10 см3 после гидролиза. В каждую колбу приливают 25 см3 0,1 н раствора йода и при перемешивании 35 см3 0,1 н раствора NaOH. Колбу закрывают и помещают в темное место на 20 мин. Затем в колбы приливают и 10 см3 0,5 н раствора соляной кислоты. Выделившийся йод титруют 0,1 н раствором тиосульфата натрия до появления светло-желтой окраски. Затем к раствору добавляют 1 см3 крахмала и продолжают титровать, до исчезновения синей окраски. Параллельно проводят контрольный опыт, в котором вместо водной вытяжки берут дистиллированную воду. Массовые доли глюкозы (Х1) до гидролиза и (Х2) после гидролиза процентах рассчитывают по формуле(1.8):
где V1 - объем 0,1 н раствора тиосульфата, израсходованный на титрование в контрольном опыте, см3; V2- объем 0,1 н раствора тиосульфата, израсходованный на титрование в рабочем опыте, см3; 0,009 количество глюкозы, соответствующее 1 см3 0,1 н раствора йода; Р- фактор разведения . Расхождения между параллельными определениями не должны превышать 0,3 %. Массовую долю сахарозы S в процентах в пересчете на сухое вещество рассчитывают по формуле (1.9):
где Х1 – количество редуцирующих сахаров до гидролиза сахарозы, %; Х2 – количество общего сахара после гидролиза дисахаридов, %; 0,95 – коэффициент пересчета инвертного сахара на сахарозу, W – массовая доля воды в продукте
Поиск по сайту: |

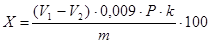 , ( 1.8)
, ( 1.8)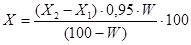 (1.9)
(1.9)