|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Абсорбция и адсорбция. Физические основы процессов. Равновесие между фазами
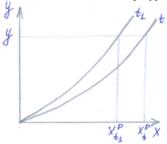
Абсорбцией называют процесс избирательного извлечения одного или нескольких компонентов из газовой смеси жидким поглотителем (абсорбентом). Обратный процесс – выделение из абсорбента растворённых в нём газов носит название десорбции. В абсорбционных процессах участвуют две фазы – жидкая и газовая. При их контактировании один компонент (либо несколько) переходит из одной фазы в другую. При наличии в газовой фазе компонента (компонентов), практически не растворяющегося в жидкой фазе, его называют инертом, или газом-носителем. Растворяющийся компонент – это абсорбируемый компонент, или поглощаемый компонент. В процессах физической абсорбции участвуют как минимум три компонента: два вещества – носителя (газ и жидкость) и компонент, переходящий из одной фазы в другую. Система из двух фаз (ф = 2) при общем числе компонентов к = согласно правилу фаз имеет применительно к равновесному состоянию три степени свободы: j = к – ф + 2 = 3 – 2 + 2 = 3. При полной нерастворимости инерта в абсорбенте и малой летучести последнего состав фаз будет полностью характеризоваться концентрациями поглощаемого компонента в каждой из фаз: х - в жидкой, у – в газовой. Параметрами равновесного состояния системы также являются температура и давление, при которых находится эта система. Таким образом, общее число переменных равновесной системы равно 4. При j = 3 три переменные могут быть выбраны произвольно – соответственно условиям технологического процесса, а четвёртая будет зависимой. Например, можно произвольно выбрать температуру и давление, а также концентрацию ПК (ПК - поглощаемый компонент) в жидкости (Х). Тогда для такой системы равновесная концентрация этого компонента в газовой фазе (уо) будет вполне определённой. Такая зависимость у от х при определённой температуре и давлении называется равновесной – линией равновесия, или кривой равновесия. Константа Генри, характеризующая растворимость газов в жидкости, зависит от свойств растворённого газа и поглотителя, а также от температуры. Зависимость от температуры с некоторым приближением выражается уравнением: lnY = c - q/RT, где q – теплота растворения газа, ккал/кгс×моль. R – газовая постоянная. c – опытная постоянная. Если газы хорошо растворимы и образуют растворы высокой концентрации, а также газы находятся под давлениями, измеряемыми десятками атмосфер, равновесия не следуют закону Генри. Для технических расчётов пользуются полученными из опыта значениями равновесного парциального давления газа Р* и вычисляют равновесное содержание компонента в газовой смеси по формуле ур* = Mк/Мн× Р*/(Р-Р*), кг/кг инертного газа xt1o< xto– растворимость поглощаемого компонента в жидкости понижается
при х = х3(у1р< у2р< у3р) – равновесные концентрации в газовой фазе ПК уменьшается при увеличении Р.
Поиск по сайту: |