 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
СИСТЕМНАЯ СКЛЕРОДЕРМИЯ
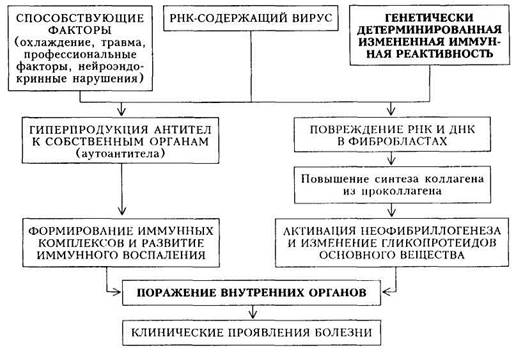
Системная склеродермия (ССД) — системное заболевание соединительной ткани и мелких сосудов, характеризующееся распространенными фиброзно-склеротическими изменениями кожи, стромы внутренних органов и симптоматикой облитерирующего эндартериита в форме распространенного синдрома Рейно. Это определение болезни, данное В.А.Насо- новой (1989), хорошо отражает существо ССД — фиброзную «трансформацию» соединительной ткани, являющейся «каркасом» внутренних органов, составным элементом кожи и кровеносных сосудов. Подобное безудержное развитие фиброза связано с избыточным коллагенообразовани-ем в связи с нарушением функционирования фибробластов. Этиология.В настоящее время придается значение вирусам, так как имеются косвенные свидетельства их роли в возникновении ССД: обнаружены вирусоподобные включения в пораженных тканях и повышенные титры антивирусных антител. Установлена семейно-генетическая предрасположенность к ССД, так как у родственников больных обнаруживают изменения белкового обмена в виде гипергаммаглобулинемии, синдром Рейно, а иногда и ССД. К неблагоприятным факторам, способствующим проявлению болезни и ее обострениям, следует отнести охлаждение, травмы, нарушение нейро-эндокринных функций, профессиональный фактор в виде вибрации. Болезнь в 8— 10 раз чаще встречается у женщин, чем у мужчин. Патогенез.Под влиянием вируса и генетического фактора (при участии предрасполагающих факторов) происходит повреждение РНК и ДНК в фибробластах, что повышает синтез коллагена из проколлагена. Это активирует неофибриллогенез и способствует изменению гликопротеидов основного вещества соединительной ткани. В результате развиваются фиб-розно-склеротические изменения соединительной ткани. Параллельно происходит дисрегуляция иммунного ответа организма на внедрение вируса, что проявляется гиперпродукцией антител к собственным тканям (ау-тоантитела). Затем формируются иммунные комплексы, оседающие в микроцирку ляторном русле и внутренних органах, что приводит к развитию иммунного воспаления, однако выраженность иммунных и аутоиммунных нарушений при ССД не столь велика, как при СКВ. Фиброзно-склеротические изменения соединительной ткани, поражение сосудов и внутренних органов (на основе иммунного воспаления) обусловливают многообразие клинических проявлений заболевания (схема 29). Классификация.В нашей стране принята рабочая классификация ССД, учитывающая характер течения, стадию развития болезни и клинико-морфологическую характеристику поражения органов и систем (табл. 20). Таблица 20. Рабочая клиническая классификация системной склеродермии
Клинические формы: I. Типичная форма (с характерным поражением кожи). Схема 29. Патогенез системной склеродермии
В последние годы стали выделять «пресклеродермию», «диффузную кожную склеродермию», «ограниченную (лимитированную) склеродермию», включающую синдром CREST (об этом синдроме будет сказано ниже), и «склеродерму без склеродермии» (этот вариант весьма редок — не более 5 % всех больных с ССД). Для хронического течения (наиболее частого при ССД) характерны прогрессирующие вазомоторные нарушения по типу синдрома Рейно и обусловленные ими трофические расстройства, что является единствен-
нервной системы
Эзофагит, дуоденит, спруподобный синдром Истинная склеродер- хронический диффузный гломеруло-нефрит, очаговый гломерулонефрит Полиневрит, нейропсихические расстройства, вегетативные сдвиги
ным проявлением заболевания в течение многих лет. В дальнейшем присоединяется уплотнение кожи и периартикулярных тканей с образованием остеолиза и медленно прогрессирующие склеротические изменения внутренних органов (пищевода, сердца, легких). Быстро прогрессирующее течение характеризуется тяжелыми фиброзными периферическими и висцеральными поражениями уже в первый год болезни и нередким поражением почек по типу истинной склеродермичес-кой почки (что является наиболее частой причиной смерти больных). Учитывая прогрессирующий характер болезни, для оценки эволюции и степени нарастания патологического процесса выделяют три стадии течения: Стадия I — начальных проявлений — преимущественно суставные изменения при подостром и вазоспастические — при хроническом течении. Стадия II — генерализации процесса — полисиндромность и полисистемность поражения многих органов и систем. Стадия III — терминальная — преобладание тяжелых склеротических, дистрофических или сосудисто-некротических процессов, нередко с отчетливыми нарушениями функции одного или нескольких органов. Клиническая картина.Болезнь отличается полиморфностью и поли-синдромностью, отражая генерализованный характер заболевания в целом. Практически нет органа или системы, которые не могли бы быть вовлечены в патологический процесс. На I этапе диагностического поиска получают информацию, на основании которой можно составить представление о диагнозе и варианте начала болезни, характере течения процесса, вовлечении в патологический процесс различных органов, проводимом ранее лечении и его эффективности, а также осложнениях. Чаще болезнь начинается с поражения кожи, затем постепенно присоединяется поражение органов (типичная форма); в других случаях (атипичная форма) в клинической картине с самого начала доминирует поражение внутренних органов при минимальных кожных проявлениях, что затрудняет диагностику. По мере течения болезни можно составить представление о характере течения (острое, подострое, хроническое). Жалобы больных при вовлечении в патологический процесс внутренних органов соответствуют субъективным симптомам при том или ином их поражении (плеврит, артрит, синдром Рейно, дуоденит и пр.). Вместе с тем больные могут предъявлять жалобы, наиболее часто встречающиеся именно при ССД: затруднение глотания и поперхивания при глотании (в результате поражения верхней части пищевода). Вазоспастические нарушения при синдроме Рейно не ограничиваются пальцами рук, а распространяются на кисти, стопы, нередко больные испытывают чувство онемения в области губ, какой-либо части лица, кончика языка. Предъявляются жалобы на сухость слизистой оболочки рта, конъюнктивы, невозможность плакать («нет слез»). Поражение кожи лица проявляется ощущением «стянутости» кожи и рта (трудно of крыть рот). Как правило, температура тела не повышена. Похудание (иногда значительное) отмечается обычно при прогрессировании и генерализации болезни. Проводившаяся ранее терапия: кортикостероиды (длительность, дозы), а также другие средства (D-пеницилламин, аминохинолиновые производные, нестероидные противовоспалительные препараты, физиолечение) — позволяет косвенно судить о характере течения и остроте процесса. После I этапа (при длительном течении болезни) можно сделать определенное заключение о диагнозе. Сделать это в самом начале бывает крайне трудно, так как проявления ССД существенно напоминают другие заболевания из группы диффузных заболеваний соединительной ткани (СКВ, РА, ДМ), а при моно(олиго)синдромности — другие заболевания, характеризующиеся поражением лишь одного органа (сердце, легкие и пр.). На II этапе диагностического поиска получают данные, свидетельствующие о поражении органов и систем и их функциональной недостаточности. При развернутой клинической картине болезни поражение кожи наблюдается у подавляющего большинства больных и выражается в последовательном развитии отека, индурации, а затем атрофии (с преимущественной локализацией на лице и кистях). Возможны также трофические изменения кожи в виде депигментации, подчеркнутого сосудистого рисунка и телеангиэктазий. Поражение слизистой оболочек выражается в повышенной сухости. На коже могут появляться изъязвления, гнойничковая сыпь; волосы выпадают, ногти деформируются. В конечной стадии болезни кожа лица становится плотной, не берется в складку, лицо амимично, маскообразно. Характерная форма рта: губы тонкие, собраны в нерас-правляющиеся складки, постепенно теряется способность широко раскрывать рот (симптом «кисета»). Вазоспастические изменения при синдроме Рейно в виде побеления кожной поверхности отмечаются в области лица, губ, кистей и стоп. Изменение суставов проявляется в их дефигурации за счет преимущественного поражения периартикулярных тканей, а также истинного склеродермического полиартрита с преобладанием экссудативно-пролифе-ративных или фиброзно-индуративных изменений. Характерно развитие «склеродермической кисти»: укорочение пальцев (вследствие остеолиза ногтевых фаланг), истончение их кончиков, деформация ногтей, легкие сгибательные контрактуры. Такую кисть сравнивают с птичьей лапой (склеродактилия). Поражение мышц, морфологически представляя собой фиброзный интерстициальный миозит или миозит с дистрофическими и некротическими изменениями, выражается в миастеническом синдроме, атрофии, уменьшении мышечной массы и нарушении движений. В мышцах возможны болезненные уплотнения (кальцинаты). Особенно часто отложения солей кальция наблюдаются в мягких тканях пальцев рук. Поражение пищеварительного тракта: эзофагит, дуоденит, синдром нарушенного всасывания или упорные запоры — в основном выявляется на I и III этапах диагностического поиска. Поражение органов дыхания выражается в виде пневмонита, протекающего остро или хронически, вяло. Физикальные данные крайне скудны, в выраженных случаях выявляют только эмфизему легких. Значительно большую информацию дает рентгенологическое исследование, оказывающее существенную помощь и при выявлении двустороннего базального пнёвмосклероза, характерного для ССД. При выраженном пневмосклерозе и длительном его существовании развивается легочная гипертензия, приводящая вначале к гипертрофии правого желудочка, а затем к его недостаточности. Легочная гипертензия проявляет себя цианозом, акцентом II тона во втором межреберье слева от грудины, одышкой, резким снижением толерантности к физической на- грузке, резким усилением пульсации в эпигастрии (обусловленной гипертрофией правого желудочка). Поражение сердца занимает основное место среди висцеральных проявлений ССД как по частоте, так и по влиянию на исход болезни. Для ССД характерен так называемый первичный кардиосклероз, не связанный с предшествующими некротическими или воспалительными изменениями миокарда. Отмечают увеличение сердца (иногда значительное), а также нарушения сердечного ритма в виде экстрасистолии или мерцательной аритмии. Поражение эндокарда приводит к развитию порока сердца, практически всегда — митральной недостаточности. Сочетание кардиосклероза и митральной недостаточности может обусловить в ряде случаев развитие сердечной недостаточности со всеми характерными ее признаками. Перикардит при ССД наблюдается редко и протекает чаще как сухой. Поражение мелких сосудов — «склеродермическая ангиопатия» — проявляется в виде вазомоторных нарушений (синдром Рейно), в выраженных случаях приводит к кровоизлияниям, некрозу тканей пальцев, те-леангиэктазиям. Поражение почек при ССД обусловлено патологией сосудов и проявляется в виде очагового или диффузного гломерулонефрита. При поражении почек в виде изолированной патологии мочевого осадка физикальное исследование не выявляет никаких существенных патологических признаков. Диффузный гломерулонефрит с формированием АГ приводит к увеличению левого желудочка, акценту II тона во втором межреберье справа от грудины. В основе поражения ЦП С лежат сосудистые, дистрофические и фиброзные изменения, проявляющиеся симптоматикой полиневрита с нарушением рефлексов и чувствительности. Таким образом, после II этапа выявляется полиорганность поражения с преимущественным поражением кожи и ее дериватов. Степень выявленных изменений весьма различная — от субклинических до значительно выраженных. Возможность постановки диагноза ССД при преимущественном поражении кожи более высокая, чем в случаях преобладания висцеральных поражений. В последнем случае имеются предпосылки для диагностических ошибок, если на первый план выступает поражение какого-нибудь одного органа (почки, сердце). На III этапе диагностического поиска возможно: 1) определить степень активности процесса; 2) уточнить выраженность поражения внутренних органов; 3) провести дифференциальную диагностику с другими заболеваниями из группы хронических диффузных поражений соединительной ткани. В определении степени активности наибольшее значение имеют неспе-цифические острофазовые показатели, к которым относятся: а) диспро-теинемия с повышением уровня осг- и у-глобулинов; 6) появление СРВ; в) увеличение содержания фибриногена; г) повышение СОЭ. О наличии и выраженности иммунных нарушений можно судить по обнаружению ревматоидного фактора (выявляется в 40 —50 % случаев), антинуклеарных антител (в 30 —90 %), LE-клеток (в 2 —7 %). В отличие от СКВ все эти показатели при СКД выявляются в значительно меньшем титре и реже. В настоящее время диагностическое значение придается так называемым склеродермическим антителам: антитело Scl-70 и антитело к центромере (центромера является элементом хромосомы). Из прочих показателей, указывающих на нарушение обмена коллагена, следует отметить увеличение содержания оксипролина в моче и крови. При поражении почек наблюдается выраженная в той или иной степени протеинурия в сочетании с минимальными изменениями мочевого осадка (микрогематурия, цилиндрурия). При «истинной склеродермической почке» (развитие некрозов почечной ткани вследствие поражения почечных сосудов) может возникнуть острая почечная недостаточность с увеличением содержания в крови мочевины и креатинина. В целом же при ССД отмечается диссоциация между выявляемыми при пункционной биопсии выраженными морфологическими изменениями почечной ткани и сосудов и сравнительно умеренными клиническими (в том числе лабораторными) проявлениями поражения почек. Если вследствие поражения почек развивается А Г, то отмечаются изменения глазного дна (сужение артерий и расширение вен). При поражении сердца на ЭКГ — неспецифические изменения конечной части желудочкового комплекса (снижение амплитуды и инверсия зубца Г), иногда нарушения внутриже луд очковой проводимости. Рентгенологически определяется увеличение сердца. Рентгенография помогает обнаружить кальцинацию мышц и мягких тканей пальцев кисти, а также дифференцировать изменения суставов при ССД от изменений при РА (при ССД не выявляются эрозии суставных поверхностей). В 60 — 70 % случаев на рентгенограмме отмечается поражение пищеварительного тракта, особенно пищевода и кишечника. Изменения пищевода выражаются в виде диффузного его расширения в сочетании с сужением в нижней трети, ослаблением перистальтики и некоторой ригидностью стенок. При биопсии кожи, синовиальной оболочки и мышц выявляются характерные для ССД фиброзные изменения, а также изменение сосудов. Однако данные морфологического исследования не оказывают решающего значения в постановке диагноза. Диагностика. Распознавание болезни основывается на выявлении «больших» и «малых» диагностических критериев. «Большие» критерии: • проксимальная склеродерма — симметричное утолщение, уплотне «М алые» критерии: • склеродактилия — перечисленные выше кожные изменения, огра • рубцы на кончиках пальцев или потеря вещества подушек пальцев; • двусторонний базальный легочный фиброз. У больного ССД должен быть либо главный критерий («большой»), либо по крайней мере два из «малых» критерия. Наиболее типично для ССД сочетание кальциноза, синдрома Рейно, эзофагита, склеродактилии и телеангиэктазий (синдром CREST — по первым буквам английских наименований перечисленных симптомов). Диагностика ССД на ранних стадиях болезни основывается на наличии «триады» первоначальных признаков (появляющихся наиболее 18-540 рано): синдром Рейно + суставной синдром (чаще полиартралгии) + плотный отек кожи. Существенно реже в ранней стадии обнаруживается одна из висцеральных локализаций процесса. Значительные трудности в диагностике ССД наблюдаются при отсутствии характерного кожного синдрома у больных с выраженной полисин-дромной висцеральной патологией (так называемая ССД без склеродермии). В этих случаях существенную помощь оказывает рентгенологическое исследование, выявляющее нарушение моторики пищевода и его расширение, дилатацию двенадцатиперстной кишки и толстой кишки. Дифференциальная диагностика.ССД следует дифференцировать от целого ряда заболеваний и прежде всего от других диффузных заболеваний соединительной ткани, а также болезней, клиническая картина которых весьма сходна с клинической картиной поражения какого-либо органа при ССД (при условии доминирования поражения этого органа). Например, при склеродермическом поражении сердца — с атеросклеротичес-ким кардиосклерозом, ревмокардитом, неспецифическим миокардитом; при легочном поражении — с хронической пневмонией, туберкулезом, профессиональными заболеваниями легких (пневмокониоз); при поражении пищевода следует исключить рак пищевода. Основой для такой дифференциации являются типичные для ССД признаки. • Преобладание своеобразных кожных поражений в сочетании с син • В отличие от СКВ при ССД поражение внутренних органов не со • Суставной синдром при ССД в отличие от РА сочетается с мышеч • Поражение сердца при ССД в отличие от ИБС не сопровождается • Доминирующее поражение какой-либо системы или органа при • При ССД доминируют кожные поражения и синдром Рейно, тогда нии со своеобразным параорбитальным отеком лилового цвета (симптом очков). • Кортикостероиды при ССД не дают такого разительного положи В ряде случаев, когда ССД проявляется суставным, кожным и асте-новегетативным синдромами, лишь длительное динамическое наблюдение позволяет поставить правильный диагноз. Формулировка развернутого клинического диагнозаучитывает рубрики, приведенные в рабочей классификации; диагноз должен отражать: 1) характер течения; 2) стадию; 3) клинико-морфологическую характеристику поражения органов и систем организма с указанием стадии функциональной недостаточности (например, при пневмосклерозе — стадию легочной недостаточности, при поражении почек — стадию почечной недостаточности и пр.). Лечение.Терапия при ССД должна быть комплексной и учитывать следующие аспекты: 1) воздействие на фиброзообразование; 2) иммуносупрессия и противовоспалительное действие; 3) воздействие на нарушение микроциркуляции; 4) воздействие на локальные проявления болезни. • Препаратом, разрушающим внутренние связи в молекуле коллаге Если лечение D-пеницилламином осложняется кожными высыпаниями, то дозу препарата уменьшают и дополнительно назначают преднизо-лон (10 — 15 мг/сут). При лечении D-пеницилламином необходимо следить за анализами мочи, так как на б—12-м месяце от начала лечения может появиться протеинурия (при ее нарастании до 0,2 r/сут препарат отменяют). Колхицин также влияет на метаболизм коллагена. Начальная доза — 0,5 мг/сут, постепенно ее повышают до 10 мг в неделю (препарат можно принимать 1V2 — 4 года). При выраженных кожных поражениях показана ферментотерапия — лидаза в виде подкожных инъекций вблизи пораженных участков или электрофорез с этим препаратом. • При ССД с висцеральными поражениями целесообразно назначить 18» При отсутствии эффекта, выраженном побочном действии, противопоказаниях (хотя положительный эффект наблюдается) назначают цитостати-ки — азатиоприн в дозе 1 —3 мг на 1 кг массы тела (150 — 200 мг/сут) в течение 2 — 3 мес, обычно в сочетании с 15 —20 мг преднизолона в сутки. При хроническом течении болезни (изолированное кожное поражение) рекомендуется длительное применение аминохинолиновых препаратов — хингамин (делагил), гидроксихлорохил (плаквенил). • Для улучшения микроциркуляции назначают сосудорасширяющие • Воздействие на локальные проявления болезни предусматривает Прогноз.При ССД прогноз определяется вариантом течения и стадией развития. Отмечено, что чем больше времени отделяет развернутую стадию от первых проявлений болезни (в частности, синдрома Рейно), тем благоприятнее прогноз. Профилактика.К группе «угрожаемых» относят лиц со склонностью к вазоспастическим реакциям, полиартралгиям, а также родственников больных, страдающих различными диффузными заболеваниями соединительной ткани. Такие лица не должны подвергаться воздействию провоцирующих факторов (охлаждение, вибрация, травматизация, воздействие химических веществ, инфекции и пр.). Больных ССД ставят на диспансерный учет. Систематически проводимое лечение (в частности, правильно подобранная поддерживающая терапия) является лучшим средством профилактики обострений. ДЕРМАТОМИОЗИТ Дерматомиозит (ДМ) — системное воспалительное заболевание скелетной и гладкой мускулатуры и кожи; реже отмечается вовлечение в патологический процесс внутренних органов. При отсутствии поражения кожи используют термин «полимиозит». Сущность заболевания состоит в прогрессирующем тяжелом некротическом миозите с преимущественным поражением мышц проксимальных отделов конечностей. По мере прогрессирования заболевания мышечная ткань атрофируется и замещается фиброзной. Аналогичные процессы наблюдаются и в миокарде. В паренхиматозных органах развиваются дистрофические процессы, в патологический процесс вовлекаются также сосуды мускулатуры, внутренних органов и кожи. Дерматомиозит — редкое заболевание. Болезни подвержены люди всех возрастных групп — от детей до стариков, но обычно болеют дети до 15 лет и лица зрелого возраста (40 — 60 лет). Женщины болеют в 2 раза чаще, чем мужчины. Этиология.Выделяют две формы ДМ — идиопатический и вторичный опухолевый. Этиология идиопатического ДМ неизвестна. Однако известны факторы, способствующие выявлению (а в дальнейшем и обострению) данного заболевания: 1) инсоляция; 2) охлаждение; 3) инфекция (ОРЗ, грипп, ангина и пр.); 4) гормональная .перестройка (климакс, беременность, роды); 5) эмоциональный стресс; 6) физическая травма, хирургическое вмешательство; 7) сенсибилизация лекарственными препаратами (аминазин, инсулин, антибиотики, D-пеницилламин); 8) вакцинация; 9) контакт с эпоксидными смолами, фоторастворителями; 10) физиотерапевтические процедуры. В развитии ДМ имеет значение, по-видимому, наследственно-генетическая предрасположенность (у больных обнаруживается антиген гисто-совместимости В-8). Опухолевый (вторичный) ДМ составляет 25 % всех случаев заболевания и развивается у больных, страдающих злокачественными опухолями. Наиболее часто ДМ возникает при раке легкого, кишечника, предстательной железы, яичника, а также при гемобластозах. Появление ДМ у лиц старше 60 лет почти всегда указывает на опухолевое его происхождение. Патогенез.Под влиянием вируса и генетического фактора (при участии предрасполагающих факторов) или опухолевых антигенов происходит нарушение (дисрегуляция) иммунного ответа, выражающееся в дисбалансе В- и Т-системы лимфоцитов: в организме вырабатываются антитела к скелетным мышцам, происходит сенсибилизация к ним Т-лимфоцитов. Реакция антиген — антитело и цитотоксический эффект сенсибилизированных к мышцам Т-лимфоцитов способствуют образованию иммунных комплексов и отложению их в мышцах, а также в микроциркуляторном русле различных органов. Элиминация иммунных комплексов приводит к высвобождению лизосомных ферментов и развитию иммунного воспаления в мышцах и внутренних органах. При воспалении высвобождаются новые антигены, способствующие дальнейшему образованию иммунных комплексов, что ведет к хронизации заболевания и вовлечению в патологический процесс не пораженных ранее мышц. Патогенез ДМ представлен на схеме 30. Клиническая картина.Проявления болезни отличаются системностью и полисиндромностью. Основными синдромами являются: 1) мышечный (миозит, мышечные атрофии, кальцификация); 2) кожный (эритема, отек кожи, дерматит, пигментация и депигментация, телеангиэктазии, гиперкератоз, крапивница); 3) суставной (артралгии, поражение периарти-кулярных тканей, истинные артриты встречаются редко); 4) висцеральный (миокардит, кардиосклероз; пневмонит, аспирационные пневмонии, пневмофиброз; желудочно-кишечные кровотечения; «миоглобулинуричес-кая почка» с развитием ОПН; полинейропатии). Выделяют следующие периоды течения болезни: I период (начальный) — от нескольких дней до 1 мес и более, проявляется только мышечными и(или) кожными признаками; II период (манифестный) — определяется развернутая картина болезни;
III период (терминальный) проявляется дистрофическими изменениями внутренних органов и признаками выраженной их функциональной недостаточности; в этом периоде наблюдаются осложнения. Различают три формы течения болезни: 1) острая: быстро нарастает генерализованное поражение скелетной 2) подострая: более медленное, постепенное нарастание симптомати 3) хроническая: длительное циклическое течение; преобладают про На I этапе диагностического поиска получают сведения о характере начала заболевания: острое (повышение температуры тела до 38 — 39 °С, кожная эритема и боли в мышцах) или постепенное (умеренная слабость, нерезкие миалгии и артралгии, усиливающиеся после физической нагрузки, инсоляции или других неблагоприятных воздействий). Наиболее характерные жалобы обусловлены мышечными поражениями: больные отмечают слабость, не могут самостоятельно сесть или встать, им крайне трудно подниматься по лестнице, нередки боли в мышцах. Мышечная слабость и болезненность локализуются симметрично в проксимальных отделах конечностей, а также в спине и шее. При поражении глоточных мышц больные жалуются на поперхивание при глотании, жидкая пища выливается через нос. Носовой оттенок голоса, охриплость обусловлены поражением мышц гортани. При поражении кожи больные отмечают стойкое изменение ее окраски в местах, подверженных действию солнца («зона декольте», лицо, кисти), а также на наружных поверхностях бедер и голеней. Характерно появление параорбитального отека лилового цвета (симптом очков). При поражении слизистых оболочек больные жалуются на сухость, жжение в глазах, отсутствие слез («сухой синдром»). Вовлечение в патологический процесс различных органов проявляется симптомами, свойственными миокардиту, кардиосклерозу, пневмониту, гломерулонефриту, полиневриту, артриту и пр. Сведения о проводимом лечении позволяют судить об его адекватности, а косвенно и о характере течения: использование аминохинолиновых препаратов свидетельствует о хроническом течении, применении предни-золона и цитостатиков — о более остром течении болезни. На II этапе диагностического поиска при развернутой клинической картине болезни прежде всего обращает внимание симметричное поражение мышц: плотные, тестоватые на ощупь, увеличены в объеме, болезненны при пальпации. При поражении мимической мускулатуры отмечается некоторая маскообразность лица. В дальнейшем наблюдается атрофия мышц, особенно выраженная со стороны плечевого пояса. Поражаются также дыхательные мышцы и диафрагма. При пальпации мышц можно обнаружить локальные уплотнения — кальцинаты, которые располагаются и в подкожной жировой клетчатке. Кальциноз чаще развивается у молодых людей с распространенным поражением мышц при переходе острого течения в подострое или хроническое. Нередко отмечается снижение массы тела на 10 — 20 кг. Поражение кожи не является обязательным для ДМ, но при его наличии на открытых частях тела отмечаются отек, эритема (в особенности над суставами — так называемая надсуставная, а также в околоногтевых зонах в сочетании с микронекрозами в виде темных точек — синдром Готтрона), капилляриты, петехиальные высыпания, телеангиэктазии. Эритема отличается большой стойкостью, синюшным оттенком, сопровождается зудом и шелушением. Типичен симптом очков. Нередко отмечаются сухость кожи, ломкость ногтей и повышенное выпадение волос. Довольно часто встречается достаточно выраженный синдром Рейно. Физикальные проявления висцеральных поражений при ДМ, так же как и при ССД, не слишком ярки в отличие от СКВ. Можно отметить известную диссоциацию между выраженностью патоморфологических изменений органов и их клиническим проявлением. Поражение сердца (миокардит, кардиосклероз) проявляется такими неспецифическими признаками, как увеличение размеров его, глухость тонов, тахикардия, нарушение ритма в виде экстрасистолии. Выраженные изменения миокардита могут привести к появлению симптомов сердечной недостаточности. Поражение легких в виде пневмонита проявляется крайне скудно. Развивающийся фиброз обнаруживают по признакам эмфиземы легких и дыхательной недостаточности. Аспирационная пневмония характеризуется всеми свойственными пневмонии физикальными симптомами. Для поражения пищеварительного тракта характерна дисфагия: твердая пища срыгивается, а жидкая выливается через нос. Поражение сосудов желудка и кишечника может привести к желудочно-кишечным кровотечениям со всеми характерными для этого осложнения признаками. Иногда отмечается умеренное увеличение печени, реже — гепатолиеналь-ный синдром с увеличением лимфатических узлов. Неврологическая симптоматика проявляется изменениями чувствительности: гиперестезией периферического или корешкового характера, гипералгезией, парестезией и арефлексией. На III этапе диагностического поиска существенную помощь оказывают методы исследования, позволяющие оценить остроту воспалительного процесса и распространенность поражения мышц. Об остроте процесса можно судить по неспецифическим острофазовым показателям (увеличение СОЭ, повышение содержания фибриногена и СРБ, гипер-аг-глобулинемия) и показателям, свидетельствующим об иммунных сдвигах (появление в невысоком титре ревматоидного фактора, увеличение содержания у-глобулинов, антител к нуклеопротеиду и растворимым ядерным антигенам; выявляются также антитела Mi2, Jol, SRP; в случае идиопатического ДМ — повышается содержание IgG). При хроническом, вялом течении болезни изменения острофазовых показателей могут отсутствовать (СОЭ может быть не увеличена). Распространенность поражения мышц характеризуется рядом биохимических показателей. Повышаются уровень сывороточных ферментов (ACT, AJIT, КФК, альдолаза), индекс креатин/креатинин за счет появления в моче креатина при снижении креатинурии. При значительном поражении мышц может наблюдаться миоглобинурия. Для ДМ опухолевого происхождения характерно увеличение аглииопротеиновой фракции сыворотки крови. Существенную помощь в диагностике поражения мышц оказывает электромиография, выявляющая нормальную электрическую активность мышц в состоянии произвольного их расслабления и низкоамплитудную при произвольных сокращениях. Биопсия кожи и мышц обнаруживает картину тяжелого миозита с потерей поперечной исчерченности мышечных волокон, фрагментацией, зернистой и восковидной дегенерацией, очаги некроза, лимфоидно-плазмо-клеточную инфильтрацию, явления фиброза. Прочие методы исследования (ЭКГ, рентгенологические и эндоскопические) необходимы для: 1) оценки состояния пораженных внутренних органов; 2) поисков опухоли при подозрении на ДМ опухолевого происхождения. Диагностика.При распознавании заболевания принимают во внимание следующие критерии: 1) симметричная проксимальная мышечная слабость; 2) результаты биопсии мышц, указывающей на некроз, лимфоидно- 3) повышение в крови содержания ферментов (на 50 % и более), ука 4) типичные электромиографические изменения (нормальная элект 5) поражение кожи. Диагноз ДМ ставится при наличии первого критерия и любых двух других. Дифференциальная диагностика.ДМ следует дифференцировать от инфекционных и неврологических заболеваний, ССД, СКВ, РА. Основой такой дифференциации могут явиться: • Упорство суставного синдрома при РА, обнаружение при рентгено • В отличие от СКВ при ДМ висцеральная патология не столь резко • В отличие от ССД кожные изменения при ДМ имеют совершенно • При остром течении ДМ необходимо исключить инфекционную па • При доминировании адинамии, нарушении рефлексов возникает не Формулировка развернутого клинического диагнозаДМ должна отражать: 1) период течения; 2) форму течения; 3) клинико-морфологи-ческую характеристику поражения систем и органов с указанием ведущих синдромов и наличия (отсутствия) функциональной недостаточности органов (систем). Лечение.Главной задачей является подавление активности иммунных реакций и воспалительного процесса на иммунной основе, а также нормализация функции отдельных, наиболее пораженных органов и систем. Лучший эффект оказывают глюкокортикоидные препараты: при ДМ предпочтительнее всего назначать преднизолон (в среднем 1 мг/(кгсут). Дозы и длительность применения зависят от остроты процесса и клинического эффекта. При остром течении назначают 80—120 мг/сут, при подостром — 60 мг/сут, при обострении хронического течения -—30 — 40 мг/сут. Преднизолон следует принимать 2 — 3 мес и более до достижения отчетливого клинического эффекта. Затем дозу очень медленно снижают до поддерживающей: на 1-м году болезни при исходном остром или подостром течении она составляет 30 — 40 мг/сут, на 2 —3-м году — 10 — 20 мг/сут. Если лечение преднизолоном не дает эффекта или невозможно его использовать вследствие непереносимости и развития осложнений, то следует назначить цитостатические препараты. Чаще всего применяют азатио-прин (имуран) в дозе 1 —3 мг на 1 кг массы тела в течение 2 — 6 мес; при сочетании с преднизолоном дозу можно уменьшить. Цитостатики принимают в течение 2 — 6 мес, а затем дозу снижают. Вместе с тем следует помнить, что отсутствие эффекта от лечения преднизолоном указывает на возможность опухолевого дерматомиозита, поэтому, прежде чем назначать цитостатические препараты, следует провести расширенный онкологический поиск для исключения злокачественной опухоли. Аминохинолиновые препараты хингамин (делагил), гидроксихлоро-хин (плаквенил) применяют в следующих ситуациях: 1) при хроническом течении болезни без признаков активности про 2) при снижении дозы преднизолона или цитостатиков для уменьше Дополнительные методы лечения: 1) при доминирующем болевом суставном синдроме назначают несте 2) при длительном применении преднизолона следует использовать 3) при кальцинатах используют комплексоны (динатриевая соль Прогноз.В настоящее время в связи с применением преднизолона и цитостатиков при острых и подострых формах прогноз значительно улучшился. В случае перехода в хроническое течение трудоспособность больного может восстанавливаться. Прогноз при вторичном (опухолевом) ДМ зависит от эффективности оперативного вмешательства: при успешно проведенной операции все признаки болезни могут исчезнуть. Профилактика.Предупреждение обострений (вторичная профилактика) достигается проведением поддерживающей терапии, санации очагов инфекции, повышением сопротивляемости организма. Для родственников больного возможна первичная профилактика (исключение перегрузок, инсоляции, переохлаждений). КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ На вопросы 189 — 204 выберите один наиболее правильный ответ. 189. Системная красная волчанка обычно встречается у: А. Пожилых женщин. 190. У молодых женщин нефрит наиболее часто может быть проявлением: A. Дерматомиозита. Б. Системной красной волчанки. В. Системной склеродермии. 191. Истинные LE-клетки являются: А. Нейтрофильными лейкоцитами, фаго 192. Гемолитическая анемия с положительной реакцией Кумбса может наблю B. Системной красной волчанке. Г. Узелковом периартериите. Д. Дерматомиозите. 193. В стационар поступила женщина 35 лет с жалобами на сухой кашель, одышка. В последние месяцы нарастает похудание, выпадают волосы, на лице появились красные высыпания. При осмотре: деформация проксимальных, межфалан-говых суставов, расширение сердца в обе стороны, глухие тоны сердца, систолический шум на верхушке; АД 150/100 мм рт.ст. При рентгеноскопии легких — плев-родиафрагмальные спайки: утолщение междолевой плевры, увеличение левого желудочка. Анализ крови: НЬ 10,6 г/л, эритроцитов 3,2'1012/л, лейкоцитов 4,3-109/л (формула без особенностей); СОЭ 60 мм/ч. Анализ мочи: плотность 1,016, белок — 1,65 %о, в осадке эритроцитов 8—10 в поле зрения, гиалиновые цилиндры — 4 — 5 в поле зрения. Наиболее вероятный диагноз: А. Ревматоидный артрит. Б. Ревматизм. В. Системная красная волчанка. Г. Хронический гломерулонефрит. Д. Системная склеродермия. 194. Один из следующих признаков не встречается при системной склеродер 195. При дерматомиозите встречаются перечисленные признаки, за исключени 196. Мужчины наиболее часто заболевают: А. Дерматомиозитом. Б. Системной 197. У 42-летней женщины в течение 15 лет синдром Рейно. В последний год 198. Выберите из данных признаков классическую триаду СКВ: А. Миокар 199. При СКВ наблюдаются следующие симптомы, за исключением одного: 200. При каком заболевании наиболее часто встречается синдром Рейно: A. Системная красная волчанка. Б. Дерматомиозит. В. Хронический гепатит (ауто 201. Какой признак не входит в понятие «CREST-синдром»: А. Эзофагит. 202. Что из перечисленных препаратов не следует применять для улучшения B. Ксантинола никотинат. Г. Верапамил. Д. Пропранолол. 203. У 25-летней девушки после возвращения с летнего отдыха в горах появи 204. У 45-летней больной системной склеродермией в течение 3 мес наблюда
Ревматоидный артрит........................................................... 540 Остеоартроз................................................................................ 553 Подагра......................................................................................... 559 Идиопатический анкилозирующий спондилоартрит (болезнь Бехтерева).................................................................................. 566 Контрольные вопросы и задачи.......................................... 570 Поражения суставов различной природы встречаются достаточно часто в клинике внутренних болезней. Заболевания суставов могут быть самостоятельной нозологической формой (ревматоидный артрит, деформирующий остеоартроз), проявлением патологии других систем (артрит при СКВ, ССД) или же быть реакцией на иной патологический процесс (реактивные артриты при какой-либо острой инфекции). Все многообразие патологии суставов может быть сведено к двум формам — артриты (воспалительные поражения суставов вне зависимости от непосредственной причины — инфекция, аутоиммунные процессы или выпадение микрокристаллов солей в синовиальной жидкости) и артрозы (дистрофически-дегенеративные поражения). В данной главе будут рассмотрены наиболее частые заболевания суставов — ревматоидный артрит, деформирующий остеоартроз и подагра. РЕВМАТОИДНЫЙ АРТРИТ Ревматоидный артрит (РА) — хроническое системное воспалительное заболевание соединительной ткани с преимущественным поражением суставов по типу эрозивно-деструктивного прогрессирующего полиартрита. Сущность заболевания состоит в поражении суставных тканей (синовиальная оболочка, суставной хрящ, капсула сустава) воспалительным процессом, развивающимся на иммунной основе и приводящим к эро- зиям суставных поверхностей костей с последующим формированием выраженных деформаций и анкилозов. В основе нередко наблюдающихся внесуставных поражений лежит иммунокомплексный васкулит, вызывающий поражение внутренних органов и систем. Этиология.Причина развития РА неизвестна. Придают значение вирусной инфекции (вирус Эпштейна — Барр), а также другим инфекционным факторам (стрептококки группы В, микоплазма). Молекулярные компоненты микробных клеток, продукты разрушения последних обладают тропизмом к суставным тканям, способны длительно персистировать в них и вызывать характерный иммунный ответ. Вирусы, встраиваясь в ДНК клеток хозяина, могут индуцировать синтез и секрецию неинфекционных белков, обладающих антигенной способностью, что является стимулом к развертыванию иммунных реакций. Предполагается, что вирус Эпштейна — Барр может длительно существовать в организме лиц с генетической предрасположенностью к такому персистированию, что ведет к нарушению супрессорной функции Т-клеток и нарушению продукции иммуноглобулинов В-лимфоцитами. Генетическим факторам в настоящее время придается значение в происхождении данного заболевания: так, определенный антиген гистосов-местимости (HLA DRW4) встречается у 52 % больных РА и лишь у 13 % в популяции. Отмечается повышенная заболеваемость РА родственников больного. Патогенез.Под влиянием гипотетических этиологических факторов повреждается синовиальная оболочка сустава, в результате чего развивается ответная местная иммунная реакция, которая сопровождается образованием агрегированных IgG (а также IgA и IgM). Этот измененный IgG (IgA, IgM) распознается иммунной системой как чужеродный антиген, поэтому иммунокомпетентные клетки синовиальной оболочки (плазмоци-ты), а также лимфатических узлов и селезенки начинают вырабатывать антитела к нему — так называемый ревматоидный фактор (РФ). Агрегированный IgG (IgA, IgM) взаимодействует с РФ и комплементом, в результате чего в суставной жидкости и синовиальной оболочке образуются иммунные комплексы. В ответ на это возникает иммунное воспаление, сопровождающееся дальнейшим повреждением тканей суставов и стимулированием иммунного ответа. Развивается и расширяется инфильтрация синовиальной оболочки плазматическими клетками и сенсибилизированными лимфоцитами, которые повреждают ткани. В воспалительном процессе участвуют нейтрофилы, выделяющие большое количество медиаторов воспаления. Иммунные комплексы плохо удаляются из организма, что способствует переходу воспалительного процесса в хронический. Главная особенность артрита — образование и разрастание рыхлой грануляционной соединительной ткани (так называемый паннус), которая постепенно разрушает хрящ и эпифизы костей с образованием узур (эрозий). Исчезновение хряща ведет к развитию фиброзного, а затем и костного анкилоза сустава. Деформацию суставов обусловливает и изменение периартикуляр-ных тканей (капсулы сустава, сухожилий и мышц). Кроме поражений суставов, при РА практически всегда наблюдаются изменения соединительной ткани, органов и систем. Морфологической основой их поражения являются васкулиты и лимфоидная инфильтрация. Патогенез РА представлена на схеме 31.
Классификация.В настоящее время в нашей стране принята рабочая классификация РА (Пленум Всесоюзного общества ревматологов, 1980), учитывающая клинико-анатомическую и клинико-иммунологическую характеристику процесса, характер течения, степень активности, рентгенологическую стадию артрита и функциональную активность больного (табл. 21). Клиническая картина.На Iэтапе диагностического поиска выясняют основные жалобы больного (как правило, связанные с поражением суставов), а также вариант начала заболевания. Выделяют подострое (чаще), острое начало заболевания, а также постепенное развитие симптомов. При подостпром начале РА поражение суставов является главным клиническим проявлением заболевания, выражается в виде стойкой поли-артралгии; у 2/5 больных с самого начала отмечаются признаки артрита. Суставные боли достаточно характерны: наиболее интенсивны во второй половине ночи и утром; в течение дня и особенно к вечеру они уменьшаются. Другой важный симптом развития РА — скованность движений по утрам. Она может исчезнуть через 20 — 30 мин после подъема больного или сохраняться в течение всего дня. При остром начале отмечаются высокая температура тела, резкие боли в суставах в результате развития полиартрита, значительная скованность движений. Температура тела может быть гектического типа. Кроме жалоб на боли и скованность, больные отмечают резкое ухудшение общего состояния. Таблица 21. Рабочая классификация ревматоидного артрита
Клинико-иммуноло-гичсская характеристика Течение болезни Степень активности Рентгенологическая стадия Функциональная активность больного
II. Ревматоидный арт III. В сочетании с ос- Серопо-зитивный Сероне-гативный Медленно прогрессирующее (классическое) Быстро прогрессирующее Без заметного про-грессирова-ния (добро-рокачест-венное, малопрогрессирующее) I.Мини II. Сред III. Вы I. Окулосус- II. Остеопо- III. Остеопо- IV. То же +
0. Сохра 1. Профес II. Про III. Утра
Чаще всего в начале заболевания поражаются мелкие суставы: луче-запястные, пястно-фаланговые, проксимальные межфаланговые, реже за-пястно-пястные и плюснефаланговые. Значительно реже (в 20 % случаев) РА начинается с олиго- или моноартрита (лучезапястный, коленный, локтевой). По мере течения заболевания больные отмечают постепенное поражение и других суставов. Плечевые и тазобедренные суставы обычно не поражаются, боли в них отмечаются только в поздней стадии РА, спустя много лет после начала болезни. Голеностопный сустав и суставы позвоночника также поражаются в поздней стадии РА. Таким образом, последовательность вовлечения суставов в патологический процесс в типичных случаях можно охарактеризовать как «сверху — вниз». По мере течения РА больные отмечают развитие деформаций пораженных суставов и ограничение в них подвижности, которая в выраженных случаях приводит к полной потере функции сустава. На I этапе можно получить сведения о возможном поражении внутренних органов (появление жалоб соответственно вовлечению в патологический процесс различных органов), а также сведения о ранее проводимом лечении. Лечение препаратами золота или D-пеницилламином указывает на развитую клиническую картину болезни, тогда как эффективность терапии нестероидными противовоспалительными препаратами и аминохинолиновыми производными свидетельствует о небольшом сроке течения, невысокой активности патологического процесса. На II этапе диагностического поиска существенную информацию дает исследование пораженных суставов: в начале заболевания или в пе- риод обострения отмечаются клинические признаки артрита в виде сглаженности контуров сустава за счет воспалительного внутрисуставного отека и отека периартикулярных тканей. Характерно симметричное поражение суставов. По мере развития болезни появляются деформации суставов, обусловленные пролиферативны-ми изменениями синовиальной оболочки и капсулы сустава, а также деструкцией суставного хряща и прилежащей костной ткани. Возникают подвывихи, усугубляющиеся развитием контрактур вследствие поражения сухожилий в местах их прикрепления к костям. Некоторые из деформаций, наиболее типичные для РА, имеют самостоятельные значения: отклонение всей кисти в локтевую сторону — «плавник моржа»; сгибательная контрактура проксимального межфалан-гового сустава при одновременном переразгибании в дистальном межфа-ланговом суставе — деформация пальца типа «пуговичной петли»; укорочение фаланг, сопровождающееся сморщиванием кожи над ними, в сочетании с ульнарной девиацией кисти — деформация кисти типа «рука с лорнетом». Поражение других суставов не отличается от артритов иного происхождения. Изменения суставов кисти при РА являются «визитной карточкой» заболевания. По мере прогрессирования заболевания развивается атрофия кожных покровов, они выглядят блестящими и как бы прозрачными. Наиболее отчетливо изменения кожи выражены в области пальцев и голеней. В некоторых случаях возникает изъязвление кожи голеней, которое может быть связано с васкулитом, обусловливающим формирование локальных некрозов. Иногда при длительном течении РА отмечается эритема в области ладоней. У 20 — 30 % больных встречаются так называемые ревматоидные узелки — безболезненные, достаточно плотные округлые образования диаметром от 2 — 3 мм до 2 — 3 см, локализующиеся обычно в местах, подвергающихся механическому давлению (разгибательная поверхность локтевой кости вблизи локтевого сустава, ахиллово сухожилие, седалищные бугры). Изредка узелки возникают в области мелких суставов кисти или стоп и в стенках синовиальной сумки, находящейся в области венечного отростка локтевой кости. Обычно узлы расположены подкожно, но могут формироваться и внутрикожно и в сухожилиях. Размер узлов с течением времени меняется, в период ремиссии они могут полностью исчезать. Они выявляются лишь у больных с серопозитивным РА. Поражение суставов сопровождается развитием мышечных атрофии. Один из ранних симптомов РА при поражении суставов кисти — атрофия межкостных мышц. При поражении других суставов развивается атрофия мышц, являющихся «моторными» для данного сустава. Со временем мышечная атрофия распространяется не только на расположенные около пораженных суставов мышцы, но и на весь мышечный массив, что ведет к общему истощению. Отмечают также хруст в суставах при активных и пассивных движениях. У больных РА можно обнаружить поражение сухожилий и синовиальных сумок. В синовиальной оболочке сухожильных влагалищ и синовиальных сумок также может развиваться воспаление, сопровождающееся воспалительным выпотом. Наиболее часто отмечается поражение влагалищ сухожилий сгибателей и разгибателей пальцев, характеризующееся болезненностью и припухлостью в области кисти. Пальпаторно выявляет- ся крепитация при движениях. Сгибание пальцев может быть затруднено из-за тендовагинита сухожилий сгибателей. В редких случаях формируются ревматоидные узелки в сухожилиях, что может послужить причиной их разрыва. Аутоиммунный характер болезни с преимущественным поражением суставов и других соединительнотканных элементов обусловливает распространение патологического процесса на внутренние органы. Как следует из рабочей классификации, при РА могут поражаться практически все внутренние органы, однако частота и степень выраженности этих поражений различны. Как правило, поражение внутренних органов протекает субклинически, без выраженных симптомов. Поражение сердца мо
Поиск по сайту: |
 характеристика поражений
характеристика поражений




 пищеварительной системы
пищеварительной системы

 Интерстициальная пневмония, склероз, адгезивный плеврит
Интерстициальная пневмония, склероз, адгезивный плеврит

 II. Атипичные формы: с очаговым поражением кожи, преимущественно висцеральная, суставная, мышечная, сосудистая.
II. Атипичные формы: с очаговым поражением кожи, преимущественно висцеральная, суставная, мышечная, сосудистая.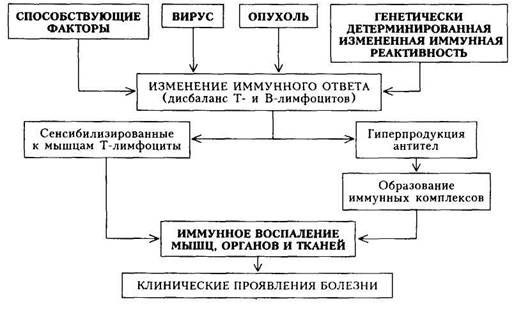
 Глава VIII БОЛЕЗНИ СУСТАВОВ
Глава VIII БОЛЕЗНИ СУСТАВОВ Содержание
Содержание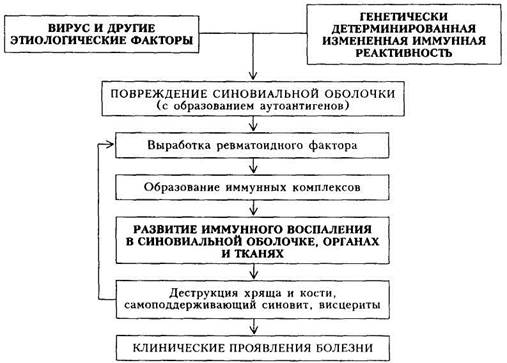
 Клинико-анатомическая характеристика
Клинико-анатомическая характеристика





 I. Ревматоидный артрит:
I. Ревматоидный артрит:
 При постепенном начале заболевания отмечаются медленное нарастание болей и припухлости суставов, движения в суставах ограничены незначительно, температура тела остается нормальной.
При постепенном начале заболевания отмечаются медленное нарастание болей и припухлости суставов, движения в суставах ограничены незначительно, температура тела остается нормальной.