 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Классификация лекарственных средств из группы биогенных стимуляторов. ⇐ ПредыдущаяСтр 6 из 6
I. Хондропротекторы: A. Средства, на основе гликозаминогликан-пептидного комплекса: румалон, глюкозамин; B. Средства, на основе сульфатированных гликозаминогликанов: хондроитин сульфат. II. Собственно биостимуляторы: A. Гидролизаты крови животных: солкосерил, активегин; B. Препараты яда пчел: апизатрон; C. Препараты растительного сырья: эхинацин, мадекассол; D. Производные пелоидов: пелоидин. Хондропротекторы Хондропротекторы – лекарственные средства, которые влияют на обмен матрикса хрящевой ткани суставов путем усиления его синтеза или торможения резорбции. Хрящевая ткань суставов состоит из клеток (хондроцитов, хондробластов) и межклеточного матрикса, который они образуют. Межклеточный матрикс представляет собой гель, построенный на основе биополимеров. В состав геля входят следующие молекулы: · Коллаген – фибриллярный («нитчатый») белок. В настоящее время описано 19 типов коллагена. Основными являются следующие 4 типа: I тип – коллаген плотной соединительной ткани; II тип – коллаген хрящей; III тип – эмбриональный коллаген; IV тип – коллаген базальных мембран эпителия. Хрящевую ткань образуют молекулы коллагена II, VI, IX и XI типов. Коллаген II типа образует фибриллярную основу хрящевой ткани. Коллаген XI типа находится внутри этих фибрилл и регулирует процессы их сборки. Коллаген IX типа – прикрепляется к поверхности фибрилл и формирует как-бы «крючки» для сшивки фибрилл в сеть. Коллаген VI типа образует микрофибриллы, которые перекидываясь от «крючка» к «крючку» сшивают фибриллы коллагена в сеть. · Гликозаминогликаны – линейные отрицательно заряженные гетерополисахариды. Основной представитель гликозаминогликанов – гиалуроновая кислота (несульфатированный гликозаминогликан). Она образует в хряще сеть, накоторую крепятся молекулы протеогликанов. · Протеогликаны (мукополисахариды) – сложные молекулы, которые состоят из 5-10% белка и 90-95% сульфатированных гликозаминогликанов. Основным протеогликаном хряща является агрекан – молекула типа «бутылочного ерша». В центре агрекана лежит нить корового белка, к которой крепятся молекулы хондроитин-сульфата (»100 цепей) и кератан-сульфата (»30 цепей). Всего в хрящевой ткани до 10% агрекана. За счет большого числа сульфатных групп молекула агрекана имеет избыточный отрицательный заряд и окружена толстой гидратной оболочкой. Таким образом, гель матрикса состояит из ячеистой сети фибрилл коллагена. Внутри ячеек сети – цепь гиалуроновой кислоты, на которую посажены агрекановые молекулы – они окружены гидратной оболочкой и удерживают воду в ячейках коллагеновой сети, обеспечивая, тем самым, рессорную функцию хряща (схема 7). При нагрузке на хрящ жидкость вытесняется до тех пор, пока давление набухания не уравновесит внешнюю нагрузку.
Схема 7. Строение и рессорная функция хряща. Слева показан хрящ в начальный момент действия внешней нагрузки. Молекулы гиалуроновой кислоты (ГУК) и агрекана (АК) лежат свободно, промежутки между ними заполнены водой гидратных оболочек. По мере вытеснения воды (справа) возникает противодействующая сила сжатия агрекановых молекул, которая уравновешивает внешнее давление на хрящ. Помимо рассмотренных выше компонентов, хрящевой матрикс содержит также минорные вещества (см. таблицу 11). Процесс обновления матрикса хрящевой ткани протекает с постоянной скоростью, активность же процессов разрушения матрикса может регулироваться за счет балланса активаторов и ингибиторов резорбции хряща, краткая характеристика которых представлена в таблице 12. Румалон (Rumalon) – экстракт хрящевой ткани и красного костного мозга крупного рогатого скота. Действующее начало – гликозаминогликан-пептидный комплекс. Таблица 11. Минорные компоненты хряща и их роль.
Таблица 12. Активаторы и ингибиторы резорбции хряща.
МД: Под влиянием румалона возникают следующие изменения в метаболизме хряща: · Усиливается синтез протеогликанов (агрекана, минорных компонентов хряща); · Подавляется продукция коллагеназ; · Связывается и нейтрализуется IL-1. ФЭ: Под влиянием румалона усиливается синтез хондроцитами и фибробластами хрящевого матрикса, гранудяционной ткани (ткань, которая образуется в процессе заживления ран), замедляется скорость распада хряща. К сожалению, столь впечатляющие эффекты были получены только на культурах клеток. Как показывает клиническая практика хондропротекторный эффект румалона у пациентов значительно скромнее. Применение. Лечение деформирующего остеоартроза. Под влиянием румалона удается снизить потребность пациента в нестероидных противовоспалительных средствах и кортикостероидах (которые также используют при лечении остеоартроза). Эффект развивается только через 2-3 недели регулярного применения. Режим дозирования: Румалон вводят глубоко внутримышечно в первый день 0,3 мл, во второй – 0,5 мл, затем по 1 мл 3 раза в неделю в течение 5-6 недель. НЭ: В целом румалон хорошо переносится пациентами. Однако, из-за содержания антигенных белков он часто вызывает серъезные аллергические реакции, поэтому в настоящее время практически не применяется. ФВ: ампулы по 1 мл. Глюкозамин (Glucosamine, Dona) Является аминосахаром, который входит в состав гликозминогликанов соединительной ткани и суставного хряща.
· Глюкозамин подавляет активность коллагеназ, разрушающих матрикс хряща. · Глюкозамин-сульфаты стимулируют синтез хондроитин-сульфата, кератан-сульфата хрящевой ткани. ФЭ: · Оказывает хондропротективный эффект. Глюкозамин стимулирует синтез хрящевого матрикса, фиксацию сульфатов и воды в нем. В итоге, под влиянием глюкозамина увеличивается гидратация хряща и оптимизируется его рессорная функция. Глюкозамин тормозит распад хрящевой ткани, ингибирует фосфолипазу А2 и подавляет генерацию в хряще провоспалительных цитокинов (лейкотриенов, простагландинов Е2, F2a). · Антиоксидантный эффект. Глюкозамин связывает и нейтрализует супероксидный радикал, подавляет ферменты нейтрофилов, которые обеспечивают генерацию этого радикала. · Усиливает минерализацию костной ткани. Применение. Лечение деформирующего остеоартроза. Эффект глюкозамина развивается только через 2 недели регулярного применения, но сохраняется до 8 недель после окончания курса лечения. На фоне глюкозамина у пациентов удается снизить дозы глюкокортикостероидов и нестероидных противовоспалительных средств. Режим дозирования. Наилучшим считается сочетанное внутримышечное и пероральное применение глюкозамина. Внутрь глюкозамин применяют по 1,5 г/сут, растворив содержимое пакетика в 200 мл воды. Рекомендуется проводить прием лекарства перед едой. Внутримышечно вводят по 400 мг 3 раза в неделю. Перед применением содержимое ампул (2 мл) растворяют в 1 мл прилагаемого растворителя. Курс лечения 4-6 недель, при необходимости его повторяют через 2 месяца. НЭ: Осложнения при лечении глюкозамином возникают достаточно редко. Возможно развитие бродильной диспепсии (мемеоризм, диарея, борборигмы). Следует помнить, что в состав растворителя глюкозамина для внутримышечного введения входит лидокаин и его нельзя применять у пациентов с непереносимостью лидокаина. ФВ: порошок по 1,5 г в пакетиках; раствор 20% в ампулах по 2 мл. Хондроитин-сульфат (Chondroitine sulfat, Structum) Это высокомолекулярный гликозаминогликан (хондроитин-4-сульфат), который в большом количестве находится в составе матрикса хрящевой ткани.
ФЭ: Подобно гликозаминогликану оказывает хондропротективное действие, однако, основной акцент смещен не в сторону образования, а в сторону подавления резорбции хряща. Обладает слабым противовоспалительным и анальгетическим действием. Применение. Хондроитин-сульфат применяют для лечения деформирующего остеоартроза. Назначают его внутрь в первые 3 недели по 750 мг 2 раза в день, затем по 500 мг 2 раза в день. Курс лечения 5-6 недель. На фоне лечения удается снизить потребность больного в кортикостероидах. НЭ: В редких случаях хондроитина-сульфат может вызвать аллергические реакции. ФВ: капсулы по 250 и 500 мг. Собственно биостимуляторы Солкосерил (Solcoseryl) Представляет собой неантигенный апирогенный депротеинизированный диализат из крови молочных телят. ФЭ: 1. Стимулирует метаболизм в тканях и оказывает антигипоксическое действие: стимулирует транспорт глюкозы в клетку, повышает синтез АТФ (за счет активации глюкозных транспортеров GLUT и активации пируватдекарбоксилазного комплекса). 2. Ускоряет регенерацию посврежденных клеток и тканей. 3. Стимулирует ангиогенез. Применение. До настоящего времени нет убедительных доказательств высокой эффективности солкосерила. Многоцентровых плацебо-контролируемых исследований посвященных изучению егодействия и эффективности не проводилось. В настоящее время есть отдельные публикации с сообщениями о положительном клиническом эффекте препарата, поэтому показания для его применения основываются только на эмпирических данных: · Лечение трофических язв, пролежней, свищей – используют местные аппликации; · Лечение длительно незаживающих язв при язвенной болезни желудка и двенадцатиперстной кишки; · Реабилитация после перенесенного острого нарушения мозгового кровообращения, черепно-мозговой травмы; · Лечение язв роговицы, механических или химических травм глаза, конъюнктивитов; · Лечение пародонтоза, гингивита, афтозного стоматита и др. воспалительных поражений полости рта. Режим дозирования. Местно применяют в виде мази, геля, желе, которые наносят тонким слоем на пораженную поверхность 2-4 раза в день. Парентерально вводят внутривенно медленно по 5-20 мл 1 раз в сутки в течение 4-5 недель. Допустимо капельное введение 250-500 мл/сут ежедневно, на курс 10-14 инъекций. Скорость введения 20-40 капель/мин. НЭ: Возможны аллергические реакции, при местном применении – небольшое жжение. ФВ: ампулы по 2, 5, 10 мл; флаконы 250 мл; гель, мазь и желе в тубах по 20,0; гель глазной по 5,0. Актовегин (Actovegin) Является весьма близким к солкосерилу по механизму действия и эффектам лекарством. Содержит депротеинизированный гемодериват крови телят, представляющий собой смесь низкомолекулярных пептидов (Mr<5.000 Да), нуклеиновых кислот, олигосахаридов, гликолипидов. В отличие от солкосерила содержит некоторые ферменты (»70ЕД/мл супероксиддисмутазы), поэтому антигипоксическое действие актовегина дополняется выраженным антиоксидантным эффектом. Применяется по тем же показаниям, что и солкосерил. Режим дозирования: · Внутрь по 200-400 мг 3 раза в день перед едой; · Внутривенно медленно 5-20 мл или медленно капельно 250 мл раствора со скоростью 2-3 мл/мин. Всего на курс 10-20 инъекций. · Местно наносят тонким слоем 1 раз в день на пораженные участки. Следует помнить, что актовегин имеет лучшую доказательную базу, чем солкосерил. Его эффективность была изучена в нескольких рандомизированных клинических испытаниях, где был показан эффект актовегина. Однако, эти исследования имели погрешности в проведении конечного этапа анализа, поэтому к оценке их результатов следует подходить весьма осторожно. Во многих странах в настоящее время применение солкосерила и актовегина прекращено в связи с потенциальной угрозой заражения пациентов прионной инфекцией (губчатым подострым энцефалитом коров). ФВ: драже форте по 200 мг; раствор 4% в мапулах по 2, 5 и 10 мл, 10% и 20% во флаконах по 250 мл для инъекционного введения; крем, мазь 5% в тубах по 20,0; гель 20% в тубах по 20,0; гель глазной 20% в тубах по 5,0. Апизартрон (Apisarthron) Содержит смесь стандартизированного яда пчел (апитоксина), метилсалицилата (нестероидного противосовпалительного средства) и действующего начала горчичного эфирного масла – аллилизотиоцианата. МД и ФЭ: · Апитоксин содержит гистамин, органические кислоты, холин, триптофан и сумму ферментов (гиалуронидазу, фосфолипазу А). Все эти вещества способствуют расширению сосудов, повышению их проницаемости и облегчают миграцию клеток иммунной системы в очаг воспаления. · Метилсалицилат оказывает слабое противовоспалительное и анальгетическое действие за счет подавления синтеза провоспалительных простагландинов в очаге воспаления. · Аллилизотиоцианат – раздражает NK-рецепторы тахикининов чувствиетльных (афферентных) нервных волокон и включает вегетативно-трофические рефлексы, которые обеспечивают усиление кровотока, выделение биологически активных веществ в очаге повреждения. Применение и режим дозирования. Симптоматическое лечение воспалительных и травматических повреждений мышц (миалгии, миозиты), суставов (артралгии, артриты), нервных стволов (невриты, невралгии, ишиас, люмбаго). Полоску мази длиной 3-5 см распределяют в проекции пораженной области слоем толщиной 1 мм и оставляют на несколько минут (в среднем на 2-3 мин) до появления гиперемии и ощущения тепла. После этого мазь медленно втирают в кожу. Применяют 2-3 раза в сутки. НЭ: Аллергические реакции, обусловленные наличием чужеродного белка в апитоксине. ФВ: мазь по 20,0; 50,0 и 100,0. Эхинацин (Echinacin liquidum, Extr. Echinaceae) Представляет собой смесь 80 мл свежего сока Echinacea purpurea, полученного прессованием и 22 об% этилового спирта на каждые 100 г препарата.
· Производные кафеиновой кислоты – эхинакозид, цикориевая, кофеатная, каффаровая, хлорогеновая кислоты; · Полисахариды: инулин, фруктаны, фукогалактоксилоглюкан, гетероксилан, арабинорамногалактон; · Липофильные компоненты: полиины эфирных масел – эхиналон, 1-пентадецен; алкиламиды ненасыщенных кислот – эхинацеин, изобутиламиды тетраеновой и додекатетраеновой кислот. Наиболее вероятными действующими началами эхинацеи являются цикориевая кислота, алкиламиды ненасыщенных кислот и полисахариды. Однако, поскольку нет точных данных о конкретном действующем начале, препараты эхинацеи в настоящее время не подвергаются биологической стандартизации. МД и ФЭ: 1. Иммуномодулирующая активность. В настоящее время имеются весьма противоречивые данные относительно иммуномодулирующей активности эхинацеи. В настоящее время мета-анализ 26 клинических испытаний эхинацеи, проведенных в 1990-1997 гг позволил четко показать, что иммуномодулирующий эффект эхинацеи в условиях целого организма заключается исключительно в повышении неспецифической активности противоинфекционного иммунитета. Экстракт эхинацеи способствует миграции фагоцитов в очаг поражения, стимулирует фагоцитоз, продукцию активных форм кислорода, которые разрушают антиген. Основным веществом, с которым связана эта форма активности является липидная липидная фракция препарата (эхинацеин, эхинолон) и цикориевая кислота. В опытах in vitro, на культурах клеток было установлено, что полисахаридные фракции эхинацеи (кислый арабиногалактон, разветвленные гетерогликаны с Mr до 5.000 Да) немсомненно повышают активность моноцитов – уисливают продукцию IL-1,6,10, ФНОa и INFb. Однако, в экспериментах на добровольцах этого обнаружено не было. Полагают, что причины данного феномена заключаются в следующем: º Полисахариды содержатся в больших количествах в корневищах и корнях эхинацеи. Надземная часть растения (из которой получают сок) бедна ими. º Если препарат эхинацеи содержит более 50 об% этанола полисахариды подвергаются преципитации и лишаются фармакологической активности (т.е. наиболее богаты полисахаридами сухие препараты эхинацеи, полученные из корней растения). º При пероральном введении 99% полисахаридов разрушается микрофлорой кисшечника и их биодоступность составляет менее 1%. Чтобы обеспечить поступление фармакологически значимого количества полисахаридов в организм человека требуется ежесутосное введение порядка 600 мл свежего сока корней эхинацеи. 2. Противовоспалительное действие. Полагают, что это связано с наличием алкиламидов ненасыщенных кислот (эхинациена, изобутиламидов докозатетраеновой кислоты), которые угнетают активность циклооксигеназы и 5-липоксигеназы в результате чего снижентся синтез медиаторов воспаления (простагландинов и лейкотриенов). Кроме того, было показано, что производные кофейной кислоты – цикориевая, каффаровая и хлорогеновая кислоты способны блокировать активность гиалуронидазы и уменьшать тем самым сосудистую проницаемость в очаге воспаления. По некоторым данным по противосовпалительной активности 0,04 мл экстракта эхинацеи эквивалентны 1 мг кортизона. Как следует из представленных данных – ни один из фармакологических эффектов эхинацеи не связан с наличием эхинакозида. В настоящее время четко установлено, что эхинакозид не отвечает за иммуномодулирующее или противовоспалительное действие. Он оболадает лишь крайне слабой бактериостатической активностью в отношении E. coli и S. aureus. Его эффект в количестве 6 мг сопоставим с эффектом 1ЕД пенициллина. Следовательно, для получения клинически значимого антибактериального действия человек должен потреблять в сутки более 0,5 кг эхинакозида. К сожалению, ряд производителей в рекламных целях указывают, что их препараты эхинацеи стандартизированы по содержанию эхинакозида. Как следует из всего вышесказанного данный метод стандартизации ничего не говорит о реальном содержании действующих веществ в препарате. Показания к применению: 1. Лечение простудных заболеваний в составе комплексной терапии. По данным ряда авторов применение эхинацеи на 25-30% ослабляет выраженность и длительность симптомов заболевания. 2. Профилактика рецидивов хронических бронхолегочных заболеваний (хронический бронхит), хронического тонзиллита, пиелонефрита. Поскольку данные об иммуномодулирующем действии эхинацеи неоднозначны не рекомендуется назначать ее лицам с ВИЧ-инфекцией, аутоиммунными заболеваниями (ревматоидным артритом), туберкулезом, пациентам с трансплантированными органами. Режим дозирования: Применяют по 6-9 мл/сут разделенных на 3-5 приемов. При простуде рекомендуется прием в первый день 40 кап (2 мл), затем по 20 капель каждые 1-2 часа до общей дозы в 9 мл. Затем применяют по 2 мл 3 раза в день. Курс терапии эхинацеей не должен превышать 8 недель. В настоящее время показано, что ее прием более длительный срок приводит к постепенному развитию толерантности к лекарству. НЭ: Возможны аллергические реакции, особенно у лиц, сенсибилизированных к подсолнечнику. Иногда отмечается неприятный вкус во рту, отрыжка, поташнивание. У лиц, применяющих алкоголь-содержащие напитки одновременно с препаратами эхинацеи возможно возникновение тетурамоподобной реакции. ФВ: флаконы по 50 мл. Пелоидин (Peloidinum) Экстракт иловой грязи, содержащий БАВ, образованные отмершей микрофлорой. Полагают, что вещества, содержашщиеся в пелоидине стимулируют митотическую активность клеток. Объективных доказательств высокой эффективности пелоидина не получено. Применение и режим дозирования. Для ускорения заживления язвенного дефекта при язвенной болезни двенадцатиперстной кисшки и желудка применяют внутрь по 40-50 мл 2 раза в день натощак. Курс лечения 4-6 недель. При лечении колитов применяют в виде микроклизм по 100 мл 2 раза в день. Курс лечения 10-15 дней. Лечение гнойных ран. Применяют наружно в виде повязок. НЭ: Не описаны. ФВ: бутылки по 500 мл. Мадекассол (Madecassole) Средство на основе Centella asiatica – растения, произрастающего в Индии, Иране, Пакистане, Шри-Ланке. Содержит тритерпеновые эфиры гликозидов азиатикозид и мадекассикозид. МД и ФЭ: [ [ Воздействует на стволовые эпидермальные клетки и оптимизирует процесс их размножения икератинизации. [ Стимулирует синтез протеогликанов и гликозаминогликанов в соединительной ткани, повышая ее гидратацию. [ Повышает элластичность кожи, за счет воздействия на миофибробласты. Показания к применению: 1. Лечение кожных ран, язв и ожогов (включая ожоги II-III степени). Профилактика развития келоидных рубцов. Показано, что за счет улучшения процессов созревания коллагена мадекассол предупреждает формирование уродующих келоидных рубцов и шрамов. 2. Лечение стрессовых язв желудка. 3. Лечение язвенных поражений кожи при лепре (проказе). 4. Лечение кожных проявлений склеродермии. Склеродермия – одно из ревматических заболеваний, для которого характерна гиперпродукция незрелого коллагена в дерме, приводящая к возникновению уплотнения кожи в виде «панциря», развитию вазоспазма. Мадекассол за счет увеличения синтеза протеогликанов, созревания коллагена и воздействия на миофибробласты повышает элластичность дермы и замедляет формирование «панцирных рубцов». Режим дозирования: Применяют внутрь по 20 мг 3 раза в день или внутримышечно по 20 мг 2-3 раза в неделю. Крем наносят в виде местных аппликаций на пораженные участки ежедневно. НЭ: При местном применении возможно раздражение кожи. У животных при длительном системном применении азиатикозид увеличивал риск развития карциномы кожи. ФВ: таблетки по 10 мг, крем 1% в тубах по 10,0. ЛИТЕРАТУРА 1. Ацетил-L-карнитин: биологические свойства и клиническое применение (обзор) / Е.В. Ефимова, Т.А. Гуськова, В.М. Копелевич, В.И. Гунар // Хим. Фарм. Журнал – 2002. – т. 36, №3. 2. Белоусов Ю.Б., Моисеев В.С., Лепахин В.К. Клиническая фармакология и фармакотерапия. Рук-во для врачей. 2-е изд. – М.: Универсум Паблишинг, 2000. – 539 с. 3. Биохимия: Учебник / Под ред. Е.С. Северина. – М.: ГЭОТАР МЕД, 2003. – 784 с. 4. Бороян Р.Г. Клиническая фармакология: психиатрия, неврология, эдокринология, ревматология. – М.: МИА, 2000. – 422 с. 5. Грэхам-Смит Д.Г., Аронсон Дж.К. Оксфордский справочник по клинической фармакологии и фармакотерапии. Пер с англ. – М.: Медицина, 2000. – 514 с. 6. Использование препарата Элькар (L-карнитин) в педиатрии / Е.С. Кешишян, Л.З. Казанцева, Е.А. Николаева, Е.В. Тозлиян // Terra Medica – 2001. – №4. – С. 42-43. 7. Катцунг Б.Г. Базисная и клиническая фармакология: в 2-х т. Пер с англ. – М.–СПб.: Бином – Невский Диалект, 1998. – Т.1 – 612 с., Т.2 – 670 с. 8. Кукес В.Г. Клиническая фармакология: Учебник. – М.: ГЭОТАР МЕДИЦИНА, 1999. – 528 с. 9. Маркова И.В., Неженцев М.В. Фармакология. Учебник для студентов педиатрических факультетов медицинских институтов. – СПб.: Сотис, 1994. – 455 с. 10. Михайлов И.Б. Настольная книга врача по клинической фармакологии. Рук-во для врачей. – СПб.: Фолиант, 2001. – 736 с. 11. Нил М.Дж. Наглядная фармакология. Пер с англ. / Под ред. М.А. Демидовой. – М.: ГЭОТАР МЕДИЦИНА, 1999. – 104 с. 12. Регистр лекарственных средств России. Энциклопедия лекарств. Выпуск 10. – М.: ООО «РЛС-2003», 2003. – 1438 с. 13. Сатоскар Р.С., Бандаркар С.Д. Фармакология и фармакотерапия: в 2-х т. Пер с англ. – М.: Медицина, 1986. – Т.1 – 528 с., Т.2 – 432 с. 14. Справочник Видаль. Лекарственные препараты в России: Справочник. – М.: АстраФармСервис, 2003. – 1488 с. 15. Фармакотерапия. Клиническая фармакология. Пер с нем. / Под ред. Г. Фюльграффа, Д. Пальма. – Мн.: Беларусь, 1996. – 689 с. 16. Харкевич Д.А. Фармакология: Учебник. – 7-е изд., перераб. и доп. – М.: ГЭОТАР МЕД, 2002. – 728 с. 17. Goodman & Gilman’s: The Pharmacologycal Basis of Therapeutics. 10th ed. / Ed. J.G. Hardman, L.E. Limbird. – McGraw-Hill, 2001. – 2148 p. 18. Bone K. Echinacea: What Makes It Work // Alt. Med. Rev. – 1997. – Vol.2, №2. – P. 87-93. 19. Integrated Pharmacology. 2nd ed. / C. Page, M. Curtis, M Sutter et al. – Mosby International Ltd., 2002. – 671 p. 20. Mycek M.J., Harvey R.A., Champe P.C. Lippincott’s Illustrated Reviews: Pharmacology. 2nd ed. – J.B. Lippincott Co – Williams & Wilkins, 2000. – 514 p. 21. Modern nutrition in health and disease 8th / Ed. M.E. Shils, J.A. Olson, M. Shike – Williams & Wilkins, 1994. – 1636 p. 22. Pharmacology. Lippincott’s Review Series / Ed. C. Paradiso. – J.B. Lippincott Co, 1998. – 636 p. 23. Stoelting R.K. Pharmacology & Physiology in Anestethetic Practice. 2nd ed. – J.B. Lippincott Co, 1991. – 872 p. 24. Tripathi K.D. Essentials of Medical Pharmacology. 3rd ed. – Jaypee Brothers Medical Publishers Ltd, 1995. – 846 p. 25. Zubay G. Biochemistry: 3rd ed. – Wm. C. Brown Publishers, 1993. – 1024 p.
[1] Подробнее о классификации поливитаминных средств и определении понятий, используемых для этой группы лекарств будет рассказано в соответствующем разделе. [2] О витаминах ВС и В12 будет рассказано в разделе, посвященном средствам, влияющим на кроветворение. [3] То есть исследование в котором ни пациент, ни врач до окончания эксперимента не знали, какое лекарство принимал пациент – аскорбиновую кислоту или плацебо. [4] Настоящее определение дано «Санитарными нормами и правилами по определению безопасности и эффективности биологически активных добавок», Российская Федерация, 1999 г. [5] Интересно отметить, что поскольку гидролиз креатинфосфата может протекать со скоростью в 2 раза большей, чем имеется у современных спринтеров, показатели мирового рекорда по бегу на короткие дистанции теоретически могут быть улучшены почти в 2 раза.
Поиск по сайту: |

 МД: В организме часть молеукл сульфатируется в 4-ом или 6-ом положении. Активностью обладает как сам глюкозамин, так и его сульфатированные метаболиты.
МД: В организме часть молеукл сульфатируется в 4-ом или 6-ом положении. Активностью обладает как сам глюкозамин, так и его сульфатированные метаболиты.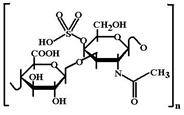 МД: Хондроитин-сульфат участвует в построении агрекана – основного протеогликана матрикса суставного хряща. Под влиянием хондроитин-сульфата увеличивается образование ингибиторов деструкции хряща – ингибиторов металлопротеиназ, TGFb.
МД: Хондроитин-сульфат участвует в построении агрекана – основного протеогликана матрикса суставного хряща. Под влиянием хондроитин-сульфата увеличивается образование ингибиторов деструкции хряща – ингибиторов металлопротеиназ, TGFb. В состав сока эхинацеи входят:
В состав сока эхинацеи входят: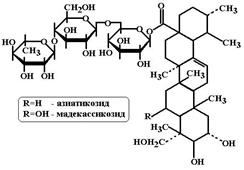 Стимулирует синтез и созревание коллагена I типа у человека. Обеспечивает быстрое заживление раневых дефектов.
Стимулирует синтез и созревание коллагена I типа у человека. Обеспечивает быстрое заживление раневых дефектов.