 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Tau - Trp - 5-HT -5_HT 5-HT 5-HIAA
Рис. 23. Изменения содержания свободных аминокислот, биогенных аминов, их предшественников и метаболитов, коэффициенты корреляции между их уровнями в отделах головного мозга крыс в динамике ежедневного в/бр введения таурина в дозе 1/10 LD5o 109 3.3.2. Субконъюнктивальное введение таурина Сравнительно низкая проницаемость гематоэнцефалического барьера для таурина затрудняет воспроизведение его нейрохимических эффектов при периферических способах введения. Особенности кровоснабжения и проницаемости гематоэнцефалического барьера для гипоталамуса позволяют предполагать реализацию возможных нейрохимических эффектов таурина при субконъюнктивальном способе его введения и, возможно, приравнять его к центральным. В связи с тем, что для таурина не доказано наличие иных метаболических превращений, кроме конъюгации с желчными кислотами, мы исходили из предположения, что весь определяемый нами счет метки относится к таурину. Результаты эксперимента по исследованию закономерностей распределения меченого 14С-таурина при его субконъюнктивальном введении животным свидетельствуют о наличии накопления метки в ткани гипоталамуса с максимумом через 6 ч после введения препарата (рис.24) и одновременным снижением уровня метки в плазме крови животных (рис 25). На этом фоне кривая накопления 14С-таурина в целом мозге (рис.26) имеет вид, сходный с таковой для гипоталамуса, однако в мозге отмечается рост счёта метки вплоть до 5 сут эксперимента. Одновременно, кривая, отражающая закономерности накопления 14С-таурина для плазмы крови (рис.25) соответствует классической кривой элиминации, за исключением падения счета через 2 ч, после чего вновь наблюдалось увеличение счета (3 и 6 ч). На основе полученных данных можно предположить существование процессов пассивной диффузии и активного транспорта таурина в гипоталамус при его субконъюнктивальном введении. Указанные процессы определяются особенностями кровоснабжения этого отдела, на что указывает высокий уровень накопления меченого 14С-таурина в гипоталамусе уже через 30 мин после введения метки (рис.24). Очевидно, что в дальнейшем (1-120 ч) таурин проникает в мозг только путём активного транспорта, что подтверждается характером элиминации метки из крови: наиболее интенсивное накопление метки в гипоталамусе (6 ч) по времени совпадает с резким снижением счёта в плазме крови, где эта кривая явно отклоняется от обычной экспоненциальной формы (рис.25). по
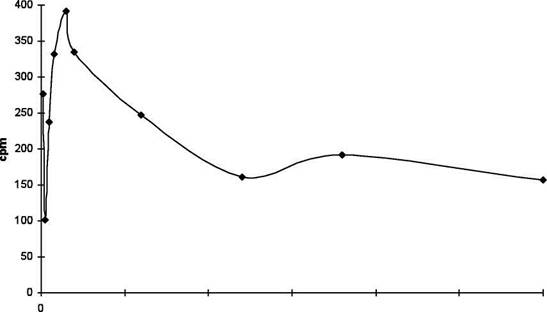
Рис. 24. Накопление метки в ткани гипоталамуса после однократного субконъюнктивального введения 30 |0,Ci 14С-таурина 9000 т
Рис. 25. Счет метки в плазме крови крыс через различные сроки после однократного субконъюнктивального введения 30ц.Ci 14С-Таурина. 2500 х 2000 ■ • 1500 ■ • 1000 ■ • 500 ■•
■г Рис. 26. Накопление метки в целом мозге крыс после однократного субконъюнктивального введения 30|xCi 14С-Таурина Из полученных нами данных очевидно, что мозг имеет более чем одну систему активного транспорта таурина: с более низким сродством была активной и явно превалировала в гипоталамусе в ранние сроки (3 ч) от введения 14С-таурина, т.е. на фоне высокой концентрации метки в системном кровотоке; другая, очевидно, была ответственной за поздний (до 120 ч) подъём кривой в целом мозге и, таким образом, может быть преимущественно представлена в других структурах ЦНС. Кроме этого, в гипоталамусе имеется также пассивная диффузия таурина, чем объясняется проникновение метки в первые минуты после введения. В то же время, в гипоталамусе вплоть до конца эксперимента счёт метки оставался стабильно высоким с тенденцией к наличию второго максимума накопления — к 3 сут после введения. Кинетические константы для таурина, рассчитанные из данных настоящего эксперимента, составили: а) в гипоталамусе: константа элиминации 0,01016 ± 0,00552 мин'1 период полувыведения Т1/2 68,22 мин константа скорости всасывания Kt 0,72122 ± 0,37076 среднее время всасывания 1,38 мин период полувсасывания 0,96 мин максимальная концентрация 3,32 (ерш* 1000) б) в плазме крови: период полувыведения TV213,88 час константа элиминации 0,05 ± 0,026 мин'1 Таким образом, данные настоящего эксперимента подтверждают, что таурин является относительно долгоживущим соединением в ЦНС, и свидетельствуют, что: 1) субконъюнктивальное введение таурина позволяет получить его 2) мозг располагает как минимум двумя системами активного 3) эффекты таурина при его субконъюнктивальном введении могут Одновременно, субконъюнктивальное введение Таи в течение 15 суток в суммарной дозе 650 мг/кг (1/10 LD5o) приводило в сроке 3 сут к повышению содержания Тгр во всех отделах мозга; |3-А1а — в стриатуме и гипоталамусе; GABA — в гипоталамусе. Содержание возбуждающих трансмиттеров Asp и Glu увеличивалось на 1 сутки опыта в стволе мозга и уменьшалось в стриатуме на 3 сутки, в сроках опыта 8 и 15 сут изменений в определяемых показателях не зарегистрировано (рис.27). Во все сроки опыта, кроме 15 сут, в стволе мозга наблюдалась достоверная положительная корреляция Таи - J3-Ala в опытных группах и ее отсутствие (или отрицательная корреляция на 8 сут) в контроле. В стриатуме такая же картина наблюдалась к 15 сут опыта (рис.27). В стволе мозга на сроках 1 и 3 сут после введения Таи появлялась положительная корреляция Таи - Asp; кроме того, в сроках 3 и 8 сут — положительные корреляции между уровнями Таи, с одной стороны, и DA и его метаболитов — DOPAC и HVA, с другой. В гипоталамусе наблюдалось появление положительной корреляции Таи - Gly в сроках 1, 3 и 8 сут, а также исчезновение Таи - GABA — в сроках 1 и 3 сут (рис.27). Таким образом, субконъюнктивальное введение Таи приводит к дисбалансу в содержании тормозных и возбуждающих аминокислот-трансмитторов в среднем мозге и гипоталамусе и, в меньшей степени, в стриатуме. Кроме этого, субконъюнктивальное введение Таи приводит к повышению в отделах мозга Тгр в коротких сроках эксперимента. Отсутствие повышения содержания Таи в отделах мозга в определенной мере может объясняться появлением положительной корреляции между его уровнями и уровнем его транспортного антагониста, р*-А1а, зарегистрированной в стволе мозга.
Рис.27 Изменения содержания свободных аминокислот, биогенных аминов, их предшественников и метаболитов в отделах головного мозга крыс в динамике субконъюнктивального введения таурина в суммарной дозе 1/10 LD50 ГЛАВА 4. КЛИНИЧЕСКИЕ АСПЕКТЫ ПРИМЕНЕНИЯ ТАУРИНА Результаты и перспективы использования Таи и его аналогов в клинической практике, отражающие современное состояние проблемы, изложены в главе 2. В предлагаемом разделе представлены результаты I и II стадий клинических испытаний Таи в качестве радио- и гепатопротекторного средства по соответствующим конкретным показаниям к проведены в специализированных клиниках и отделениях г.Гродно, Витебска и Минска, в процессе реализации которых создан и зарегистрирован новый эффективный отечественный лекарственный препапрат "таблетки таурина". Клинические испытания на I стадии в рандомизированных исследованиях проведены нами в клинике инфекционных болезней ГГМИ на 10 практически здоровых волонтёрах (студенты 6 курса ГГМИ, средний возраст —22г, 1таб. X 3 раза в день, на протяжении 7 дней) с соблюдением всех этических и юридических правил. В процессе исследования, кроме субъективных признаков и объективного статуса добровольцев, в крови из локтевой вены до и после курса Таи определялись маркерные для печени клинико-биохимические показатели, а также пул свободных аминокислот и их дериватов. Испытания препарата на волонтёрах не выявили никаких побочных эффектов препарата (таб.25). Кроме того, его применение сопровождалось обогащением пула серусодержащих аминокислот (таб. 26), что может свидетельствовать об активации их синтеза и превращений и подтверждает обоснованные ранее антиоксидантные, радио- и гепатопротекторные свойства Таи. II стадия клинических испытаний препарата (1 таблетка 3 раза в день в течение 3-х недель) в рандомизированных исследованиях проведена: • в клинике инфекционных болезней у 21 больного острым вирусным • в педиатрической клинике в комплексном лечении у 100 больных детей • в клинике онкологии у 25 больных раком желудка П-Ш стадии; • в клинике лучевой диагностики и лучевой терапии у 30 больных • в хирургической клинике на фоне лечения облитерирующего 115 атеросклероза сосудов нижних конечностей (30 больных); Результаты применения препарата у больных вирусным гепатитом А в желтушный период представлены в таблице 27. На фоне применения таблеток таурина у данной категории больных по сравнению с группой контроля, получавшей традиционное базисное лечение быстрее происходит улучшение общего состояния и уменьшение интоксикации в острую фазу болезни по сравнению с контрольной группой: общее состояние больных в испытуемой группе улучшалось раньше на 1-2 дня, исчезновение желтухи и длительность желтушного периода сокращалась на 2 дня, чем в контрольной группе. Таблица 25 Клинико-биохимические показатели волонтёров до- и после курсового назначения таурина (0,5x3 — 7 дней)
- р<0,05 при сравнении с группой до приёма Таи Таблица 26 Свободные аминокислоты и их производные (|ХМ) в плазме крови волонтёров до- и после курсового назначения таурина (0,5 хЗ — 7 дней)
- р<0,05 при сравнении с группой до приёма Таурина Таблица 27 Сравнительная характеристика клинико-лабораторных показателей при лечении препаратом "таблетки таурина" больных вирусным гепатитом А в желтушный период.
Показатели
Поиск по сайту: |

 20
20 20
20
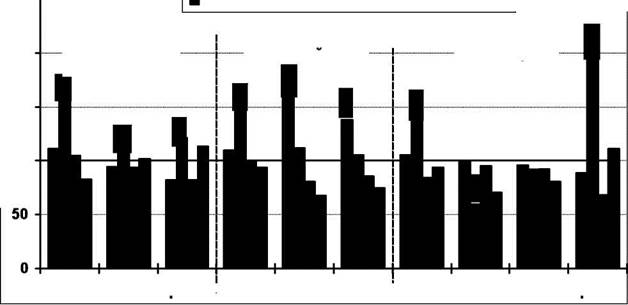 1 сутки ■ 3 суток ■ 8 суток ■ 15 суток
1 сутки ■ 3 суток ■ 8 суток ■ 15 суток