|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Сопряжения и разобщения окислительного фосфорилирования
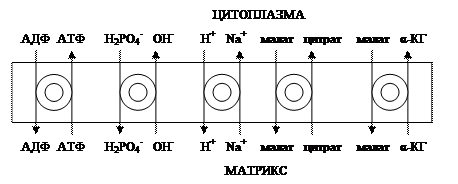
Так как необходимый для сопряжения электрохимический потенциал создают I, III и IV комплексы дыхательной цепи, их называют пунктами сопряжения окисления и фосфорилирования. Повреждение внутренней мембраны митохондрий или увеличение ее проницаемости под действием разобщителей вызывает исчезновение электрохимического потенциала, разобщение процессов окисления и фосфорилирования, и прекращение синтеза АТФ.Разобщение дыхания и фосфорилирования называют явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ. Разобщителями являются вещества, которые могут переносить протоны (протонофоры) или другие ионы (ионофоры) через мембрану минуя каналы АТФ-синтетазы. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О2, окисления НАДН2, ФАДН2, а образовавшаяся свободная энергия выделяется в виде теплоты. Как правило, разобщители — липофильные вещества, легко проходящие через мембраны. Например, вещество 2,4-динитрофенол (переносит Н+), лекарство - дикумарол, метаболит - билирубин, гормон щитовидной железы - тироксин, антибиотики - валиномицин и грамицидин. Коэффициент окислительного фосфорилированияДля оценки эффективности окислительного фосфорилирования используют коэффициент окислительного фосфорилирования (Р/О).Коэффициентом окислительного фосфорилирования называют отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания. При окисление молекулы НАДН2, е- по дыхательной цепи проходят 3 пункта сопряжения, что обеспечивает синтез 3 АТФ при затрате 3 Н3РО4 и 3 АДФ на 1 атом кислорода. Соответственно для НАДН2 Р/О=3. При окисление молекулы ФАДН2, е- по дыхательной цепи проходят только 2 пункта сопряжения, что обеспечивает синтез 2 АТФ при затрате 2 Н3РО4 и 2 АДФ на 1 атом кислорода. Соответственно для ФАДН2 Р/О=2. Эти величины Р/О отражают теоретический максимум синтеза АТФ, фактически эта величина меньше из-за затрат на транспорт. Транспорт веществ через мембрану митохондрий 1). Внутренняя мембрана митохондрии проницаема для незаряженных простых молекул О2, Н2О, СО2, NH3, а также для монокарбоновых кислот. Эти вещества проходят мембрану самостоятельно по градиенту концентраций. 2). Для ионов мембрана не проницаема, через мембрану их переносят специальные насосы за счет энергии электрохимического потенциала. Только на транспорт АТФ и АДФ расходуется около четверти всей энергии электрохимического потенциала. Симпортом с Н+ в матрикс перемещается ПВК и Са2+. Антипортом перемещаются:
В результате обменных механизмов антипорта поддерживается осмотическое равновесие. Теплопродукция 30-35% свободной энергии рассеивается в виде теплоты и используется теплокровными животными на поддержание температуры тела. Кроме того, дополнительное образование теплоты может происходить при paзобщении дыхания и фосфорилирования в бурой жировой ткани. Она содержит много митохондрий с большим количеством дыхательных ферментов и разобщающего белка термогенина (РБ-1, около 10% всех белков). Разобщение окислительного фосфорилирования в бурой жировой ткани позволяет генерировать тепло для поддержания температуры тела у новорождённых, зимнеспящих животных и у всех млекопитающих в процессе адаптации к холоду. У взрослых людей важную роль в термогенезе при переохлаждении играют жирные кислоты. Охлаждение стимулирует выделение норадреналина, который активирует липазу в жировой ткани и гидролиз ТГ. Образующиеся свободные жирные кислоты способны не только быть топливом дыхательной цепи, но и переносить протоны через мембрану в матрикс митохондрий разобщая дыхание и фосфорилирование. Обратно жирные кислоты в ионизированной форме возвращаются с помощью переносчиков. Дыхательный контроль В норме субстраты тканевого дыхания и О2 находятся в достаточном количестве и не лимитируют окислительное фосфорилирование. Активность окислительного фосфорилирования ограничивает только концентрация АДФ, которая обратно пропорциональна концентрации АТФ. При нагрузке концентрация АТФ снижается, а АДФ увеличивается, что ускоряет дыхание и фосфорилирование. В состоянии покоя количество АТФ увеличивается, а АДФ снижается, что тормозит дыхание и фосфорилирование. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается. Макроэргические связи и макроэргические соединения, роль в организме. АТФ как важнейший аккумулятор и источник энергииВ живых организмах существует целая группа органических фосфатов, гидролиз которых приводит к освобождению большого количества свободной энергии. Такие соединения называют высокоэнергетическими фосфатами. Разные фосфорилированные соединения обладают разным запасом свободной энергии. К группе высокоэнергетических фосфатов, помимо АТФ, относят енолфосфаты, ангидриды и фосфогуанидины. При гидролизе концевой фосфоангидридной связи АТФ превращается в АДФ и Рн. При этом изменение свободной энергии составляет —7,3 ккал/моль. Величина свободной энергии гидролиза АТФ делает возможным его образование из АДФ за счёт переноса фосфатного остатка от таких высокоэнергетических фосфатов, как, например, фосфоенолпируват или 1,3-бисфосфоглицерат; в свою очередь, АТФ может участвовать в таких эндергонических реакциях, как фосфорилирование глюкозы или глицерина. АТФ выступает в роли донора энергии в эндергонических реакциях многих анаболических процессов. Некоторые биосинтетические реакции в организме могут протекать при участии других нуклеозидтрифосфатов, аналогов АТФ; к ним относят гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ) и цитидинтрифосфат (ЦТФ). Все эти нуклеотиды, в свою очередь, образуются при использовании свободной энергии концевой фосфатной группы АТФ. Наконец, за счёт свободной энергии АТФ совершаются различные виды работы, лежащие в основе жизнедеятельности организма, например, такие как мышечное сокращение или активный транспорт веществ. Таким образом, АТФ — главный, непосредственно используемый донор свободной энергии в биологических системах. В клетке молекула АТФ расходуется в течение одной минуты после её образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 ч. Использование АТФ как источника энергии возможно только при условии непрерывного синтеза АТФ из АДФ за счёт энергии окисления органических соединений. Цикл АТФ—АДФ — основной механизм обмена энергии в биологических системах, а АТФ — универсальная «энергетическая валюта». ЛЕКЦИЯ № 6
Поиск по сайту: |