 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Оксидазный путь использования кислорода в клетке
Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% О2 и обеспечивает процесс окислительного фосфорилирования. Окислительным фосфорилированием называют синтез АТФ из АДФ и Н3РО4 за счет энергии движении электронов по дыхательной цепи. Окислительное фосфорилирование является основным источником АТФ в аэробных клетках.Хемиосмотическая теория МитчеллаДля объяснения механизма окислительного фосфорилирования в 1961 году Митчеллом была предложена хемиосмотическая теория, которая включала четыре независимых постулата, касавшиеся функции митохондрий:1. Внутренняя мембрана митохондрий непроницаема для всех ионов. 2. Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов. 3. При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+ из матрикса в межмембранное пространство. 4. При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровождается синтезом АТФ. Современные представления о механизме окислительного фосфорилированияВ настоящее время открыты все основные компоненты окислительного фосфорилирования, изучено их строение и свойства. Открыты основные принципы окислительного фосфорилирования, регуляция и механизмы некоторых стадий.МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯОкислительное фосфорилирование состоит из процессов окисления и фосфорилирования, которые между собой сопряжены. Процесс окисления Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами. Комплекс I – НАДН2 дегидрогеназный комплекс –самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок.Комплекс III – Комплекс b-c1 (фермент QH2 ДГ), имеет молекулярную массу 500КДа, состоит из 8 полипептидных цепей, и вероятно существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железо-серный белок.Комплекс IV – Цитохромоксидазный комплекс имеет молекулярную массу 300КДа, состоит из 8 полипептидных цепей, существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди.Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q10). Убихинон переносит по 2Н+ и 2е-. Комплекс I – НАДН2 дегидрогеназный комплекс –самый большой из дыхательных ферментных комплексов – имеет молекулярную массу свыше 800КДа, состоит из более 22 полипептидных цепей, в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок.Комплекс III – Комплекс b-c1 (фермент QH2 ДГ), имеет молекулярную массу 500КДа, состоит из 8 полипептидных цепей, и вероятно существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железо-серный белок.Комплекс IV – Цитохромоксидазный комплекс имеет молекулярную массу 300КДа, состоит из 8 полипептидных цепей, существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди.Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q10). Убихинон переносит по 2Н+ и 2е-.  убихинон ↔ семихинон ↔ гидрохинонЦитохром с. Периферический водорастворимый мембранный белок с массой 12,5КДа, содержит 1 полипептидную цепь из 100 АК, и молекулу гема.Молекулярные соотношения между компонентами дыхательной цепи отличаются в разных тканях. Например, в миокарде, на 1 молекулу НАДН2 дегидрогеназного комплекса приходиться 3 молекулы комплекса b-c1, 7 молекул цитохромоксидазного комплекса, 9 молекул цитохрома С и 50 молекул убихинона.Электрохимический потенциал.Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии.I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла. убихинон ↔ семихинон ↔ гидрохинонЦитохром с. Периферический водорастворимый мембранный белок с массой 12,5КДа, содержит 1 полипептидную цепь из 100 АК, и молекулу гема.Молекулярные соотношения между компонентами дыхательной цепи отличаются в разных тканях. Например, в миокарде, на 1 молекулу НАДН2 дегидрогеназного комплекса приходиться 3 молекулы комплекса b-c1, 7 молекул цитохромоксидазного комплекса, 9 молекул цитохрома С и 50 молекул убихинона.Электрохимический потенциал.Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии.I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла.  Этапы движения е- по дыхательной цепи1. 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).2. КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).3. КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.4. Цитохром С переносит е- c III комплекса на IV комплекс.5. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов ∆рН = 60 мВ (при ∆рН=1) (в матриксе рН выше, чем в цитозоле). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов ∆V=160мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 мВ. Механизм переноса Н+ через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:1) фосфорилирования АДФ в АТФ; 2) транспорта веществ через мембрану митохондрий; 3) теплопродукцию.Процесс фосфорилированияПроцесс фосфорилирования осуществляется АТФ-синтетазой (Н+-АТФ-аза), которая потребляет 40-45% свободной энергии, выделившейся при окислении. Н+-АТФ-аза интегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов F0 и F1. Этапы движения е- по дыхательной цепи1. 2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).2. КоQ с 2е- забирает у воды 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).3. КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.4. Цитохром С переносит е- c III комплекса на IV комплекс.5. IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен). При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов ∆рН = 60 мВ (при ∆рН=1) (в матриксе рН выше, чем в цитозоле). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов ∆V=160мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 мВ. Механизм переноса Н+ через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:1) фосфорилирования АДФ в АТФ; 2) транспорта веществ через мембрану митохондрий; 3) теплопродукцию.Процесс фосфорилированияПроцесс фосфорилирования осуществляется АТФ-синтетазой (Н+-АТФ-аза), которая потребляет 40-45% свободной энергии, выделившейся при окислении. Н+-АТФ-аза интегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов F0 и F1. 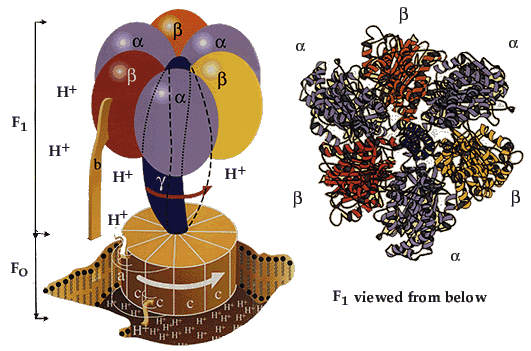
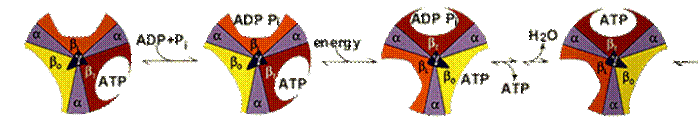 АТФ-синтетаза обеспечивает обратимое взаимопревращение энергии электрохимического потенциала и энергии химических связей.Электрохимический потенциал внутренней мембраны заставляет Н+ двигаться из межмебранного пространства по каналу АТФ-синтазы в матрикс митохондрий. При каждом переносе протонов через канал Fo энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация а- и β-субъединиц и все 3 активных центра, образованных парам α- и β-субъединиц, катализируют очередную фазу цикла: 1) связывание АДФ и Н3РО4; 2) образование фосфоангидридной связи АТФ; 3) освобождение конечного продукта АТФ. АТФ-синтетаза обеспечивает обратимое взаимопревращение энергии электрохимического потенциала и энергии химических связей.Электрохимический потенциал внутренней мембраны заставляет Н+ двигаться из межмебранного пространства по каналу АТФ-синтазы в матрикс митохондрий. При каждом переносе протонов через канал Fo энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация а- и β-субъединиц и все 3 активных центра, образованных парам α- и β-субъединиц, катализируют очередную фазу цикла: 1) связывание АДФ и Н3РО4; 2) образование фосфоангидридной связи АТФ; 3) освобождение конечного продукта АТФ.
Поиск по сайту: |
©2015-2020 studopedya.ru Все права принадлежат авторам размещенных материалов.
