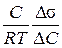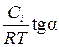|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Використовуємо формулу рівння Гіббса
Г = – [Г] = Відповідь: Г = 7,2 × 10−6 моль/м2. Приклад 2.При 293 К поверхневий натяг ртуті становить 0,458, а амальгами калію (С = 0,11 моль/л) − 0,393 Дж/м2. Визначити адсорбцію калію на поверхні ртуті. Розв’язання: 1. Г − ? В рівнянні (2) можна замінити похідну Г = – [Г] = Відповідь: Г = 2,66 × 10−5 моль/м2. За рівнянням Гіббса можна обчислити адсорбцію розчиненої речовини при різних концентраціях. Для цього будують графік залежності поверхневого натягу від концентрації. Необхідні значення
Рис. 1. Визначення надлишкової адсорбції
Перемноживши одержані значення tga на С/RT одержують Г, за якими можна побудувати повну криву Г= f(C) – ізотерму адсорбції, з якої потім знайти адсорбцію за іншими концентраціями (рис. 1). Зі збільшенням концентрації адсорбція зростає до певної межі, деякого максимального (граничного) значення Г¥. За величиною Г¥ можна одержати відомості про будову адсорбційного шару. З рівняння Гіббса випливає, що основною характеристикою адсорбата є величина g = –( Чим більше зменшується поверхневий натяг з зростанням концентрації адсорбата, тим більше його поверхнева активність. Приклад 3.Визначити адсорбцію масляної кислоти на поверхні розділу водний розчин − повітря при 283 K та концентрації С = 0,104 моль/л, використавши наступні експериментальні дані. Сі, кмоль/м30,00 0,021 0,050 0,104 0,246 0,489 sі×103, Дж/м2 74,01 69,51 64,30 59,85 51,09 44,00 Задачу вирішити розрахунковим та графічним способом. Розвۥязання: Розрахунковий спосіб. 1. Г = ? Г = – Графічний спосіб. DСі/Dsі−? Гі =? tga1 = tga2 = tga3 = tga4 = tga5 =
Графічні визначення зведені до таблиці
Відповідь: Гтеор = 6,02·10−6 моль/м2, Гграф = 5,72·10−6 моль/м2. Для жирних кислот (поширених ПАР) на підставі великого експериментального матеріалу було знайдено, що поверхнева активність в водних розчинках зростає у 3÷3,5 рази при збільшенні карбонового ланцюгу на групу СН2 (правило Дюкло −Траубе).
Поиск по сайту: |
 = –
= –  = + 7,2 × 10−6 моль/м2.
= + 7,2 × 10−6 моль/м2. . Оскільки Г > 0 і σ2 < σ1, то адсорбція позитивна.
. Оскільки Г > 0 і σ2 < σ1, то адсорбція позитивна.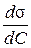 на
на 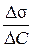 .
.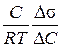 = –
= – 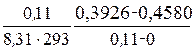 = + 2,66 × 10−5 моль/м2.
= + 2,66 × 10−5 моль/м2.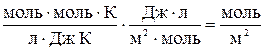 .
. відповідають різним концентраціям С1, С2, С3 і т.д., проводять дотичні; за кутами нахилу їх до вісі абсцис визначають тангенси кутів tga =
відповідають різним концентраціям С1, С2, С3 і т.д., проводять дотичні; за кутами нахилу їх до вісі абсцис визначають тангенси кутів tga = 

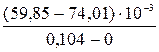 = 6,02·10−6 моль/м2.
= 6,02·10−6 моль/м2.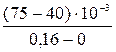 = 0,215
= 0,215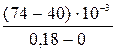 = 0,18
= 0,18 = 0,13
= 0,13 = 0,66
= 0,66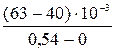 = 0,043
= 0,043