 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Тема 3. Компоненти середовища, які містять азот та їх асиміляція мікроорганізмами
3.1 Азотмісткі компоненти середовища
Всім живим організмам, у тому числі мікроорганізмам, необхідний азот. Земна атмосфера містить його набагато більше, ніж потрібно для задоволення потреб живих істот. Однак азот хімічно стійкий, він важко окисляється. Круговорот азоту в природі являє собою складний цикл, у ході якого спочатку повинна бути порушена хімічна інертність азоту. Ряд мікроорганізмів володіє здатністю поглинати вільний азот повітря й зв'язувати його у вигляді органічних сполук. Промислово важливі культури, як правило, не є фіксаторами атмосферного азоту. Виключення становлять ті виробництва, де для потреб сільського господарства готують бактеріальні препарати азотфіксаторів. У середовищах для культивування необхідно мати такі азотмісткі речовини, які можуть бути засвоєні мікроорганізмами. А це значить, що вони повинні мати таку структуру, що здатна проходити через клітинну стінку. Клітина повинна мати ферментні системи, які забезпечать включення цього з'єднання в обмін речовин. Крім того, азотмісткі речовини, так само як й інші компоненти середовища, повинні задовольняти наступним умовам: забезпечувати досить високий вихід біомаси або синтезованого продукту, бути вигідними економічно. Азот поживного середовища йде головним чином на синтез білків мікроорганізмів. Білки, як відомо, складаються з амінокислот. Можуть бути два принципово різних шляхи для задоволення потреби в амінокислотах: одержання готових амінокислот ззовні й самостійний синтез амінокислот з компонентів середовища. Азот у середовищах для культивування може бути присутнім у мінеральних з'єднаннях або входити до складу органічних речовин, що втримуються в рослинному або тваринному продуктах. Для лабораторних дослідів або одержання особливо важливих або дорогих продуктів мікробіологічного синтезу можуть бути використані м'ясні середовища Однак вони із украй обмеженими областями використання. Може бути використане рибне борошно. Гарним для багатьох процесів продуктом є молочна сироватка, однак не вирішені питання, пов'язані з її концентруванням і транспортуванням. З рослинних продуктів досить широко поширені кукурудзяний екстракт, соєве, арахісове, кукурудзяне борошно, різні макухи й шроти. В останні роки одержує поширення середовище із дріжджів, вирощених на вуглеводнях або гідролізатах деревини. Дріжджі звичайно попередньо піддають ферментативній або хімічній обробці для одержання розчинних продуктів. Істотним недоліком цих продуктів є мінливість їхнього хімічного складу й відсутність можливості скільки-небудь надійно стандартизувати їх. З азотмістких з'єднань тут переважають білки, пептиди, вільні амінокислоти, нуклеїнові кислоти, олігонуклеотиди і т. д У кукурудзяному екстракті приблизно половина кількості по масі доводиться на воду; вміст загального азоту коливається в межах 3,0-8,0 % (у перерахуванні на суху масу); амінного азоту-1,0-3,0%. Цей екстракт містить всі протеїногенні амінокислоти. Кількість окремих амінокислот істотно коливається залежно від ступеня зрілості, сорту, місця зростання й методу обробки кукурудзи. Останнє рівною мірою відноситься і до всіх інших рослинних продуктів. Кукурудзяний екстракт на відміну від інших природних продуктів, використовуваних як компоненти середовищ, містить відносно небагато білкових речовин і більше вільних амінокислот або низькомолекулярних пептидів. Білковими речовинами більш багате соєве борошно Необхідно мати у виді, що всі перераховані речовини одночасно служать джерелами вуглецю. Як було відзначено в попередній темі білки, що втримуються в середовищі, перш ніж надійти в клітину повинні бути гідролізовані до амінокислот чи олігопептидів. У ряді випадків, коли в культури відсутня транспортна система для тих або інших амінокислот, вони піддаються дезамінуванню. Ферментативний гідроліз білків середовища здійснюють позаклітинні протеази й пептидази В різних мікроорганізмів залежно від їхніх генетичних особливостей і фізіологічного стану синтезуються й виділяються в середовище ферменти, що діють у різних інтервалах рН й володіють виборчою специфічністю. З мінеральних з'єднань азоту до складу середовищ вводять солі, що містять іон амонію або нітрат-іон. Безпосередньо в обмін речовин мікробної клітини включається іон амонію. У зв’язку із цим якщо в середовище уведений нітрат-іон, то він повинен бути відновлений. Відновлення нітрату-іона до нітриту відбувається в нітрат-редуктазній реакції, здійснюваній молибденмісткою нітрат-редуктазою. Ферментні системи, які каталізують хід реакцій від нітриту до аміаку, не описані. Передбачається, що проміжними продуктами тут є гіпоінтрит і гідроксиламін. Однак вони не були ідентифіковані як продукти даної реакції в мікробних клітинах:
Застосування солей азотної кислоти може викликати різке зрушення рН середовища в лужну зону. Відбувається це внаслідок інтенсивного використання азоту й незбалансованого нагромадження катіона, що був внесений разом із сіллю. При введенні в середовища амонійних солей спостерігається зрушення рН у кислу область. Щоб уникнути закислювання, у середовище додають крейду. Іон Са2+ утворює із багатьма аніонами нерозчинні солі. Якщо в якості кінцевого готового продукту використовується біомаса, то цей метод непридатний, тому що нерозчинні солі кальцин залишаться на фільтрі.
3.2 Ферментативні механізми асиміляції
Амонійний азот, потрапляючи в клітину, включається шляхом амінування в органічні сполуки, утворюючи амінокислоту. Такими органічними сполуками в першу чергу є кислоти, що містять кетогрупу: піровиноградна, α-кетоглутарова, щавлевооцтова. Синтез глютамінової кислоти відбувається завдяки активності глутаматдегідрогенази:
Є точка зору, що система НАДФ функціонує тоді, коли відбувається синтез амінокислоти, а НАД - у випадку катаболічного процесу. Глутаматдегідрогеназа є алостеричним ферментом, що вкрай важливо у зв'язку із центральним місцем, що вона займає в обміні амінокислот. Із глютамінової кислоти за допомогою ряду ферментативних реакцій синтезується пролін, аргінін, а також ряд інших амінокислот за допомогою реакції транс-амінування. У багатьох мікроорганізмів глутаматдегідрогеназа є єдиною ферментною системою, що здійснює включення амонійного азоту в молекулу органічної речовини. Через піровиноградну кислоту відбувається синтез α-аланіну. Аланіндегідрогеназа здійснює наступну реакцію:
Питання про безпосереднє ензиматичне включення іону амонію в молекулу щавлевооцтової кислоти залишається відкритим. Аспарагінова кислота утворюється з фумарової кислоти і іона амонію. Ферментативний каталіз здійснює аспартаза (аспартат-аміак-ліаза):
Як у реакціях анаболізму, так і катаболізму амінокислот беруть участь трансамінази (амінотрансферази), що здійснюють перенос α-аміногрупи амінокислоти до α-вуглецевому атома піровиноградної, α-кетоглутарової або щавлевооцтової кислот. У результаті реакції утворюється α-кетоаналог амінокислоти, а α-кетокислота перетворюється у відповідну α-амінокислоту:
Реакції, які каталізують трансамінази, легко оборотні, та їхні константи рівноваги звичайно близькі до одиниці. Для всіх відомих трансаміназ коферментом служить піридоксальфосфат. Вище було відзначено, що через відсутність транспортних систем для переносу амінокислот у клітині може відбуватися ензиматичне відщіплення аміногруп. Думають також, що цей механізм дозволяє культурі створювати необхідну буферну систему в середовищі. Відомо кілька ферментних систем, що здійснюють дегідрогеназні реакції на аліфатичних амінокислотах, у результаті чого одним із продуктів реакції є іон амонію:
У цих реакціях функцію акцептора виконує НАД+ або НАДФ+. Існують також ферментні системи, де акцептором служить кисень. Це оксидаза L-амінокислот:
При зрушенні рН у кислу зону відзначається реакція декарбоксилювання амінокислот з утворенням амінів:
Серед амінів зустрічаються високотоксичні речовини, що утворюються при декарбоксилюванні лізину й орнітину, відповідно кадаверин і путресцин; з гістидина - гістамін, сильний засіб, що впливає на кров'яний тиск. У бактерій й актиноміцетів є ферментні системи декарбоксилювання глютамінової кислоти. При цьому залежно від того, яка з карбоксильних груп піддається декарбоксилюванню, утворюється α- або γ-аміномасляна кислота. Ароматичні амінокислоти проходять більш складний шлях катаболізму, ніж аліфатичні, перетворюючись у метаболіти, які легко асимілюються клітиною. Ці ферментні системи звичайно перебувають усередині клітини. При вивченні можливості використання амінокислот як джерела вуглецевого і азотного харчування до складу середовища вводять досліджувану амінокислоту, потім визначають її кількісний вміст по ходу культивування. Паралельно проводять спостереження за ростом культури. При використанні комплексних середовищ, що містять продукти невизначеного хімічного складу (дріжджовий екстракт, соєве борошно й т.п.), частина амінокислот перебуває у вільному стані, частина - у зв'язаному. В цьому випадку дуже важко встановити, які із присутніх у середовищі амінокислот найбільше інтенсивно включаються в метаболізм. Білок середовища протягом деякого часу залишається не повністю гідролізованим протеазами мікроорганізму. Амінокислоти поступово звільняються при гідролізі білка, тому для оцінки інтенсивності включення амінокислот в обмін речовин створюють синтетичні середовища, що складаються з індивідуальних амінокислот. Аналіз вмісту амінокислот у таких середовищах показує, наприклад, що в дослідах з актиноміцетом раніше інших із середовища зникають глютамінова й аспарагінова кислоти і α-аланін. Такі досліди дозволяють урахувати можливу взаємодію між амінокислотами. Вплив джерела азоту на біосинтез продукту або ріст біомаси залежить не тільки безпосередньо від конкретного джерела азоту, але також і від загальної композиції середовища. Істотне значення тут має відношення присутнього в середовищі азоту до вуглецю (N: С). Стосовно до кожного штаму-продуцента в цільовому продукту ця величина буде різною.
Контрольні питання: 1. Навести приклад найбільш вживаних у біотехнології азотмістких компонентів поживних середовищ 2. Розкрити особливості засвоювання азоту середовища мікроорганізмами 3. Охарактеризувати ферментативні механізми асиміляції
Поиск по сайту: |

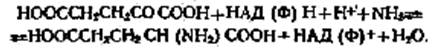 .
.




