|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
УТИЛИЗАЦИЯ ОТХОДОВ И ОБЕЗВРЕЖИВАНИЕ ОТХОДЯЩИХ ГАЗОВ В ПРОИЗВОДСТВЕ СЕРНОЙ КИСЛОТЫ ⇐ ПредыдущаяСтр 8 из 8
В производстве серной кислоты образуются твёрдые, жидкие и газообразные отходы. К твёрдым отходам следует отнести огарок и селеновый шлам при производстве серной кислоты из серы. К жидким отходам следует отнести кислые воды (содержащие серную кислоту). При нормальной работе цеха серной кислоты кислых вод не образуется. Кислые стоки образуются только в аварийных ситуациях при течи холодильников или разрыве трубопроводов. Кислая вода нейтрализуется на стадии известковым молоком или содой. При производстве серной кислоты из колчедана на 1 т серной кислоты образуется 700-750 кг огарка. Огарок используется для: - производства цемента в виде железосодержащего шлака вводится в цементную шихту, что позволяет снизить температуру обжига клинкера, понизить расход топлива и повысить прочность цемента - производства стекла - удобрения почв в сельском хозяйстве. На эти цели используется приблизительно 50% огарка. Огарок содержит более 50% железа. В нём также содержится медь, цинк, свинец, кобальт, мышьяк, серебро и другие металлы. В настоящее время стоит задача комплексной переработки огарка с получением цветных и благородных металлов. Комплексная переработка огарка состоит в том, что его подвергают низкотемпературному обжигу в присутствии хлорида натрия, хлора и хлороводорода. После обжига огарок, содержащий хлориды металлов, обрабатывают раствором серной кислоты с переводом в раствор меди, цинка, кобальта и серебра. Оставшийся твёрдый огарок перерабатывают в доменных печах. Степень извлечения меди составляет 78%, серебра–72%, цинка–74%, кобальта–51%. В Японии разработана технология, где из огарка извлекают 14 элементов. Селеновый шлам – рассмотрен ранее. Битум, содержащий более 50% серы, при производстве серной кислоты из серы в настоящее время используется в дорожном строительстве. Комплексная переработка битума с извлечением серы является важнейшей задачей, но пока технологии нет. Газовые выбросы В технологических схемах производства серной кислоты одинарного контактирования в отходящих газах содержится 0,2% SO2 и приблизительно 0,007% SO3. По санитарным нормам такие газы нельзя выбрасывать в атмосферу без предварительной очистки. Ежегодно в мире выбрасывается в атмосферу около 200 млн. тонн SO2 и каждые 20 лет эта цифра удваивается. 50,3 – ТЭУ 20 – автотранспорт 7,4 – цветные металлы 2,3 – нефтепереработка 1,2 – химическая промышленность 0,4 – промышленность стройматериалов. Существуют следующие основные способы утилизации SO2. 1. Если концентрация SO2 в отходящих газах составляет 4 %, то такие газы можно перерабатывать на серную кислоту по существующим схемам. 2. Поглощение SO2 химическими поглотителями с их последующей регенерацией или с получением ценных химических продуктов. 3. Каталитические способы очистки отходящих газов с получением серной кислоты. Предельно допустимая концентрация SO2 в зоне производственных помещений составляет 10 мг/м3, SO3 – 1 мг/м3. Наиболее широкое распространение получили следующие методы: - сульфит-бисульфитный - кислотно-каталитический - магнезитовый Сульфатно-бисульфитный метод. SO2+2NH4OH=(NH4)2SO3+H2O (NH4)2SO4+SO2=2NH4 HSO3 SO3+2NH4OH+H2O=(NH4)2SO4+H2O Имеющиеся пары кислоты взаимодействуют с аммиачной водой с образованием сульфата аммония. H2SO4+2NH4OH=(NH4)2SO3+H2O Сульфит-бисульфитный раствор может использоваться в кожевенном производстве. В последние годы сульфит-бисульфитный раствор нашёл применение как консервант кормов для животных в сельском хозяйстве. При добавлении в раствор серной кислоты будет образовываться сульфат аммония и чистый SO2. (NH4)2SO3+H2SO4=(NH4)2SO4+SO2+H2O Если при поглощении аммиачной водой SO2 в газовой фазе высокое парциальное давление аммиака, то взаимодействие SO2 осуществляется не в растворе, а в газовой фазе с образованием тумана (NH4)2SO3. В промышленности поглощение SO2 осуществляется сульфит-бисульфитным раствором и отношение SO2 и аммиака составляет 0,7%, а рН раствора составляет 5-5,5. По мере понижения рН в раствор вводят NH4OH. Технологическая схема очистки газов сульфит-бисульфитным способом(рисунок 28).
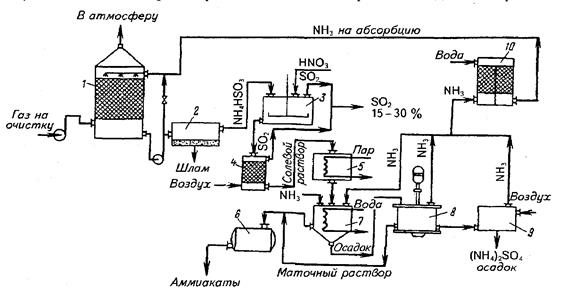
Рисунок 28 - Технологическая схема очистки газов сульфит-бисульфитным способом
1 - распылительный абсорбер, 2 – фильтр, 3 – реактор, 4 – отгонная колонна, 5 – выпарной аппарат, 6 – сборник, 7 – смеситель, 8 – центрифуга, 9 – отдувочный аппарат, 10 – абсорбер поглощения аммиака. Отходящие газы после абсорбции поступают в распылительный абсорбер, который орошается сульфит-бисульфитным раствором с рН 5-5,5 и отношением SO2:NH3=0,2. В сборник для поддержания постоянного рН вводят 25% раствор NH4OH. Избыточный раствор из цикла абсорбера подаётся в насадочный скрубер, в нижней части которого имеется кипятильник раствора. Нагрев кубовой части осуществляется паром до температуры 103-105°С. В верхнюю часть скрубера подаётся 93% серная кислота и сульфит-бисульфитный раствор разлагается с образованием сульфата аммония и 100% SO2. 100% SO2 возвращается в продувочную колонну серной кислоты, а 40% раствор сульфата аммония перерабатывается на удобрение. На некоторых предприятиях абсорбцию осуществляют не аммиачной водой, а содой. В этом случае получают раствор сульфит-бисульфита натрия. Кислотно-каталитический способ очистки. Он основан на том, что соли марганца в жидкой фазе могут окислять SO2 до серной кислоты. Этот способ можно применить только для очистки отходящих газов, не содержащих другие примеси, например CO2. 2MnO2+3SO2=MnSO3 +MnS2O6 MnS2O6 +H2SO4 =MnSO4 + H2S2O6 H2S2O6=2HSO3 HSO4+O2+2H2O = 2H2SO3+2OH (радикал) 2MnSO4+2OH(-)+H2SO4 = Mn2(SO4)3 + H2O Mn2(SO4)3 + H2O+ SO2=MnSO4 + 2H2SO4 Технологическая схема(рисунок 29).
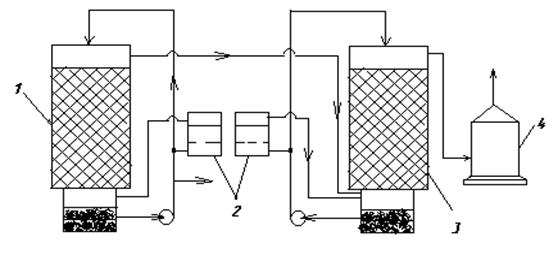
Рисунок 29 - Технологическая схема кислотно-каталитического способа очистки
1 – первый абсорбер, 2 - фильтры, 3 – второй абсорбер, 4 – брызгоуловитель. Отходящие газы последовательно проходят две насадочные башни. Первая орошается 15-20% раствором серной кислоты, а вторая–5% раствором. Кислота перед орошением последовательно проходит фильтры, где насыщается MnO2. Концентрация MnO2 поддерживается на уровне 0,3-0,1%. Степень очистки составляет 60-70%. Основной недостаток – это коррозия металла из-за трещин, а также выделяющегося водорода, который восстанавливает серу до сероводорода и при этом резко тормозится реакция окисления SO2 в жидкой фазе до серной кислоты.
Магнезитовый способ В этом процессе поглотителем служит суспензия MgO. MgO+ H2O= Mg(OH)2 Mg(OH)2+SO2+5H2O =MgSO3*6H2O При термическом разложении кристаллогидрат разлагается с образованием SO2. MgSO3*6H2O= SO2+6H2O+MgO Технологическая схема магнезитовой очистки отходящих газов(рисунок 30).
Рисунок 30 - Технологическая схема магнезитовой очистки отходящих газов
1 – бункер с вибратором для хранения MgO, 2 – система весов, 3 –емкость для свежего раствора, 4 – неочищенный дымовой газ, 5 - дымосос, 6 – абсорбер SO2, 7 –дымовая труба, 8 – пылеуловитель, 9 – центрифуга, 10 – конвейер для мокрого кека, 11 – емкость для маточного раствора, 12 – барабанная сушилка, 13 – бункер для хранения MgSO3. Отходящие газы, содержащие SO2, поступают в абсорбер, который орошают суспензией сульфита гидроксида магния. ТЭА. 1:10 С(MgO)=180-190 г/л, рН сусп.=6,7-7,2 на выходе и 5,5-5,8 на входе. Содержание SO2 на выходе 0,03%. Суспензия, выходящая из абсорбера, частично поступает в сборник, а оставшаяся часть проходит гидроциклоны и фильтр-пресс. Жидкая фаза после ленточного фильтра возвращается в сборник, а кристаллы MgCO3*6H2O поступают в печь кипящего слоя. В нижнюю часть печи подаются топочные газы с температурой 1000°С. На первых двух полках происходит сушка, дегидратация MgCO3*6H2O . Не ост. термическое разложение (750-800°С). Отходящие газы, содержащие 15-18% SO2, перерабатывают на элементарную серу или серную кислоту, а оксид магния идёт в сборник для поддержания концентрации MgO в суспензии 180-190 г/л и рН раствора 7,2-7,3. Достоинства: - MgO возвращается в продукт - оксид магния является дешёвым продуктом и стоимость очистки ниже значения стоимости других способов очистки. - магнезитовый способом можно поглощать SO2 из отходов газов ТЭУ, которые содержат кроме SO2, сажу. Степень очистки от SO2 при Х=0,2% составляет 75%. Недостатки: высокий расход энергии на сушку и термообработку сульфата магния.
Содержание Предисловие......................................................................................... 2 Введение............................................................................................... 3 Лекция 1. Применение серной кислоты............................................... 4 Лекция 2. Сырьё для производства серной кислоты.......................... 8 Лекция 3. Физико-химические основы и аппаратурное оформление процесса обжига колчедана................................................................................................. 12 Лекция 4. Мокрая очистка газа......................................................... 19 Лекция 5. Осушка обжигового газа.................................................. 25 Лекция 6. Каталитическое окисление SO2 в SO3............................... 28 Лекция 7. Абсорбция SO3.................................................................. 40 Лекция 8. Получение серной кислоты из природной серы по короткой схеме 42 Лекция 9. Концентрирование серной кислоты................................. 49 Лекция 10. Пути усовершенствования производства СК................. 57 Лекция 11. Утилизация отходов и обезвреживание отходящих газов в производстве серной кислоты........................................................................................ 62 Литература......................................................................................... 69
Поиск по сайту: |