|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Исследование других органов 9 страница
У больных с ФК IV по NYHA, которые при проведении 6-минутного теста-ходьбы могут пройти в умеренном темпе не более 150 м (см. выше), показаны регулярные дыхательные упражнения или физические упражнения в положении сидя. Например, больным можно рекомендовать редкое, медленное и глубокое дыхание с пролонгированным вдохом или выдохом (4–5 дыхательных циклов за 1 мин). У больных ФК III (дистанция 6-минутной ходьбы до 300 м), находящихся в стабильном состоянии, наиболее простым и доступным методом физической тренировки является дозированная ходьба. В течение первых 5 недель рекомендуется ежедневно проходить 1 км за 13–15 мин (всего около 8–10 км в неделю). В зависимости от индивидуальной переносимости, начиная с 6-й недели, увеличивают расстояние, пройденное за неделю до 10–20 км; при этом скорость ходьбы увеличивается до 11 мин на 1 км. Больным ФК I–II по NYHA (дистанция 6-минутной ходьбы, соответственно, до 500 м и 400 м) рекомендуют сочетание нескольких видов нагрузки, например ходьбы и плавания. В зависимости от функционального состояния больных и индивидуальной тренированности величина и мощность дозируемой физической нагрузки могут быть пересмотрены.
Диета больных ХСН должна быть калорийной, легкоусвояемой и скорректированной в отношении суточного приема соли и жидкости. Целесообразно дробное питание 5–6 раз в сутки. Общая калорийность питания рассчитывается с учетом массы тела (МТ) и ФК больных ХСН. Для характеристики МТ в настоящее время используют расчет так называемого индекса массы тела (ИМТ) по формуле:
В табл. 2.10. приведены значения ИМТ у пациентов с избыточным весом, ожирением и дефицитом МТ. Таблица 2.10 Характеристика массы тела в зависимости от величины ИМТ
Обычно для больных ХСН с нормальной МТ (ИМТ — 20–25), ведущих малоподвижный образ жизни или выполняющих легкую физическую нагрузку, общая калорийность суточного рациона составляет 1900–2500 ккал. Если у больных имеется избыточная МТ или ожирение, следует предусмотреть уменьшение пищевого рациона на 20–30%, в частности за счет содержания в пище животных жиров. Наоборот, при дефиците МТ (ИМТ меньше 20) у больных с сердечной кахексией суточная калорийность диеты должна быть на 20–30% больше. Из рациона питания больных ХСН целесообразно исключить шоколад, крепкий чай и кофе, острые блюда, копчености, продукты, богатые холестерином (животный жир, икра, мозги и т.п.), мучные изделия, жирные сорта мяса, сало и т.п. Резко ограничивают или исключают прием алкоголя и запрещают курение. Потребление поваренной соли обычно ограничивают до 5–6 г в сутки. Более значительное ограничение в пище натрия хлорида (до 1,5–3,0 г в сутки) показано в периоды дестабилизации состояния больных, при быстром прогрессировании симптомов левожелудочковой недостаточности или отечного синдрома. В этих случаях больным предлагается не подсаливать пищу и не употреблять продукты, содержащие повышенное количество NаCl (соленые огурцы, рыба, копчености). Даже такое ограничение обычно обеспечивает потребление соли не более 3,0 г в сутки. Если необходимо еще больше ограничить поступление NаСl (до 1,0–1,5 г в сутки), например, при выраженном отечном синдроме, пациентам ХСН дополнительно рекомендуют приготовление пищи без соли. Ограничение потребляемой жидкости должно быть достаточно разумным. При любой стадии ХСН не следует уменьшать количество вводимой жидкости меньше 0,8 л. Обычно оно составляет 1,2–1,5 л в сутки, включая все жидкие блюда (супы, чай, соки и т.п.). Даже на фоне отечного синдрома резкое ограничение вводимой жидкости в ряде случаев может сопровождаться повышением осмолярности плазмы, что приводит к избыточной продукции антидиуретического гормона (АДГ) и способствует еще большей задержке жидкости в организме и усилению отеков. В этих случаях ограничение приема натрия хлорида оказывается более эффективным, чем уменьшение количества вводимой жидкости. Больным ХСН рекомендуют употреблять в пищу продукты, содержащие калий (курагу, изюм, печеный картофель, орехи, брюссельскую капусту, бананы, персики, гречневую и овсяную крупу, телятину и др.). Калиевая диета особенно показана при лечении мочегонными средствами и сердечными гликозидами. | |||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
Представления о наиболее рациональных способах медикаментозной терапии больных ХСН за последние 50 лет претерпели существенные изменения. До 50-х годов прошлого века, когда господствовала так называемая кардиальная модель ХСН и вся симптоматика недостаточности кровообращения однозначно связывалась с падением сократимости миокарда, основным средством лечения считались сердечные гликозиды, обладающие положительным инотропным действием на сердце.
В 50–60-е годы, когда разрабатывалась кардиоренальная модель ХСН, согласно которой ведущая роль в прогрессировании ХСН и избыточной задержке Nа+ и воды отводилась почкам (циркулирующая РААС), наряду с сердечными гликозидами стали активно внедряться разнообразные мочегонные средства.
В 70-е годы была продемонстрирована роль нарушений периферического кровообращения в патогенезе ХСН (циркуляторная модель), и в клиническую практику стали широко внедряться периферические вазодилататоры, снижающие нагрузку на сердце.
В 80–90-е годы сформировалась нейрогуморальная концепция патогенеза ХСН, связывающая изменения, происходящие в органах, в том числе в сердце, с активацией не только циркулирющих, но и тканевых нейрогормонов, в первую очередь катехоламинов, ангиотензина II, альдостерона, эндотелиальных факторов. Это привело к представлению о необходимости блокирования активности нейрогормонов с помощью ингибиторов АПФ и b-адреноблокаторов, несмотря на отрицательное инотропное действие последних на сердце.
Наконец, в последние годы была вновь продемонстрирована ведущая роль гемодинамических расстройств, связанных с изменением систолической и диастолической функции миокарда, происходящим в том числе под влиянием нейрогормонов (миокардиальная, систоло-диастолическая модель).
В соответствии с этой концепцией все ЛС, применяемые при ХСН, можно разделить на 3 группы. 1. Основные (базисные) ЛС, эффективность и безопасность применения которых у больных ХСН хорошо доказана и не вызывает сомнений. К их числу относят 4 класса препаратов:
2. Дополнительные ЛС, эффективность которых также достаточно высока, но требуют уточнения некоторые вопросы показаний и противопоказаний, а также влияния этих препаратов на отдаленный прогноз больных ХСН. К дополнительным ЛС относятся:
3. Вспомогательные ЛС,применение которых необходимо в определенных конкретных клинических ситуациях:
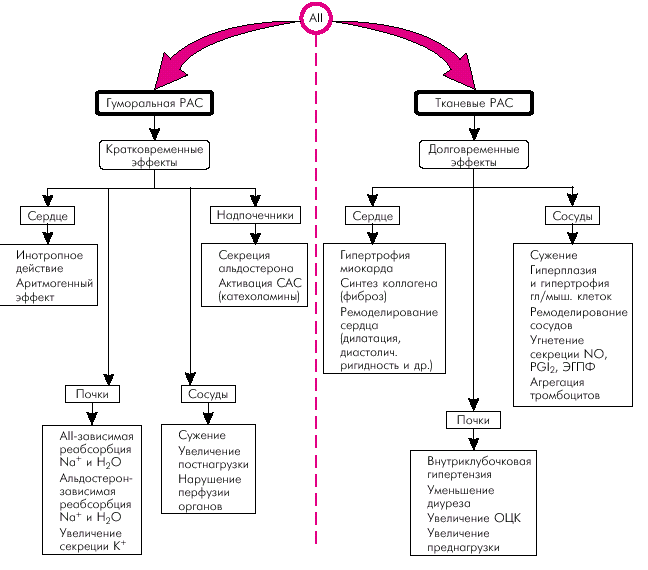
Рассмотрим применение у больных ХСН базисных и некоторых вспомогательных (дополнительных) лекарственных препаратов. Ингибиторы АПФ По современным представлениям, ингибиторы АПФ являются “золотым стандартом” терапии больных ХСН (T. Cohn, 1988, E. Braunwald, 1991). В последние годы были получены убедительные доказательства способности ингибиторов АПФ замедлять прогрессирование ХСН, снижать летальность, улучшать прогноз и качество жизни больных ХСН. Механизм действия Механизм действия ЛС, относящихся к классу ингибиторов АПФ, связан с их способностью блокировать эффекты ключевого фермента РААС, “запускающего” целый каскад изменений в органах и тканях, которые закономерно приводят к развитию и прогрессированию СН (см. выше). При этом речь идет о действии ингибиторов АПФ как на ренально-надпочечниковую (гуморальную) РААС, так и на тканевые РАС (рис. 2.37). Последнее обстоятельство имеет особенно важное значение, поскольку активация именно тканевых нейрогормонов лежит в основе ремоделирования сердца и формирования систолической и диастолической дисфункции миокарда.
Напомним, что повышение в миокарде содержания тканевого АII сопровождается вазоконстрикцией коронарных сосудов, развитием гипертрофии миокарда, быстрым прогрессированием интерстициального фиброза, нарушением кальциевого обмена в кардиомиоцитах, что приводит к развитию диастолической ригидности миокарда и повышает риск развития аритмий. Кроме того, активация тканевых РАС в сосудистой стенке различных органов ведет к пролиферации гладкомышечных клеток, гипертрофии и утолщению стенки сосудов, а также уменьшает высвобождение эндотелиальных факторов релаксации. Повышается также агрегация тромбоцитов и риск тромбообразования, что еще больше усугубляет нарушения перфузии жизненно важных органов (сердце, головной мозг, почки).
Кроме того, воздействие ингибиторов АПФ на гуморальную (эндокринную) РААС и уменьшение образования циркулирующегоАII также имеют несколько важных следствий. 1. Расширение сосудов (артериол и вен) обусловлено, прежде всего, уменьшением сосудосуживающих влияний самого АII. Однако следует помнить, что АПФ не только катализирует превращение АI в АII, но одновременно регулирует функциональное состояние калликреин-кининовой системы, являясь ферментом (кининаза II), инактивирующим один из наиболее мощных вазодилататоров организма — брадикинин (рис. 2.38). В результате подавления активности АПФ лекарственными препаратами, относящимися к его ингибиторам, увеличивается концентрация в крови брадикинина и развивается вазодилатация. Брадикинин, в свою очередь, стимулирует секрецию эндотелиальных факторов расслабления (PGI2, NO, ЭГПФ), также обладающих выраженным вазодилатирующим и антиагрегантным эффектами. В результате происходит системная артериальная вазодилатация, сопровождающаяся снижением ОПСС, системного АД и величины постнагрузки на ЛЖ. Венозная дилатация, развивающаяся под действием ингибиторов АПФ, способствует уменьшению притока крови к сердцу, снижению давления наполнения и, соответственно, величины преднагрузки. 2. Под действием ингибиторов АПФ уменьшается синтез альдостерона в надпочечниках, что сопровождается снижением альдостеронзависимой реабсорбции Nа+ и воды в дистальных канальцах почек. Одновременно уменьшается секреция ионов К+. 3. Снижая содержание циркулирующего АII, ингибиторы АПФ уменьшают ангиотензинзависимую реабсорбцию Nа+ и воды в проксимальных канальцах. Таким образом, происходящее под действием ингибиторов АПФ уменьшение задержки Nа+ и воды также ведет к уменьшению ОЦК и величины преднагрузки. 4. Наконец, ингибиторы АПФ подавляют стимулированное АII образование норадреналина и, соответственно, снижают активность САС.
Показания Лечение ингибиторами АПФ показано у большинства больных ХСН, независимо от генеза, стадии сердечной недостаточности и функционального класса ХСН. К числу наиболее частых клинических ситуаций, при которых целесообразно назначение ингибиторов АПФ (в качестве монотерапии или в комбинации с диуретиками, сердечными гликозидами и/или b-адреноблокаторами), относятся:
В настоящее время доказана эффективность ингибиторов АПФ практически у всех больных с сердечной недостаточностью, независимо от уровня активности почечно-надпочечниковой (гуморальной) РААС, в том числе при высокоренинной и низкоренинной формах ХСН. Побочные эффекты При лечении ингибиторами АПФ побочные эффекты в целом развиваются у 7–9% больных ХСН. К числу наиболее клинически значимых побочных эффектов ингибиторов АПФ относятся:
Артериальная гипотензия встречается у 4–5% больных ХСН, даже при правильном назначении ингибиторов АПФ. Наиболее часто артериальная гипотензия развивается в первые 1–3 дня от начала лечения. Следует помнить, что риск артериальной гипотензии увеличивается:
Особенно тяжелая артериальная гипотензия наблюдается у больных с высокоренинной формой ХСН с высоким содержанием циркулирующего ангиотензина II. Для этой формы заболевания характерны низкое пульсовое АД (меньше 20 мм рт. ст.), высокое ЦВД (шейные вены набухают в вертикальном положении пациента), признаки гипоперфузии периферических органов (холодные на ощупь, бледно-цианотические конечности) и гипонатриемия (меньше 130 ммоль/л), развивающаяся при длительном употреблении мочегонных средств. В этих случаях, как правило, наблюдаются выраженная систолическая дисфункция с критическим снижением сердечного выброса и ФВ, высокое давление наполнения желудочков, выраженный отечный синдром, рефрактерный к действию сердечных гликозидов, мочегонных и вазодилататоров. Единственным эффективным и патогенетически оправданным средством лечения высокоренинной формы ХСН являются ингибиторы АПФ. Однако быстрая гемодинамическая разгрузка сердца, наступающая после назначения ингибиторов АПФ в первые 1–2 дня лечения, может сопровождаться еще большим, хотя и временным, снижением СИ и выраженной артериальной гипотензией.
Ухудшение функции почек у некоторых больных ХСН (около 1,5%) на фоне лечения ингибиторами АПФ связано со свойством этих препаратов снижать уровень фильтрационного давления в клубочках вследствие значительного уменьшения тонуса выносящих артериол клубочков. Этот эффект усугубляется в связи с тем, что большинство ингибиторов АПФ выводится из организма исключительно почками. Это свойство ингибиторов АПФ используется при лечении больных сахарным диабетом и диабетической нефропатией, у которых изначально внутриклубочковое фильтрационное давление повышено. Однако в других случаях, когда скорость клубочковой фильтрации снижена менее 30 мл/ч, на фоне приема ингибиторов АПФ может увеличиваться протеинурия и азотемия. Особенно значительные нарушения функции почек, вплоть до развития тяжелой почечной недостаточности, возможны при выраженных стенозах почечных артерий, у которых по понятным причинам уровень исходного фильтрационного давления и скорость фильтрации очень низкие. Риск ухудшения функции почек возрастает также у лиц старше 70 лет, у пациентов с низкими значениями ФВ и СИ и при одновременном приеме диуретиков.
Следует подчеркнуть, что начальные стадии ХПН с уровнем креатинина не выше 265 мкмоль/л и систолическим давлением больше 90 мм рт. ст. не являются абсолютным противопоказанием для лечения ингибиторами АПФ. Ангионевротический отекявляется редким, но наиболее грозным осложнением лечения ингибиторами АПФ. Он возникает в результате аллергической реакции, в основе которой лежит высокая концентрация брадикинина, сопровождающая лечение данными препаратами (см. выше). При развитии отека языка, гортани, глотки следует немедленно ввести адреналин и прекратить прием ингибиторов АПФ. Гиперкалиемия может развиться при применении любых ингибиторов АПФ, вызывающих, как известно, задержку ионов К+ в организме. Это следует учитывать при выборе диуретической терапии, если она применяется в комбинации с ингибиторами АПФ. Прием ингибиторов АПФ нельзя сочетать с применением калийсберегающих диуретиков (триампур, верошпирон) или препаратов калия. Риск развития гиперкалиемии возрастает у больных ХСН старческого возраста в связи со снижением у них функции почек, а также при сахарном диабете, гиперальдостеронизме и применении НПВС. Сухой кашельявляется самым частым побочным эффектом лечения ингибиторами АПФ. Он появляется обычно через несколько недель от начала лечения. Кашель при приеме этих препаратов обусловлен высоким уровнем брадикинина, субстанции Р и простагландинов, которые, воздействуя, в частности, на кининовые рецепторы, богато представленные в легких, вызывают кашлевой рефлекс. Нередко упорный сухой кашель является причиной отмены ингибиторов АПФ. Применение ингибиторов АПФ При лечении больных ХСН ингибиторами АПФ следует придерживаться некоторых общих принципов, рекомендованных Европейским обществом кардиологов (1997). 1. Отменить диуретики, как минимум, за 24 ч до применения ингибитора АПФ. 2. В течение 2–3-х часов после первого приема ингибиторов АПФ необходимо врачебное наблюдение (контроль АД, риск возникновения ангионевротического отека гортани и др.). 3. Лечение ингибиторами АПФ следует начинать с минимальной дозы препарата. 4. На начальном этапе лечения или при увеличении дозы препарата через 3–5 дней следует контролировать функцию почек (креатинин сыворотки крови, относительная плотность мочи, диурез и др. показатели) и содержание электролитов крови (К+, Nа+). В дальнейшем контроль проводится каждые 3 и 6 мес. 5. Прием ингибиторов АПФ нельзя сочетать с применением калийсберегающих диуретиков, препаратов калия и НПВС. Следует учитывать также рекомендации, приведенные выше. В табл. 2.11. представлены ориентировочные начальные и поддерживающие дозы наиболее часто используемых в России ингибиторов АПФ. Таблица 2.11 Начальная и поддерживающая дозы ингибиторов АПФ при лечении больных с хронической сердечной недостаточностью
Противопоказания Применение ингибиторов АПФ противопоказано при следующих состояниях. 1. Беременность. 2. Индивидуальная непереносимость препарата. 3. Двусторонний или выраженный односторонний стеноз почечных артерий. 4. Выраженная исходная артериальная гипотензия (САД ниже 85–90 мм рт. ст.). 5. Выраженное снижение функции почек с азотемией. 6. Аортальный стеноз, митральный стеноз, ГКМП (обструктивный вариант).
Диуретики Диуретики — это ЛС, которые оказывают избирательное действие на почки, вследствие чего угнетается реабсорбция Nа+ и/или воды в канальцах и усиливается диурез. Диуретики издавна применяются для лечения больных ХСН. Их эффективность при сердечной декомпенсации связана главным образом с уменьшением ОЦК, снижением ОПСС и притока крови к сердцу и, следовательно, величины пред- и постнагрузки. Таким образом, под влиянием диуретиков происходит преимущественно гемодинамическая разгрузка сердца. Диуретики следует рассматривать как симптоматическое средство, которое целесообразно использовать только при наличии клинических признаков избыточной задержки жидкости в организме или для профилактики отечного синдрома после его устранения. К сожалению, большинство мочегонных препаратов, несмотря на клиническую эффективность и незбежность их применения у многих больных ХСН с застоем крови в легких и отечным синдромом, оказывают значительное влияние на активность нейрогуморальных систем, ответственных за прогрессирование ХСН (см. выше). Речь идет о рефлекторном увеличении под действием диуретиков активности ренина, повышении уровня ангиотензина II, концентрации альдостерона и катехоламинов. Такая рефлекторная реакция связана главным образом со снижением под влиянием диуретиков ОЦК. Поэтому диуретические ЛС, по меньшей мере, не следует применять у больных ХСН в качестве монотерапии; во всех случаях их целесообразно сочетать с ингибиторами АПФ, b-адреноблокаторами или сердечными гликозидами. Механизм действия В зависимости от локализации и механизма действия различают 4 группы диуретиков (рис. 2.39). 1. Диуретики, действующие на проксимальные извитые канальцы нефрона (ингибиторы карбоангидразы и осмотические диуретики).
Поиск по сайту: |
 Запомните
Основными условиями для проведения физической реабилитации больных ХСН являются: стабильное состояние больных и отсутствие признаков обострения основного заболевания (например, ИБС); отсутствие признаков обострения СН, в частности прогрессирующей левожелудочковой недостаточности или выраженного отечного синдрома; неукоснительное выполнение больным рекомендаций по приему ЛС; периодический контроль за основными гемодинамическими показателями и ЭКГ; выполнение больными ХСН физических упражнений не должно сопровождаться ухудшением самочувствия больного и ощущением большего, чем обычно, утомления.
Запомните
Основными условиями для проведения физической реабилитации больных ХСН являются: стабильное состояние больных и отсутствие признаков обострения основного заболевания (например, ИБС); отсутствие признаков обострения СН, в частности прогрессирующей левожелудочковой недостаточности или выраженного отечного синдрома; неукоснительное выполнение больным рекомендаций по приему ЛС; периодический контроль за основными гемодинамическими показателями и ЭКГ; выполнение больными ХСН физических упражнений не должно сопровождаться ухудшением самочувствия больного и ощущением большего, чем обычно, утомления.