|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Определение подлинностиСтр 1 из 2Следующая ⇒
Производные пиримидина 5 часов
Пиримидин – 6-ти членный гетероцикл с двумя атомами азота в положениях 1,3

N В основе хим структуры ЛС данной группы лежит 2,4,6 триоксо производное пиримидина или барбитуровая кислота
мочевина молоновая кислота O Сама барбитуровая кислота не обладает лечебным действием. Барбитураты - производные барбитуровой кислоты, у которых атомы водорода метиленовой группы в положении 5 замещены на радикалы, для них характерна имидо-имидольная или лактим-лактамная таутомерия, обуславливающая кислотный характер этих соединений. Общая характеристика производных барбитуровой кислоты.
O
Barbitalum Барбитал (Веронал)
C2H5
5,5 диэтилбарбитуровая кислота
Barbitalum-natrium Барбитал-натрий (Мединал)
C2H5
5,5 диэтилбарбитурат натрия
Benzonnalum Бензонал (Бензобарбитал)
1 бензоил 5 этил 5 фенил барбитуровая кислота
Aethaminalum – nanrium Этаминал натрий (Нембутал)
5 этил 5 (2 амил)-барбитурат натрия
Phenobarbitalum Фенобарбитал (Люминал)
5 этил 5 фенил барбитуровая кислота
Свойства. Барбитураты – белые кристаллические порошки без запаха. Барбитураты-кислоты не растворимы в воде и растворимы в этаноле, барбитураты-соли легко растворимы в воде и мало в этаноле.
Химические свойства: Барбитураты обладают кислотными свойствами за счет имидо-имидозольной таутомерии
O O
OH Диссоциируют как кислоты в присутствии –ОН ионов и проявляют свойства одноосновных кислот, поэтому образуют соли с едкими щелочами и солями тяжелых металлов. Определение подлинности 1. Общие реакции 1.1. С CuSO4 в присутствии KHCO3, K2CO3 комплексные соединения различной окраски:
1.2. (ГФ)Все препараты с Co(NO)3 в присутствии CaCl2 дают комплекс Со-Са-Na сине-фиолетового цвета
1.3. С AgNO3 в присутствии Na2CO3 или буры образование однозамещенных растворимых в воде и двузамещенных нерастворимых в воде солей серебра.
O O
ONa OAg растворим в воде не растворим в воде Эта реакция используется для количественного определения барбитуратов 2. (не ГФ) Реакция сплавления с едкими щелочами. Все барбитураты при сплавлении с едкими щелочами полностью разлагаются с образованием производных уксусной кислоты, аммиака, карбоната натрия.
O Растворение плава: Na2CO3 + НС1 = NaCl + H2O + CO2
R1 R1 характерный запах
Поиск по сайту: |

 N
N
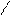
 O барбитуровая кислота – циклический уреид
O барбитуровая кислота – циклический уреид

 NH—C H продукт конденсации мочевины и 2-х
NH—C H продукт конденсации мочевины и 2-х
 О=С C основной молоновой кислоты
О=С C основной молоновой кислоты
 NH—C H
NH—C H
 O O
O O

 NH2 НООС HN H
NH2 НООС HN H


 О=С + СН2 O=
О=С + СН2 O=
 NH2 НООС HN H
NH2 НООС HN H

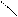


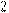


 -CH-CH2-CH2-CH3
CH3
-CH-CH2-CH2-CH3
CH3

 -C-C6H5
O
-C-C6H5
O


 НN O
НN O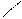 C2H5
C2H5 O=
O=
 НN O
НN O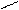


 НN O
НN O



 —С—N C2H5
—С—N C2H5

 O=
O=
 HN O
HN O
 CH—СН2—СН2—СН3
CH—СН2—СН2—СН3