 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Сильные электролиты. Активность электролитов ⇐ ПредыдущаяСтр 3 из 3
Сильные электролиты в растворе полностью распадаются на ионы. Уравнение процесса электролитической диссоциации сильного электролита записывается с указанием его практической необратимости: приводится лишь одна стрелка HNO3 → H+ + N Так как количество ионов в растворах сильных электролитов велико, а расстояние между ними малы, наблюдается сильное электростатическое взаимодействие между ионами противоположного знака. Вследствие этого растворы сильных электролитов ведут себя так, как будто число частиц в растворе меньше их реального количества, а все свойства раствора электролита, зависящие от концентрации ионов, проявляются так, как если бы число ионов в растворе было бы меньше, чем это соответствует полной концентрации электролита. Поэтому во все законы, описывающие сильные электролиты, входит не концентрация вещества, а его активность. Под активностью иона понимают ту эффективную, условную концентрацию его, соответственно которой он действует при химических реакциях. Активность иона а равна его концентрации с, умноженной на коэффициент активности f: a = f∙ c. В разбавленных растворах взаимодействие между ионами мало и f = 1, следовательно, a = c, (то есть активность совпадает с концентрацией). В концентрированных растворах взаимодействие между ионами значительно, f меньше единицы и a меньше с. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации Рассмотрим в свете ТЭД свойства веществ, которые в водном растворе проявляют свойства электролитов. Кислоты Для кислот характерны следующие общие свойства: а) способность взаимодействовать с основаниями с образованием солей; б) способность изменять цвета индикаторов, в частности, вызывать красную окраску лакмуса; в) кислый вкус. При диссоциации любой кислоты образуются ионы водорода. Поэтому все свойства, которые являются общими для водных растворов кислот, мы должны объяснить присутствием гидратированных ионов водорода. Это они вызывают красный цвет лакмуса, сообщают кислотам кислый вкус и т.д. С устранением ионов водорода, например, при нейтрализации, исчезают и кислотные свойства. Поэтому теория электролитической диссоциации определяет кислоты как электролиты, диссоциирующие в растворах с образованием ионов водорода. Одноосновные кислоты диссоциируют в одну ступень: HNO3 Многоосновные кислоты диссоциируют ступенчато:
При составлении уравнений диссоциации следует помнить, что суммы зарядов в левой и правой частях уравнения должны быть одинаковыми.
Основания Для водных растворов оснований характерны следующие общие свойства: А) Способность взаимодействовать с кислотами с образованием солей; б) способность изменять цвет индикаторов иначе, чем их изменяют кислоты (например, они вызывают синюю окраску лакмуса); в) своеобразный «мыльный» вкус Поскольку общими для всех растворов оснований является присутствие в них гидроксид-ионов, то ясно, что носителем основных свойств является гидроксид-ион. Поэтому с точки зрения теории электролитической диссоциации основания – это электролиты, диссоциирующие в растворах с отщеплением гидроксид-ионов. Однокислотные основания диссоциируют в одну ступень:
Многокислотные основания диссоциируют ступенчато:
Существуют гидроксиды, способные вступать во взаимодействие и образовывать соли не только с кислотами, но и с основаниями. К таким гидроксидам принадлежит гидроксид цинка. При взаимодействии его, например, с соляной кислотой получается хлорид цинка
А при взаимодействии с гидроксидом натрия при недостатке воды – цинкат натрия:
Гидроксиды, обладающие этим свойством, называются амфотерными гидроксидами или амфотерными амфолитами – амфолитами. К таким гидроксидам кроме гидроксида цинка относятся гидроксиды алюминия, хрома(III),железа(III), меди(II), олова(IV) и другие. Явление амфотерности объясняется тем, что в молекулах амфотерных электролитов прочность связи между металлом и кислородом незначительно отличается от прочности связи между кислородом и водородом. Диссоциация таких молекул, возможна, следовательно, по местам обеих связей. Например, диссоциацию гидроксида цинка можно выразить схемой:
Таким образом, в растворе амфотерного электролита существует сложное равновесие, в котором участвуют продукты диссоциации как по типу кислоты, так и по типу основания.
Соли Таких ионов, которые были бы общими для водных растворов всех солей, нет, поэтому соли и не обладают общими свойствами. С точки зрения ТЭД соли – это электролиты, которые при растворении в воде диссоциируют на катионы металла и анионы кислотного остатка. Средние соли диссоциируют в одну ступень
Кислые соли диссоциируют ступенчато: сначала отщепляются все катионы металла, а затем – по одному – ионы водорода.
Основные соли диссоциируют ступенчато: сначала отщепляются все ионы кислотных остатков, а затем – по одному – гидроксид-ионы.
Таким образом, при составлении уравнений диссоциации следует помнить: катионы водорода и гидроксид-ионы диссоциируют ступенчато, а катионы металлов и анионы кислотных остатков – сразу, в одну ступень.
Поиск по сайту: |
 , направленная от молекулярной формы электролита к его ионам, например:
, направленная от молекулярной формы электролита к его ионам, например: .
. H+ + N
H+ + N  ;
; ;
;
 .
. ,
, .
. ,
, .
.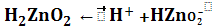






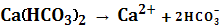

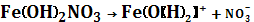 ,
, ,
, .
.