 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Методы изучения ДНК. Секвенирование генома. Современная геномика
МЕТОДЫ ИЗУЧЕНИЯ ДНК 1. Для выделения ДНК из гомогената тканей удаляют фрагменты клеточных органелл и мембран с помощью центрифугирования. Белки, разрушенные
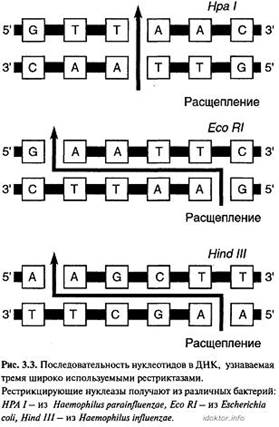
Для фрагментирования используют рестриктазы — ферменты, выделяемые из бактерий. У бактерий эти ферменты участвуют в уничтожении чужеродных для них ДНК. Рестриктазы «узнают» специфические последовательности из 4—6 нуклеотидов (сайты рестрикции), которые встречаются в ДНК человека. Известно множество различных рестриктаз, причем каждая из них «узнает» свой сайт рестрикции (рис. 3.3). С помощью набора рестриктаз можно разрезать молекулу ДНК на фрагменты желаемой длины. Например, для изучения первичной структуры удобны фрагменты размером около 300 нуклеотидных пар н.п . Следовательно, цельную молекулу ДНК в 150 000 000 н.п. нужно разрезать на 500 000 фрагментов и каждый из фрагментов изучать отдельно. Полимеразная цепная реакция (ПЦР). Для проведения некоторых исследований необходимо большое количество хорошо очищенной высокомолекулярной ДНК. Метод ПЦР дает возможность избирательно синтезировать in vitro небольшие участки ДНК и получить за 3—4 ч несколько миллионов копий исследуемого фрагмента. Объектами для выделения ДНК могут быть кровь, биоптат ткани, слюна, моча, околоплодные воды и т.д. Подробно этот метод и его применение в ДНК-диагностике будут рассмотрены в теме 3.10. Гибридизация. Для изучения видовой специфичности нуклеиновых кислот применяют метод гибридизации. Он основан на способности ДНК к денатурации при нагревании (80—90 °С) и ренативации при последующем охлаждении. Возможно использование метода для проведения гибридизации ДНК-ДНК и ДНК-РНК. Методом гибридизации можно установить сходство и различия первичной структуры разных образцов нуклеиновых кислот. Секвенирование генома. Секвенирование генома здорового человека в большинстве случаев не способно предсказать развитие у него в будущем тех или иных заболеваний. Результаты этой работы были представлены на Ежегодной встрече Американской Ассоциации по исследованию рака (Association for Cancer Research), а также опубликованы в журнале Science Translational Medicine. Полное секвенирование генома представляет собой «каталогизирование» всех генов, полученных человеком от обоих родителей, и их проверку на наличие повреждений ДНК, которые могли бы повысить восприимчивость человека к раку и иным заболеваниям. Поскольку стоимость секвенирования генома постоянно снижается (в настоящее время цена процедуры составляет 1-3 тысячи долларов США), многие здоровые люди начали задумываться над тем, чтобы пройти такое обследование и определить для себя риск развития того или иного заболевания. Однако исследователи из Центра по изучению рака Johns Hopkins Kimmel призывают их не торопиться. Выводы ученых вовсе не означают, что секвенирование генома не имеет никакой медицинской ценности. «Во-первых, секвенирование генома остается лучшим средством для предсказания „семейных“ заболеваний, таких как рак и некоторые другие, — говорит профессор онкологии Берт Фогельштайн (Bert Vogelstein). — Во-вторых, детальное изучение генома индивидуума помогает лучше понять механизм уже протекающего у него заболевания и точнее подобрать для него индивидуальную терапию. Однако в случае со здоровым человеком геном перестает быть надежным предсказателем». Исследователи проследили развитие 24 заболеваний у более чем 50 тысяч близнецов из 5 стран, прошедших процедуру секвенирования генома. Результаты показали, что в случае 23 заболеваний анализ генома дал отрицательный результат и отнес риск их развития к разряду «низкий». Однако, по словам профессора Фогельштайна, это вовсе не означает, что данное заболевание у данного человека не разовьется. «Это означает всего лишь, что его персональный риск немного ниже, чем средний риск по популяции, который может быть очень существенным, — говорит исследователь. — Таким образом, даже негативный результат не гарантирует отсутствия заболевания в будущем». При этом риск 4 из 24 заболеваний— заболевания сердца у мужчин, аутоиммунный тиреоидит, диабет I типа и болезнь Альцгеймера — устойчиво определялся в ¾ случаев, что позволяет назвать секвенирование генома достаточно надежным средством определения предрасположенности к этим болезням. Современная геномика. Длительное время геномом называли гаплоидный набор хромосом. Накопление сведений об информационной роли внехромосомной ДНК изменило определение термина «геном». В настоящее время он означает полный состав ДНК клетки, т.е. совокупность всех генов и межгенных участков. Можно считать, что геном - полный набор инструкций для формирования и функционирования индивида. Общие принципы построения геномов и их структурно-функциональную организацию изучает геномика, которая проводит секвенирование, картирование и идентификацию функций генов и внегенных элементов. Методы геномики направлены на расшифровку новых закономерностей биологических систем и процессов. Геномика человека является основой молекулярной медицины и имеет важнейшее значение для разработки методов диагностики, лечения и профилактики наследственных и ненаследственных болезней. Для медицины первостепенное значение имеют исследования в области геномики патогенных микроорганизмов, поскольку они проливают свет на природу инфекционного процесса и создание лекарств, направленных на специфические мишени бактерий. Геномика, несмотря на её «молодой возраст», подразделяется на несколько почти самостоятельных направлений: структурную, функциональную, сравнительную, эволюционную, медицинскую геномику. Структурная геномика изучает последовательность нуклеотидов в геномах, определяет границы и строение генов, межгенных участков и других структурных генетических элементов (промоторов, энхансеров и т.д.), т.е. составляет генетические, физические и транскриптные карты организма. Функциональная геномика. Исследования в области функциональной гено-мики направлены на идентификацию функций каждого гена и участка генома, их взаимодействие в клеточной системе. Очевидно, это будет осуществляться путём изучения белковых ансамблей в разных клетках. Эту область исследований называют протеомикой. Сравнительная геномика изучает сходства и различия в организации геномов разных организмов с целью выяснения общих закономерностей их строения и функционирования. Эволюционная геномика объясняет пути эволюции геномов, происхождение генетического полиморфизма и биоразнообразия, роль горизонтального переноса генов. Эволюционный подход к изучению генома человека позволяет проследить за длительностью формирования комплексов генов, отдельных хромосом, стабильностью его частей, недавно обнаруженными элементами «непостоянства» генома, процессом расообразования, эволюцией наследственной патологии. Медицинская геномика решает прикладные вопросы клинической и профилактической медицины на основе знания геномов человека и патогенных организмов (например, диагностика наследственных болезней, генотерапия, причины вирулентности болезнетворных микроорганизмов и т.д.). Все шаги эволюции живой природы, несомненно, должны были закрепляться в информационной системе ДНК (а для некоторых существ - в РНК), а также в организации её в клетке для выполнения консервативной функции сохранения наследственности и противоположной функции - поддержания изменчивости. Такое представление о формировании генома каждого вида наиболее обоснованно. Применительно к геному человека можно сказать, что эволюция человека - это эволюция генома. Такое представление подтверждается теперь многочисленными молекулярно-генетическими исследованиями, поскольку стало возможным сопоставление геномов разных видов млекопитающих, в том числе человекообразных обезьян, а также в пределах вида Homo sapiens геномов разных рас, этносов, популяций человека и отдельных индивидов. Организация генома каждого эукариотического вида представляет собой последовательную иерархию элементов: нуклеотидов, кодонов, доменов, генов с межгенными участками, сложных генов, плеч хромосом, хромосом, гаплоидного набора вместе с внехромосомной и внеядерной ДНК. В эволюционном преобразовании генома каждый из этих иерархических уровней мог вести себя совершенно дискретно (изменяясь, комбинируясь с другими и т.д.). Наши представления о геноме человека - обширная область генетики человека, включающая по меньшей мере понятия «инвентаризации» генов, групп сцепления, картирования генов (локализация), секвенирования всей ДНК (генов, их мутаций и хромосом в целом), мейотических преобразований, функционирования отдельных генов и их взаимодействий, интеграции структуры и функции генома в целом. На решении всех этих вопросов была сосредоточена обширная многолетняя международная программа «Геном человека» (с 1990 по 2000 г.). Главным направлением работ были последовательное секвенирование участков генома и их «состыковка». Успешные разработки в этой области придали программе клинико-генетический аспект. Клинические приложения сведений о геноме человека
Систематическое изучение генома человека фактически началось с применения менделевского анализа наследственных признаков человека (начало XX века). Генеалогический метод вошел тогда в широкую практику, и шаг за шагом стал накапливаться материал по «инвентаризации» дискретных наследственных признаков человека, но этот процесс постепенно замедлялся (за 50 лет было открыто не более 400 менделирующих признаков и 4 группы сцепления), возможности клинико-генеалогического метода в чистом виде были исчерпаны. Бурный прогресс цитогенетики человека, биохимической генетики и особенно генетики соматических клеток в 60-х годах в комплексе с генеалогическим подходом поставил изучение генома человека на новые теоретические основы и высокий методический уровень. Обнаружение новых менделирующих признаков человека стало быстро продвигаться, особенно на биохимическом и иммунологическом уровне, появились возможности изучения сцепления и локализации генов. Особый импульс изучению генома человека придали молекулярно-генетические методы, или технология генной инженерии (70-е годы). Процесс познания генома углубился до выделения гена в чистом виде и его секвенирования. В отличие от классической, в новой генетике изменился подход к анализу генов. В классической генетике последовательность была следующей: идентификация менделирующего признака —> локализация гена в хромосоме (или группе сцепления) —> первичный продукт гена —> ген. В современной генетике стал возможным и обратный подход: выделение гена —> секвенирование —> первичный продукт, в связи с чем был введён новый термин для определения такого направления исследований: «обратная генетика» или «генетика наоборот». Продолжаются совершенствование молекулярно-генетических методов и, что не менее важно, их автоматизация. В США и Великобритании были разработаны и внедрены автоматические приборы по секвенированию геномов. Их назвали геномотронами. В них осуществляется до 100 000 полимеразных реакций в час. Это означает, что в течение недели может быть просеквенирован участок (или участки) длиной в несколько миллионов пар нуклеотидов. Большую роль в расшифровке генома человека играют вычислительная техника и информационные системы. Благодаря им решаются вопросы накопления информации (базы данных) из разных источников, хранения её и оперативного использования исследователями из разных стран.
Поиск по сайту: |
 2. Молекула ДНК среднего размера содержит 150 000 000 нуклеотидных пар и имеет длину 4 см.
2. Молекула ДНК среднего размера содержит 150 000 000 нуклеотидных пар и имеет длину 4 см.