 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Выполнение экспериментаСтр 1 из 2Следующая ⇒
ЛАБОРАТОРНАЯ РАБОТА № 3 Тема: ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ ЭЛЕКТРОПРОВОДНОСТИ ПРИ БЕСКОНЕЧНОМ РАЗБАВЛЕНИИ СИЛЬНОГО ЭЛЕКТРОЛИТА. Литература:Лекция №6; [1]: С. 283-300. Цель: приобретение навыков измерения электропроводности раствора при помощи цифрового кондуктометра, определение молярной электропроводности при бесконечном разбавлении сильного электролита кондуктометрическим методом. Реактивы и оборудование: Кондуктометр цифровой с электродом, раствор NaCl0,1 моль/л; вода дистиллированная, бюретка объемом 50 мл, воронка, стакан объемом 50 мл (под бюретку), пронумерованные мерные колбы объемом 100 мл с пробкой — 5 штук, высокий стакан объемом 150 мл для измерений электропроводности. Теоретические основы Электропроводность растворов электролитов, то есть способность проводить электрический ток, обусловлена направленным движением ионов под воздействием электрического поля. В проводниках первого рода (металлах) заряд переносится электронами. Растворы электролитов – проводники второго рода, носителями электричества в них служат анионы и катионы. Электропроводность раствора электролита зависит от природы электролита и растворителя, концентрации, температуры и некоторых других факторов. Удельная электропроводность раствора электролита – это электрическая проводимость объема раствора, заключенного между двумя параллельными электродами, имеющими единичную площадь и удаленными друг от друга на расстояние, равное единице длины. Единицы измерения удельной электрической проводимости c в СИ [Ом–1∙м– 1] или [См∙м–1]; на практике также используют внесистемные единицы [Ом–1∙см–1] или [См∙см–1]. Сложный характер зависимости c от C требует использования других количественных способов выражения электропроводности. В электрохимии наряду с удельной электропроводностью χ используют величину молярной электропроводности l, равную электрической проводимости такого объема раствора, который содержит 1 моль растворенного вещества, при условии, что раствор заключен между двумя параллельными электродами, удаленными друг от друга на расстояние, равное единице длины. В единицах СИ молярная электропроводность λ имеет размерность [Ом−1∙м2∙моль−1] =[См∙м2∙моль−1]. На практике концентрацию раствора часто выражают не в [моль/м3], а в [моль/л], а χ − во внесистемных единицах [Ом−1∙см−1] = [См∙см−1], поэтому при вычислениях следует внимательно относиться к размерности λ в зависимости от используемых единиц c и С. Молярная электрическая проводимость тоже зависит от концентрации раствора.С увеличением концентрации молярная электрическая проводимость λ уменьшается в растворах сильных и для слабых электролитов вследствие возрастания взаимного влияния ионов или изменения степени диссоциации с разбавлением. Для сравнения электропроводности электролитов используют значение молярной электропроводности бесконечно разбавленного раствора l¥, то есть раствора такой концентрации, когда взаимным влиянием ионов можно пренебречь, именно эти значения приводятся в справочных таблицах для характеристики электропроводности электролита. Прямое определение l¥ невозможно,поскольку нельзя на практике приготовить «бесконечно разбавленный раствор». Найти l¥ из графической зависимости l от С (при бесконечном разбавлении С → 0, значение λ максимально) также довольно сложно из-за практических трудностей экстраполяции кривой к оси ординат. Экстраполяция упрощается, если зависимость будет иметь линейный характер.
Рис. 6. Зависимость молярной электрической проводимости растворов сильных электролитов от концентрации
Эмпирически линейная зависимость зависимости l от С обнаружена немецким физиком Кольраушем и известна как «закон квадратного корня»:
В координатах l −
Рис. 7. Зависимость молярной электрической проводимости растворов сильных электролитов от Выполнение эксперимента 1. Для экспериментального определения молярной электропроводности при бесконечном разбавлении потребуются 6 растворов одного и того же вещества разной концентрации. Каждого раствора необходимо не менее 100 мл. Используя в качестве исходного (№1) 0,1 М раствор, вычисляют, сколько мл этого раствора нужно разбавить водой до 100 мл, чтобы получить рабочие растворы для измерения электропроводности с концентрациями а)№2 — 0,08 М; б) №3 — 0,06 М; в) №4 — 0,04 М; г) №5 — 0,02М; д) №6 — 0,01 М.
2. Приготавливают по 100 мл каждого раствора, отмеряя необходимые объемы 0,1 М исходного раствора при помощи бюретки в мерную колбу объемом 100 мл с нужным номером и доводя объем до метки на колбе дистиллированной водой. Приемы работы с бюреткой и мерной колбой описаны в лабораторной работе №1. 3. Измеряют удельную электропроводность χ каждого раствора. Для измерения раствор переливают в высокой стакан. Для измерения удельной электропроводности растворов в лабораториях кафедры химии используется цифровой кондуктометр «Hanna» с четырьмя диапазонами измерений. Этот прибор снабжен измерительным датчиком, который защищен съемным пластиковым кожухом.
При работе с кондуктометром важно, чтобы датчик был погружен в раствор до нужного уровня (отверстия в пластиковом кожухе датчика полностью погружаются в раствор). Включение и выключение кондуктометра производится кнопкой «ON/OFF». Необходимый диапазон измерений выбирают, нажимая последовательно кнопки «199,9 μS/см» , «1999 μS/см», «19,99 mS/см», «199.9 mS/см». Обозначения mS/см и μS/см означают, что отображаемая на дисплее величина χ имеет размерность «мили См∙см–1» или «микро См∙см–1». Смену диапазона производят, если на дисплее отображается «1» (зашкаливание), если цифровые значения быстро меняются («прыгают»), или измеренное значение содержит мало значащих цифр. В данном приборе постоянная ячейки заложена в память, поэтому при измерениях на дисплее высвечивается действительное значение удельной электропроводности изучаемого раствора. Для работы с растворами NaCl рекомендуется использовать диапазон измерений «19,99 mS/см». При переходе к измерению удельной электропроводности раствора NaCl другой концентрации электрод, не снимая кожуха, следует промокнуть фильтровальной бумагой снаружи и снизу.
Поиск по сайту: |

 .
. это уравнение выражается прямой, отсекающей на оси ординат отрезок, равный l¥. Постоянная h, зависящая от природы растворителя и электролита, может быть найдена из тангенса угла наклона прямой. Это уравнение используется для экспериментального определения l¥ сильных электролитов в области невысоких концентраций.
это уравнение выражается прямой, отсекающей на оси ординат отрезок, равный l¥. Постоянная h, зависящая от природы растворителя и электролита, может быть найдена из тангенса угла наклона прямой. Это уравнение используется для экспериментального определения l¥ сильных электролитов в области невысоких концентраций.
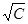 .
.