|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Примеры решения задач
1. Для реакции первого порядка А → В определите время, за которое реагирует 90% вещества А, если половина его реагирует за 115,5мин. Период полураспада для реакции первого порядка
Время разложения 90% вещества А:
2. Установлено, что разложение оксида азота (4) 2NO2г → 2NOг + О2г является реакцией второго порядка. Определите константу скорости реакции, если в начальный момент времени в реакторе находился только NO2 с концентрацией 2моль/л, а через 15 мин концентрация кислорода составляла 0,5моль/л.
Для образования 0,5моль/л О2 должно было разложиться 1 моль/л NO2. Следовательно через 15 мин концентрация NO2 составляла 1 моль/л. Для реакции 2-ого порядка
для условий задачи
3. Кинетика реакции 1-ого порядка в газовой фазе А → 2В изучались манометрическим методом. Начальное состояние системы – вещество А под давлением 40кПа. Через 11,5 мин общее давление увеличилось до 60 кПа. Рассчитайте константу скорости реакции.
Допустим, из 1 моля вещества А разлагается х холей. Общая сумма молей 1 – х + 2х = 1 + х; в единицах давления х = 20кПа (приращение давления); 1-х=20кПа.
4. Для некоторой реакции первого порядка установлено, что время полупревращения составляет 6*103с при 323К и 9*102 при 353К. Рассчитайте энергию активизации этой реакции и температурный коэффициент константы скорости.
Рассчитываем константы скорости при двух температурах.
Энергия активации равна:
Температурный коэффициент константы скорости:
5. В реакции второго порядка А + В → продукты. Начальные концентрации веществ А и В равны соответственно 2,0моль/л и 3,0 моль/л. Константа скорости реакции равна 3,2.10-4л/моль.с Рассчитайте время τ, за которое прореагирует половина вещества А.
К моменту времени τ прореагирует по 1 моль вещества А и В. Конечные концентрации [А]=1моль/л, [В]=2моль/л.
6. В параллельных реакциях первого порядка
Выход вещества В равен 63%, а время превращения на 1/3 равно 7 мин.
Выход вещества В равен 63%, следовательно выход D равен 37% Отношение выходов В и D равно отношению конечных концентраций этих веществ, следовательно, отношению констант скоростей образования В и D.
откуда к1=0,037мин-1; к2=0,021мин-1
7. В последовательности радиоактивных превращения
периоды полураспада соответственно равны 15 суток для Вычислите константы скорости К1 и К2. Определите время, через которое количество образующегося актиния достигаем максимума. Радиоактивные превращения отвечают кинетике реакции первого порядка, поэтому
1. В настоящее время уран содержит изотопы 238U (99,28%) и 235U (0,72%) с периодом полураспада соответственно 4,5*109 и 7,1*108 лет. Определить, каким было естественное содержание каждого изотопа урана в момент образования Земли 4,5 млрд. лет назад. 2.Константа скорости реакции первого порядка А→В+С к=5*10-5с-1 Определить концентрацию вещества А и В через 1 и 5час,если начальная концентрация А составляла 0,2моль/л.
3.Разложение ацетона протекает по реакции первого порядка в соответствии с уравнением СН3СОСН → С2Н4 + СО +Н2 (все вещества газы) При температуре 802К за 390с давление изменилось от начального Р0=41,6кПа до Р=54,4кПа. Рассчитайте константу скорости реакции.
4.В присутствии концентрированной серной кислоты муравьиная кислота разлагается с образованием оксида углерода (2) НСООН→СО+Н2О По нижеприведенным экспериментальным данным определите порядок и константу скорости реакции:
5.Скорость реакции ацетона с иодом СН3СОСН3+J2→CН3СОСН2J+НJ прямо пропорциональна концентрации ацетона и не зависит от концентрации иода. За какое время прореагирует 80% ацетон, если при той же температуре концетрация его уменьшается вдвое за 30мин.?
6.Разложение азотного ангидрида N2O5→N2O4 + ½О2 является реакцией первого порядка. Константы скорости для 293 и 323К равны соответственно 1,72*10-5 и 7,59*10-4с-1. Рассчитайте время, за которое подвергнется разложению 99% исходного вещества при указанных температурах, и определите энергию активации этой реакции.
7.Изучая кинетику реакции ClСН2СН2Cl→CН2=СН2+Cl2 При 3600С получили следующие данные:
Проверьте, действительно ли это реакция первого порядка. Рассчитайте её константу скорости.
8. В реакции первого порядка концентрация исходного вещества составляла 1,345моль/м3 через 5 мин после начала реакции и 1,209 моль/м3 через 10мин после её начала. Определите константу скорости и начальную концентрацию исходного вещества.
9.термический распад паров ацетона является реакцией первого порядка СН3СОСН3→СН2 = СН2 + СО +Н2 и протекает при 5040С с константой скорости 4,27*10-4с-1. Определите, за какое время в реакторе останется 20% первоначального количества исходного вещества. Как изменится давление в ректоре, если в начальный момент продукты реакции отсутствовали?
10. При исследовании методом меченых атомов в организм животных вводят соль, содержащую радиоактивный изотоп 24Na с периодом полураспада 14,8 ч. Вычислите время, в течение которого активность радиоактивного изотопа в организме животного уменьшится до 0,1 начальной дозы.
11. В настоящее время уран содержит изотопы 238U(99,28%) и 235U(0,72%) с периодом полураспада соответственно 4,5*109 и 7,1*108лет. Определите, каким было естественное содержание каждого изотопа урана в момент образования Земли 4,5млрд. лет назад.
12. Изучение кинетики реакции изомеризации циклопропана в пропен проводили при 5000С в газовой фазе, измеряя конечное давление циклопропана в зависимости от времени при различных начальных давлениях. Были получены следующие результаты:
Определите порядок реакции и константу скорости в этих условиях.
13.Разложение иодоводорода НJг→½Н2г+½J2г на золотой поверхности - реакция нулевого порядка. За 1с концентрация иодоводорода уменьшилась с 0,335моль до 0,285моль Рассчитайте константу скорости и период полураспада при начальной концентрации иодоводорода 0,400моль.
14. Установлено, что жидкофазная реакция А→В+С имеет нулевой порядок. Через какой промежуток времени прореагирует половина исходного вещества, если известны (А0)=1м и константа скорости 0,03моль*л-1*мин-1? Через какое время вещество А израсходуется практически полностью?
15.Увеличение начальной концентрации реактива вдвое вызывает удвоение времени полупревращения реакции. Определите порядок реакции по данному компоненту.
16.Константа скорости для реакции первого порядка SO2Cl2 = SO2 + Cl2 равна 2,2*10-5 с-1 при 3200 С. Какой процент SO2Cl2 разложится при выдерживании его в течение 2ч при этой температуре?
17.Константа скорости реакции первого порядка 2N2O5г =2NO2г + O2г при 250С равна 3,38*10-5 с-1 . Чему равен период полураспада N2O5? Чему будет равно давление в системе через 10мин, если начальное давление было равно 500 торр?
18.Реакция первого порядка с константой скорости 8,95*10-4с-1 протекает с выделением теплоты. Общее количество выделившейся теплоты при 96%-ном превращении некоторого количества вещества составляет 41,8кДж. Определите, какое количество теплоты выделится через 10; 20; 30; 40 и 50 минут с момента начала реакции.
1.В реакции второго порядка А+В→С за 1 час концентрации веществ А и В уменьшились по сравнению с начальной (А)0 = (В)0 =0,2моль/л на 30%. Рассчитайте константу скорости реакции.
2.Реакция разложения иодоводорода 2НJ=Н2+J2 протекает с константой скорости 1,85*10-4 л/(моль*с). Рассчитать время, за которое прореагирует 99% исходного вещества, если начальная концентрация была равна 1моль/л; 0,1моль/л.
3.Вычислите порядок реакции и константу скорости, если при изменении начальной концентрации с 0,502моль/л до 1,007моль/л время полупревращения уменьшается с 51 до 26с.
4.Установлено, что реакция 2-го порядка (1 реагент) завершается на 75% за 92мин при исходной концентрации реагента 0,24моля. Какое время потребуется, чтобы при тех же условиях концентрация реагента достигла 0,16моля.
5.Реакция второго порядка А+В→С+Д проводится в растворе с начальными концентрациями (А)0=0,060моль/л и (В)0=0,080моль/л. Через 60мин концентрация вещества А уменьшилась до 0,025моль/л. Рассчитать константу скорости и период полупревращения веществ А и В.
6.Реакция второго порядка 2А→В протекает в газовой фазе. Начальное давление равно Р0 (В отсутствует). Через какое время давление уменьшится в 1,5раза по сравнению с первоначальным? Какова степень протекания реакции к этому времени. Константа скорости равна 1(время в минутах).
7.Газовая реакция 2А→В имеет второй порядок по А и протекает при постоянном объёме и температура с периодом полураспада 1 час. Если начальное давление равно 1атм, то каковы парциальные давления А и В и общее давление через 1час. 2часа, 3часа после начала реакции?
8.Для реакции разложения ацетальдегида при температуре 5180С найдено, что время полупревращения равно 410с при начальном давлении 363торр и Т=880с при начальном давлении 169торр. Установите порядок реакции.
9.Для реакции второго порядка 2А→Р константа скорости равна 3,5*10-4 л*моль-1 *с-1. Вычислите время, в течение которого концентрация А уменьшится с 0,260 до 0,011м.
10.Какая из реакций – первого или второго порядка – закончится быстрее, если начальные концентрации веществ равны 1моль/л и константы скорости, выраженные через моль/л и с, равны 1 (За конец реакции принять степень конверсии, равную 99%).
11.При изучении реакции омыления эфира СН3СООН3 + NаОН→СН3СООNа + СН3ОН установлено, что порядок реакции по каждому из исходных веществ равен 1, константа скорости равна 0,137л*моль-1 *с-1 при 250С. Определите время, в течение которого прореагирует 5% эфира: а)если начальная концентрация в реакционной смеси одинаковы и равны 0,1моль; в)если начальная концентрация эфира равна С01 =0,1моль, С02 =0,2моль.
12.Константа скорости реакции второго порядка СН3СООС2Н5 + NаОН → СН3СООNа + С2Н5ОН равна 5,4л-моль*с. Сколько эфира прореагирует за 10мин при (СН3СООС2Н5)=(NаОН)=0,02моль/л. Какова должна быть исходная концентрация эфира и спирта, чтобы за это же время прореагировало 98% эфира?
13.Реакция СН3СН2NО2 + ОН- → СН3СНNО2- + Н2О имеет второй порядок и константу скорости к=39,1л*моль-1 *мин-1 ,при 00С.Был приготовлен раствор, содержащий 0,004моль нитроэтана и 0,005моль NаОН. Через какое время прореагирует 90% нитроэтана?
14. Щелочной гидролиз этилацетата-реакция второго порядка с константой скорости к=0,084л*млоль-1*с-1 при 250С. Взят 1л 0,05М раствора этилацетата. Какое время понадобится для образования 1,15г этанола при исходной концентрации щелочи: а)(ОН-)0 =0,05М; в)(ОН-)0=0,1М?
15.Реакция второго порядка А+В→Р проводится в растворе с начальными концентрациями (А)0=0,050моль*л-1 и (В) =0,080моль*л-1. Через 1час концентрация вещества А уменьшилась до 0,02 моль*л-1. Рассчитать константу скорости и период распада обоих веществ.
16.Реакция А+В→С имеет первый порядок по веществам А и В. Смешаны равные объемы растворов А и В с концентрацией, равной 1моль*л-1. Через 1час прореагировала половина веществ А.Какое количество веществ А останется в растворе через 2часа?
17. Гидролиз бутилацетата в щелочной среде - реакция второго порядка. Константа скорости её при некоторой температуре равна 3,93л*моль-1*мин-1. За сколько времени прореагирует 70% эфира, если: 1)исходные концентрации эфира и NаОН одинаковы и равны 0,05моль*л-1; 2)исходная концентрация эфира равна 0,05моль*л-1, щелочи 0,1моль*л-1.
18. Изучение кинетики окислительно – восстановительной реакции НJО3 + Н2SO4 = НJO2 + Н2SО4 показало, что её скорость пропорциональна концентрации каждого из исходных веществ в первой степени. Экспериментально получено, что при смешивании реагентов с равными концентрациями концентрация каждого из них равнялась 0,25моль/л через 40с и 0,2моль/л через 60с после начала опыта. Рассчитать начальную концентрацию исходных веществ и константу скорости.
19.Реакция второго порядка 2А=В протекает за 600с на 25%. Сколько времени необходимо, чтобы реакция прошла на 50% при той же температуре?
Поиск по сайту: |
 , откуда
, откуда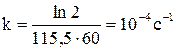


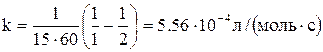

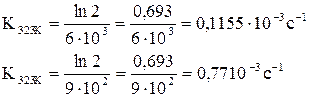

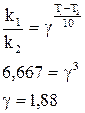


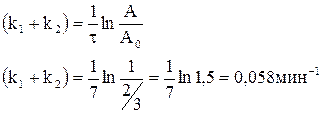
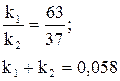
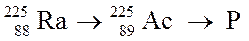
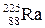 и 10 суток для
и 10 суток для