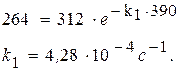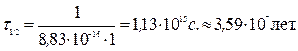|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Молекулы комплекс реакции ⇐ ПредыдущаяСтр 2 из 2
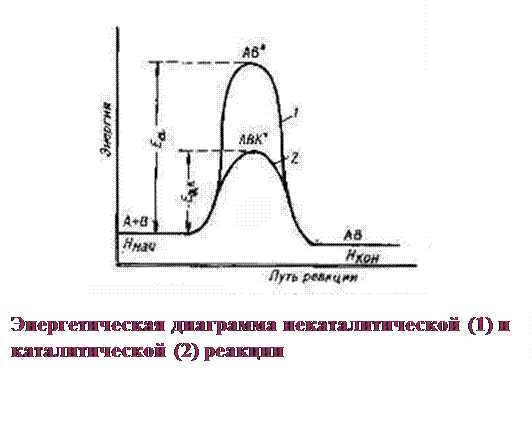
Для образования активированного комплекса необходима энергия Еа:
Если ΔrHпрямой реакции > 0 Þ
Положительный катализ – процесс, ускоряющий реакцию Отрицательный катализ– процесс, замедляющий реакцию Kt – ингибиторы (Сl- - ингибитор коррозии) Антидетонатор Pb(C2H5)4 – замедляет взрывную реакцию топлива Автокатализ – kt - один из продуктов реакции FeO + H2 = Fe + H2O Fe - kt
Ферменты являются полимерами (белками) или комплексами полимеров с низкомолекулярными соединениями. Размеры их превышают размеры ионов и молекул в растворах, поэтому ферменты иногда называют микрогетерогенными катализаторами. Механизм их действия включает образование комплекса активный центр фермента - реагент по типу «замок-ключ».
Особенности kt: ■ kt – участвует в образовании промежуточных нестойких соединений, а в конце выделяется в химически неизменном виде. ■ S(ЕIа +EIIа) промежуточных стадий < Еа неkt реакции
б) Sа- промежуточное соединение- более «рыхлое»- менее упорядоченное- значит более активное. ■ небольшие количества kt - резко ускоряют процесс
MgO СН3СНО + Н2 ■ kt – не изменяют DrН и DrG: DrG0неkt = DrG0kt DrG0 = -RTlnKp Þ не влияет на равновесие, только ускоряет его достижение, т.к. в одинаковое число раз изменяет как J прямой р-ции так и Jобр.р-ции (К =kпрям /kобр)
Гомогенный катализ: 1.скорость прямо пропорционально зависит от конц.kt; 2.дешевые, доступные; 3.остаются в реакционной среде – надо выделять – плохо Гетерогенный катализ ◘ Действие kt зависит от способа получения kt:
K2O, Al2O3 – для Fe – kt: N2 + 3H2 = 2NH3
H2S, C2H2, O2 – для Pt-kt: 2SO2 + O2 = 2SO3 ◘ уменьшение поверхности kt – надо чистить Þудорожание
1. Задача. За 1 с в единице реакционного пространства образуется по трем реакциям 66 г СО2, 68 г Н2S и 51 г NН3. Скорость образования какого из веществ больше? Решение. Найдем количество вещества (ν) в молях каждого из продуктов реакции
где R – реакционное пространство, Dν – изменение количества вещества за время Dτ; получаем, что скорость образования NН3 больше, чем скорости образования Н2S и СО2.
2. Задача. Во сколько раз изменится скорость реакции 2СО(г) + О2(г) ® 2СО2(г) при увеличении давления в системе в 10 раз? Температура системы поддерживается постоянной.
Решение. Предположим, что рассматриваемая реакция является элементарной, т. е. для нее справедлив закон действующих масс:
υ = k×с2(СО)×с(О2). Учитывая, что концентрация и парциальное давление связаны прямо пропорциональной зависимостью рi = сi×RT, получим, что υ= k×р2(СО)×р(О2).
После увеличения давления в системе в 10 раз парциальное давление каждого из реагентов возрастет тоже в 10 раз, т. е.
Отсюда υ¢/υ = 1000. Следовательно, скорость реакции увеличится в 1000 раз.
3. Задача. В реакции А ® В + С с общим порядком, равным единице, константа скорости k1 = 5×10-5 с-1. Определите концентрацию веществ А и В и скорость реакции через 1 час и через 5 часов, если начальная концентрация А составляла 0,2 моль/л.
Решение. Для реакции 1-го порядка справедливо уравнение где с – текущая концентрация вещества в момент времени τ, с0 – начальная концентрация, k – константа скорости, τ – время.
Через 1 час
Через 5 часов
Концентрация вещества В находится по стехиометрическому соотношению веществ А и В. Из уравнения реакции следует, что концентрация вещества В возрастает на ту же величину, на какую убывает концентрация А, т. к. из 1 моль А получается 1 моль В.
Поэтому через 1 час
Через 5 часов
Рассчитаем скорость реакции по уравнению:
Через 1 час
Через 5 часов
4. Задача. Для реакции первого порядка А ® 2В определите время, за которое прореагирует 90 % вещества А. Константа скорости реакции k1 = 10-4 с-1.
Решение. После превращения 90 % вещества А его концентрация составит 10% от начальной концентрации, т. е. 0,1 с0.
Из уравнения получим, что
Следовательно, τ = ln 10/k1 = 23026 с = 6,4 ч.
5. Задача. При изучении кинетики термического разложения ацетона, являющегося реакцией первого порядка, в соответствии с уравнением: СН3СОСН3(г) ® С2Н4(г) + СО(г) + Н2(г) получены следующие экспериментальные данные при Т = 802 К: давление в реакторе изменилось от начального р0 = 312 мм. рт. ст. до 408 мм. рт. ст. за 390 с. Рассчитайте константу скорости реакции.
Решение. Все вещества в системе находятся в газообразном состоянии, и, учитывая условия проведения опыта, предполагаем, что они подчиняются законам идеальных газов. Следовательно, концентрация и парциальное давление газа связаны зависимостью pi=ci×R×T или
Отсюда, для реакции I-го порядка
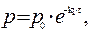
и
Если р0 – это начальное давление ацетона в реакционном сосуде, то для решения задачи необходимо определить парциальное давление этого вещества к моменту времени, когда общее давление
Из стехиометрии реакции видно, что 1 моль ацетона, распадаясь, образует 3 моль газа. Из закона Авогадро следует, что при уменьшении парциального давления ацетона на Dр сумма парциальных давлений образовавшихся газов составит 3Dр. Таким образом, можно записать P = p0 – Dp + 3×Dp или 408 = 312 + 2×Dp, Dp = 48 мм рт.ст. Следовательно, парциальное давление ацетона через 390 с после начала опыта составило 312 – 48 = 264 (мм. рт. ст.).
После подстановки в уравнение получим:
6. Задача. При температуре 100°С константа скорости реакции второго порядка 2НI(г) ® Н2(г) + I2(г) равна 8,83×10-16 л/(моль×с). Определите время полупревращения йодистого водорода, если начальная концентрация его равна 1 моль/л.
Решение. Воспользуемся уравнением для реакции второго порядка:
Далее рассчитаем
7. В реакции второго порядка А + В ® D за 1 час концентрации веществ А и В уменьшились по сравнению с начальной с0 А = с0 В = 0,2 моль/л на 30 %. Определите константу скорости и скорость реакции в начальный момент времени и через час после начала реакции.
Решение. Концентрации веществ А и В за 1 час уменьшились на 0,3×с0 = 0,06 моль/л. Отсюда, через час концентрации составят сА = сВ = 0,2 – 0,06 = 0,14 (моль/л).
Для реакции II-го порядка
Отсюда
8. Рассчитайте изменение константы скорости реакции, имеющей энергию активации 191 кДж/моль, при увеличении температуры от 330 до 400 К.
Решение. Зависимость константы скорости реакции от температуры определяется уравнением Аррениуса
или
Логарифм отношения констант скоростей реакции при температурах Т2 и Т1 соответственно равен
где R = 8,31 Дж/(моль×К) – универсальняая газовая постоянная.
Следовательно,
9. Реакция разложения пероксида водорода 2Н2О2 ® 2Н2О + О2 в кислой среде и в присутствии ионов брома в качестве катализатора протекает по следующему механизму: k1 Н2О2 + Вr- + Н+ ® НВrО + Н2О (1) k2 Н2О2 + НВrО ® Н2О + Вr- + Н+ + О2 (2) .
Поиск по сайту: |
 Þ
Þ
 Þ kэндотерм. с температурой быстрее kэкзотерм реакции.
Þ kэндотерм. с температурой быстрее kэкзотерм реакции.


 H2O2 HI-kt H2O + 1/2O2 (H+, OH- -самые активные kt)
H2O2 HI-kt H2O + 1/2O2 (H+, OH- -самые активные kt)
 H2O2 Pt-kt H2O + 1/2O2
H2O2 Pt-kt H2O + 1/2O2

 k =Z×e-Ea/RT×eSa/R Þ скорость , если а) Еа
k =Z×e-Ea/RT×eSa/R Þ скорость , если а) Еа ■ избирательность kt: Al2O3 С2Н4 + Н2О
■ избирательность kt: Al2O3 С2Н4 + Н2О
 С2Н5ОН H3PO4 С2Н5ОС2Н5+ Н2О
С2Н5ОН H3PO4 С2Н5ОС2Н5+ Н2О

 актCu(NO3)2 to Cu + 2NO2 + O2
актCu(NO3)2 to Cu + 2NO2 + O2 Cu-kt
Cu-kt неакт. Cu(NO3)2 электролиз Cu + O2 +HNO3
неакт. Cu(NO3)2 электролиз Cu + O2 +HNO3 ◘ присутствия других веществ: активаторы - активность kt
◘ присутствия других веществ: активаторы - активность kt каталит.яды - активность kt
каталит.яды - активность kt


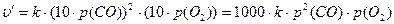

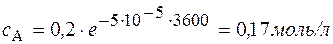









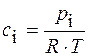
 составило 408 мм. рт. ст.
составило 408 мм. рт. ст.