 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Властивості кристалівСтр 1 из 2Следующая ⇒
Лекція 10 . Властивості твердих тіл та рідин. План. 1. Властивості кристалів. Види кристалів. Теплоємність кристалів. 2. Властивості рідин. Поверхневий натяг. 3. Явища змочування та незмочування. Капілярні явища. 4. Фазові рівноваги та фазові переходи. 5. Потрійна точка. Діаграма станів.
Властивості кристалів.
Істинно тверді тіла — кристали. У межах всього тіла дальній порядок розташування молекул зберігається тільки в монокристалах (умовна модель монокристала — кубики, складені в один великий куб (а). У природі монокристали зустрічаються рідко, частіше зустрічаються полікристали. Вони складаються з великого числа маленьких монокристалів (кристалітів, зерен), розташованих один відносно одного невпорядковано (модель полікристала — куб, що розсипався (б). Умовне зображення дальнього порядку в монокристалі — решітка, у вузлах якої — атоми, зображувані як матеріальні точки. Найменше утворення, багаторазовим повторенням якого можна одержати монокристал — елементарна комірка. Є 7 основних типів комірок: кубічна (залізо, алюміній, кам'яна сіль), гексагональна (цинк, графіт), тетрагональна, ромбічна і ін.
Основною властивістю монокристалів є анізотропія. Анізотропієюназивається залежність більшості фізичних властивостей речовини (за винятком теплоємності й густини)від напрямку в кристалі. Якщо провести по дві прямі через центри найближчих атомів у різних напрямах (1, 2, 3, 4), то відстані між кожною парою прямих (а отже й між відповідними атомними площинами) виявляться різними: d1 і d2 максимальні, d3 - менша й d4 - мінімальна . Отже, міцність монокристала була б Полікристали, на відміну від монокристалів, ізотропні (кожен кристаліт анізотропний, але розташовуються кристаліти невпорядковано). Через невпорядкованість кристалітів анізотропні властивості полікристалів не проявляються. Окремим різновидом є рідкі кристали. Рідкими кристаллами називають рідини з дальнім порядком розташування молекул. Нараховується їх більше 3000, багато які з них біологічного походження (мозок людини має складну рідкокристалічну структуру; дезоксирибонуклеїнова кислота — рідкий кристал з величезних молекул). На відміну від твердих кристалів, у рідких кристалах дальній порядок спостерігається тільки в одному напрямі. · смектичні кристали, молекули яких паралельні одна одній і розташовані шарами (як у розчині мила у воді);
· нематичні кристали, менш упорядковані (їх молекули паралельні, але довільно зсунуті одна відносно одної вздовж своїх осей); · холестеричні (за структурою схожі на нематичні, але їх молекули закручені перпендикулярно своїм довгим осям). · Застосування: цифрова індикація (в тому числі і в годинниках), перетворення інфрачервоного випромінювання у видиме; одержання плоских екранів моніторів; термоіндикація). Аморфними називають численні речовини (різні смоли, віск, скло, пластмаси), які мають лише ближній порядок. За структурою такі речовини — рідини (дуже в'язкі). Розташування частинок у вузлах кристалічної решітки відповідає мінімальному значенню їх потенціальної енергії. Коливальний рух частинок у кристалі може відбуватися в трьох взаємно перпендикулярних напрямках, тому кожна частинка має три ступені вільності, яким відповідає енергія kT . Для одного моля хімічно простих речовин вираз для внутрішньої енергії має вигляд:
Приріст внутрішньої енергії при зміні температури на один градус дорівнює теплоємності при сталому об’ємі, тобто Оскільки об’єми твердих тіл незначно змінюються при нагріванні, то Таким чином, справедливий емпіричний закон Дюлонга і Пті::
Поиск по сайту: |
 Більшість твердих тіл в природі мають кристалічну будову, тобто частинки речовини (атоми або молекули) розташовані в просторі впорядковано або, як кажуть, знаходяться у вузлах кристалічної решітки, біля яких здійснюють коливальний рух. Саме з цим пов’язані такі властивості твердих тіл, як наявність та збереження форми та об’єму, опір деформаціям, тощо.
Більшість твердих тіл в природі мають кристалічну будову, тобто частинки речовини (атоми або молекули) розташовані в просторі впорядковано або, як кажуть, знаходяться у вузлах кристалічної решітки, біля яких здійснюють коливальний рух. Саме з цим пов’язані такі властивості твердих тіл, як наявність та збереження форми та об’єму, опір деформаціям, тощо.
 мінімальною при дії на нього в напрямах 1 і 2.
мінімальною при дії на нього в напрямах 1 і 2. Розрізняють:
Розрізняють:
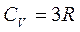 .
. і говорять тільки про теплоємність твердих тіл.
і говорять тільки про теплоємність твердих тіл.