|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
D. Реакція з натрій гідроксидомСтр 1 из 2Следующая ⇒
Визначення доброякісності лікарських препаратів, які належать до амінокарбонових кислот аліфатичного ряду та солей аліфатичних карбонових кислот.
Лікарські засоби з групи амінокислот Амінокислоти –похідні карбонових кислот, які містять у молекулі одну або більшее аміногруп –NH2. Вони є біфункціональними сполуками, тому що містять у молекулах, з одного боку, карбоксильні групи –СООН (кислотні групи), а з іншого – аміногрупи –NH2 (основні групи). Амінокислоти належать до найважливіших біологічно активних речовин. α-Амінокислоти є структурними одиницями білків і широко поширені в природі. З білкових гідролізатів отримано понад 20 α-амінокислот загальної формули:
З них незамінними (вітагенними) є 10 амінокислот: аргінін, валін, гістидин, ізолейцин, лейцин, лізин, метіонін, треонін, триптофан, фенілаланін. Вони не можуть синтезуватися в організмі, а мають надходити з їжею. Білки як одна з трьох основних складових продуктів харчування (разом з жирами і вуглеводами) під дією ферментів гідролізують до окремих амінокислот, з яких в організмі синтезуються специфічні для даного органу білки. Найбільшеа кількість певних амінокислот міститься у таких білкових речовинах: 1) глутамінова кислота – гліадин пшениці (45,7 %), b-лактоглобулін, міозин (білок м'язів), казеїн (білок молока); 2) цистеїн – білки покривних тканин (ріг, вовна, волосся, пір’я); 3) цистин (його відновленням одержують цистеїн) – ріг (6–7 %), волосся людини (13–14 %); 4) метіонін – β-лактоглобулін, міозин, казеїн.
Застосування амінокислот Застосування амінокислот у медичній практиці грунтується на їх участі в азотистому обміні, у синтезі необхідних для нормального функціонування організму білків, пептидів, ферментів, гормонів, утворенні кінцевих продуктів азотистого обміну (амоніак, сечовина) і інших життєво важливих процесах. Це „основной будівельний матеріал” специфічних тканинних білків та інших ендогенних сполук. Замінні амінокислоти синтезуються в організмі людини, а незамінні (10 амінокислот) організмом не синтезуються і надходять з їжею. Деякі амінокислоти, крім того, відіграють роль нейромедіаторів (глютамінова, аспарагінова кислоти, гліцин, таурин, g-аміномасляна кислота й ін.). Фенілаланін і тирозин є попередниками в синтезі дофаміну, норадреналіну; триптофан – серотоніну; гістидин – гістаміну. Похідними амінокислот є енкефаліни, ендорфіни, динорфіни та інші нейропептиди, а також звільняючі фактори (рилізинг-фактори) гіпоталамусу, гормони гіпофізу і т.д. Деякі амінокислоти застосовуються самостійно як лікарські засоби. Глютамінову кислотузастосовують для лікування захворювань центральної нервової системи: епілепсії, психозів, реактивних станів; у педіатрії – при затримці психічного розвитку, церебральних паралічах, хворобі Дауна. Застосовують також для попередження нейротоксичних явищ, які можуть виникати при застосуванні ізоніазиду, ізонікотинової кислоти та ін.
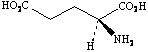
Кислота глутамінова ДФУ Acidum glutaminicum GLUTAMIC ACID
C5H9NO4 М.м. = 147,1 г/моль Хімічна назва: (S)-2-амінопентан-1,5-дикарбонова кислота; a-аміноглутарова кислота. Кислота глютамінова містить не менше 98,5 % і не більше 100,5 %(S)-2-амінопентан-1,5-дикарбонової кислоти, у перерахунку на суху речовину. Одержання 1. Гідроліз білкових речовин з наступним виділенням глутамінової кислоти з гідролізатів хроматографічним методом. ДФУ. Виробництво.Якщо субстанція одержана в результаті процесу, що включає стадії ферментації, вона має витримувати випробування статті“Продукти ферментації”. 2.Синтетичний метод, оснований на конденсації ацетиламіномалонового естеру з акрилонітрилом.
Ідентифікація Перша ідентифікація: А, В. Друга ідентифікація: А, С,D.А. Поляриметрія. Вимірювання питомого оптичного обертання. Від +30,5 ° до +32,5 °, у перерахунку на суху речовину. Визначення проводять, використовуючи розчин S (субстанцію розчиняють при слабкому нагріванні в 1 М розчині кислоти хлоридної). В. ІЧ-спектроскопія.ІЧ-спектр поглинання субстанції, одержаний у дисках, має відповідати спектру ФСЗ кислоти глютамінової.С. Тонкошарова хроматографія. На хроматограмі випробовуваного розчину має виявлятися основна пляма на рівні основної плями на хроматограмі розчину порівняння, яка відповідає їй за розміром і забарвленням. D. Реакція з натрій гідроксидом 0,2 г субстанції при слабкому нагріванні розчиняють у 2 мл 1 М розчину кислоти хлоридної Р HCl, додають 0,1 мл розчину фенолфталеїну Р, від3,0 до 3,5 мл 1 М розчину натрій гідроксиду NaOH до появи рожевого забарвлення. Потім додають суміш 3 мл розчину формальдегіду Р НСНО, 3 млводи, вільної від СО2, Р и 0,1 мл розчину фенолфталеїну Р, до якої попередньо додали 1 М розчин натрій гідроксиду NaOH до появи рожевогозабарвлення; розчин знебарвлюється. До одержаного розчину додають 1 М розчин натрій гідроксиду NaOH до появи рожевого забарвлення. Загальний обьем витраченого 1 М розчину натрій гідроксиду NaOH має бути від 4,0 мл до 4,7 мл.
Поиск по сайту: |