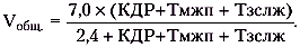|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Осмотр, пальпация и перкуссия сердца
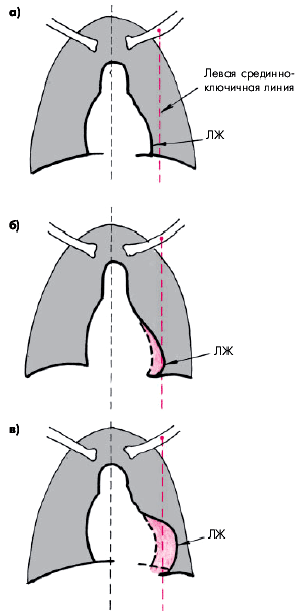
У больных ГБ I стадии (повышение АД без признаков поражения органов-мишеней) верхушечный толчок и границы сердца не изменены. II стадия ГБ характеризуется, как известно, концентрической гипертрофией миокарда ЛЖ, что приводит к увеличению силы верхушечного толчка. Его локализация, так же как и левая граница относительной тупости сердца, длительное время могут почти не изменяться, пока не наступит дилатация ЛЖ (эксцентрическая гипертрофия ЛЖ). Прогрессирующее снижение сократительной способности миокарда ЛЖ сопровождается значительной (миогенной) дилатацией ЛЖ. Усиленный верхушечный толчок при этом смещается влево и становится разлитым. Влево смещается и левая граница относительной тупости сердца (рис. 7.11).
При перкуссии иногда выявляется расширение сосудистого пучка во II межреберье, обусловленное расширением аорты, ее удлинением и разворотом (см. рис. 7.11), характерными для многих больных ГБ. Аускультация сердца I тон сердца. Громкость I тона у больных ГБ может изменяться по-разному. В начальных стадиях заболевания (ГБ I–II стадии), особенно когда преобладает гиперкинетический синдром, характеризующийся достаточно высокой скоростью сокращения миокарда ЛЖ, а его гипертрофия выражена умеренно, как правило, выявляется громкий I тон сердца (рис. 7.12, а). По мере прогрессирующего увеличения массы миокарда ЛЖ, развития кардиосклероза и дилатации ЛЖ происходит заметное уменьшение громкости I тона, обусловленное снижением скорости изоволюмического сокращения ЛЖ. В составе I тона начинают преобладать низкочастотные компоненты, и он приобретает характер “глухого” тона (рис. 7.12, б). Еще большее ослабление I тона может быть обусловлено возникновением относительной недостаточности митрального клапана, которая развивается на поздних стадиях болезни на фоне дилатации ЛЖ и его систолической дисфункции (рис. 7.12, в).
II тон сердца акцентуирован на аорте, что объясняется прежде всего высоким уровнем АД. Интересно, что у больных ГБ II–III стадии над аортой может определяться акцент II тона даже при нормализации АД. Это объясняется уплотнением аорты (в том числе за счет сопутствующего атеросклероза) и улучшением условий проводимости II тона на поверхность грудной клетки (рис. 7.13).
Дополнительные тоны. Гипертрофия миокарда ЛЖ закономерно сопровождается более или менее выраженной его диастолической дисфункцией. Последняя, как известно, сопровождается значительным замедлением раннего наполнения желудочка (в фазу быстрого наполнения) и увеличением предсердной фракции наполнения (систола предсердий). В результате в начальных стадиях болезни на верхушке нередко выслушивается патологический IV тон сердца (рис. 7.14).
В дальнейшем, когда происходит снижение сократимости ЛЖ, развивается его систолическая дисфункция и выраженная дилатация ЛЖ, на верхушке определяется патологический III тон сердца, связанный с объемной перегрузкой желудочка, характерной для поздних стадий болезни. Шум. Функциональный систолический шум на аорте (II межреберье справа от грудины) — довольно частая находка у больных ГБ. Шум связан с расширением аорты и наличием атеросклеротических изменений в ее стенке, что сопровождается турбулентным током крови. Если систолический шум выслушивается на верхушке, проводится в левую подмышечную область и сочетается с ослаблением I тона и увеличением размеров ЛП, речь идет об относительной недостаточности митрального клапана. Артериальный пульс Артериальный пульс при ГБ хорошего наполнения и напряжения, большой, твердый. Нередко выявляется тахикардия и аритмии. Артериальное давление Измерение АД имеет ключевое значение в диагностике ГБ. Общепризнанным и наиболее распространенным во всем мире способом неинвазивного определения АД является аускультативный метод, предложенный в 1905 г. Н.С. Коротковым (рис. 7.15). Чаще всего этим методом определяют АД на плечевой артерии. Измерение проводят в положении пациента лежа на спине или сидя, после 10–15-минутного отдыха. Во время измерения АД исследуемый должен лежать или сидеть спокойно, без напряжения, не разговаривать.
Манжета сфигмоманометра плотно накладывается на обнаженное плечо пациента. В локтевой ямке находят пульсирующую плечевую артерию и прикладывают к этому месту стетофонендоскоп. После этого нагнетают воздух в манжету несколько выше (примерно на 20 мм рт. ст.) момента полного прекращения кровотока в плечевой (или лучевой) артерии, а затем медленно (со скоростью 2 мм рт. ст. в сек) выпускают воздух, снижая давление в манжете и, тем самым, уменьшая сжатие артерии. При снижении давления в манжетке чуть ниже систолического артерия начинает пропускать в систолу первые пульсовые волны. В связи с этим эластичная артериальная стенка приходит в короткое колебательное движение, что сопровождается звуковыми явлениями (рис. 7.16). Появление начальных негромких тонов (I фаза) соответствует систолическому АД.
Дальнейшее снижение давления в манжетке приводит к тому, что артерия с каждой пульсовой волной раскрывается все больше. При этом появляются короткие систолические компрессионные шумы (II фаза), которые в дальнейшем сменяются громкими тонами (III фаза). Когда же давление в манжете снизится до уровня диастолического АД в плечевой артерии, последняя становится полностью проходимой для крови не только в систолу, но и в диастолу. В этот момент колебания артериальной стенки минимальны, и тоны резко ослабевают (IV фаза). Дальнейшее снижение давления в манжете ведет к полному исчезновению звуков Короткова (V фаза). Считается, что именно этот момент соответствует уровню диастолического АД. Определение АД описанным способом производят три раза с интервалом 2–3 мин. Целесообразно определять АД на обеих руках.
Следует помнить, что максимальное и минимальное АД при измерении по Н.С.Короткову не совсем совпадают с истинным внутрисосудистым давлением. Во многом такое несоответствие объясняется методикой искусственного пережатия артерии манжетой. Измеренное таким образом систолическое АД оказывается чуть выше “истинного” или бокового систолического давления, которое существует при свободном течении крови в сосуде. Диастолическое давление, определяемое по полному исчезновению звуков Короткова, также не совпадает с моментом, когда давление в сосуде соответствует истинному диастолическому. Тем не менее аускультативный метод определения АД занимает ведущее место в диагностике артериальных гипертензий. Иногда при измерении АД аускультативным методом врач может встретиться с двумя важными в практическом отношении феноменами: “бесконечным тоном Короткова” и с феноменом “аускультативного провала”. “Бесконечный тон Короткова” можно зарегистрировать при значительном повышении сердечного выброса или/и снижении тонуса сосудов (рис. 7.17, а). В этих случаях тоны Короткова определяются даже после снижения давления в манжетке ниже диастолического (иногда до нуля). “Бесконечный тон Короткова” обусловлен либо значительным ростом пульсового АД (недостаточность клапана аорты), либо резким падением тонуса сосудов, особенно при увеличенном сердечном выбросе (тиреотоксикоз, нейроциркуляторная дистония), и лучше выявляется на фоне физической нагрузки. Понятно, что ни в том, ни в другом случае истинное диастолическое АД в сосуде не равно нулю. Феномен “аускультативного провала”. Иногда у больных с артериальной гипертензией при измерении АД аускультативным методом после появления первых тонов, соответствующих систолическому АД, звуки Короткова полностью исчезают, а затем, после снижения давления в манжетке еще на 20–30 мм рт. ст., появляются вновь (рис. 7.17, б). Считают, что феномен “аускультативного провала” связан с резким повышением тонуса периферических артерий. Возможность его появления следует учитывать при измерении АД у больных с артериальной гипертензией, ориентируясь при первоначальном нагнетании воздуха в манжетку не на аускультативную картину, а на исчезновение пульсации на лучевой или плечевой артерии (пальпаторно). В противном случае возможно ошибочное определение значений систолического АД на 20–30 мм рт. ст. ниже, чем истинное систолическое АД. Следует добавить, что больным с сосудистой патологией (например, при облитерирующем атеросклерозе артерий нижних конечностей) показано обязательное определение АД на обеих верхних и нижних конечностях. Для этого АД определяют не только на плечевых, но и на бедренных артериях в положении пациента на животе. Звуки Короткова выслушивают при этом в подколенных ямках.
Исследование других органов Аускультация легких дает возможность своевременно диагностировать одно из тяжелейших осложнений ГБ — острую левожелудочковую недостаточность. Напомним, что при сердечной астме (интерстициальном отеке легких) на фоне ослабленного везикулярного дыхания выслушивается умеренное количество влажных мелкопузырчатых незвучных хрипов, преимущественно в нижних отделах легких. Иногда можно выслушать единичные сухие хрипы. При альвеолярном отеке легких на фоне ослабленного везикулярного дыхания быстро нарастает количество влажных хрипов — мелко- и среднепузырчатых, а затем и крупнопузырчатых. Хрипы вначале выслушиваются в задненижних отделах легких, постепенно распространяясь по всей поверхности легких сзади и спереди. Исследование почек необходимо, прежде всего, для исключения некоторых симптоматических (почечных) АГ. Метод пальпации почек в некоторых случаях позволяет обнаружить увеличение почек (поликистоз, пиелонефрит, мочекаменная болезнь, осложненная гидронефрозом и др.). Аускультация сосудов почек дает возможность выявить систолический шум в проекции почечных артерий на переднюю брюшную стенку, обусловленный их стенозом, что дает повод для более углубленного исследования больного на предмет реноваскулярной АГ. Исследование органов брюшной полости позволяет получить в основном информацию о наличии признаков застоя в большом круге кровообращения (гепатомегалия, асцит), что все же довольно редко встречается у больных ГБ.
В табл. 7.5 перечислены наиболее важные методы лабораторного и инструментального исследования больных ГБ. Так же как и методы клинического исследования, их применение преследует несколько целей:
Остановимся на некоторых из этих методов. Таблица 7.5 Обязательные и дополнительные диагностические процедуры
В последние годы в кардиологических клиниках все чаще применяют различные автоматические системы длительного мониторного наблюдения за суточными колебаниями уровня АД (рис. 7.18). В них используются разные методы определения давления, основанные либо на регистрации с помощью микрофонов звуковых явлений над областью сдавленного сосуда, либо на оценке изменений местного кровотока, возникающих во время программируемой компрессии и декомпрессии сосуда.
В этих последних случаях изменение кровотока регистрируют с помощью ультразвуковых датчиков, реографических электродов или осциллометрическим или тахоосциллометрическим методом. При этом АД автоматически измеряют через определенные промежутки времени, например, каждые 30 мин. Автоматические мониторинговые системы измерения АД используют для изучения динамики изменений давления в течение длительного времени: 1) с целью уточнения этиологии и патогенеза артериальной гипертензии; 2) при неотложных состояниях для оценки основных показателей гемодинамики; 3) при индивидуальном подборе лекарственных препаратов у больных с артериальными гипертензиями. Следует помнить, что использование мониторинговых систем для измерения АД, основанных на аускультативном или осциллометрическом методах, не рекомендуется при наличии у больных аритмии, в частности, мерцательной аритмии, поскольку значительная вариабельность сердечного выброса делает точное мониторное определение АД весьма затруднительным. Суточный профиль АД оценивается обычно по нескольким количественным показателям (рис.7.19):
При анализе суточного профиля АД следует помнить, что даже у здорового человека в течение суток происходят значительные колебания как систолического, так и диастолического АД. Оно изменяется под влиянием физической нагрузки, психоэмоционального и умственного напряжения, а также в результате существования биологических суточных (циркадных) ритмов. В дневное время наблюдаются два пика более высокого уровня АД: между 9 и 11 ч утра и около 18 ч. В вечернее и ночное время АД снижается, достигая минимума между 2 и 5 ч. Утром вновь наблюдается рост АД. Такой суточный профиль АД может встречаться как у больных с АГ, так и у здоровых пациентов, отличаясь лишь уровнем подъемов АД. Возможны и другие варианты суточного профиля АД. Например, у некоторых больных АГ (в том числе с почечной симптоматической гипертензией) максимальные значения АД регистрируются в вечерние часы суток, а ночное понижение АД слабо выражено. Результаты 24-часового мониторирования АД используются для индивидуального подбора антигипертензивной терапии.
При ЭКГ-исследовании может быть выявлена ценная информация, указывающая на формирование у больного ГБ гипертрофии ЛЖ, наличие рубцовых изменений миокарда, признаков коронарной недостаточности, а также нарушений сердечного ритма и проводимости. Гипертрофия миокарда ЛЖ. Известно, что на начальных стадиях развития гипертрофия может не отражаться на ЭКГ. Однако по мере увеличения массы ЛЖ его электрическая активность все более преобладает над электрической активностью ПЖ, и суммарный результирующий вектор QRS, а также моментные векторы 0,04–0,05 с все больше отклоняются влево и назад, в сторону ЛЖ (рис. 7. 20).
Если в норме амплитуда зубца RV4 превышает амплитуду RV5, 6 (RV4 >= RV5 >= RV6), то при гипертрофии ЛЖ соотношение этих зубцов меняется: при умеренной гипертрофии RV4<= RV5 >RV6, а при выраженной гипертрофии RV4 < RV5 <= RV6. В правых грудных отведениях (V1, 2) отмечается значительное увеличение зубцов S, что обусловлено увеличением проекции вектора 0,04–0,06 с на отрицательные части осей отведений V1 и V2. Обычно чем больше амплитуда RV5, 6, тем глубже становится зубец SV1, 2. Вторым ЭКГ-признаком гипертрофии ЛЖ является поворот сердца вокруг его продольной оси против часовой стрелки (если смотреть со стороны верхушки). МЖП располагается теперь почти перпендикулярно к передней грудной стенке. В связи с этим переходная зона смещается вправо, в отведение V2 (реже V1). Кроме того, в отведениях V5, 6 исчезает отрицательный зубец S и комплекс QRS приобретает форму qR. Этот признак весьма характерен для гипертрофии ЛЖ, причем в грудных отведениях в большинстве случаев наблюдается не плавное, как в норме, уменьшение амплитуды зубцов S от V1 (V2) к V6, а резкий переход от сравнительно глубоких зубцов S в отведениях V1–V3 к почти полному или полному исчезновению S в V4–V6. Замедление проведения электрического импульса по гипертрофированному ЛЖ приводит к увеличению продолжительности интервала внутреннего отклонения в левых грудных отведениях (V5, V6) более 0,05 с. Наконец, выраженная гипертрофия ЛЖ нередко сопровождается нарушением реполяризации желудочков. В левых грудных отведениях (V5, V6) отмечается косонисходящее смещение сегмента RS–Т ниже изоэлектрической линии и инверсия зубца Т, а в правых грудных отведениях (V1, V2) — дискордантный подъем сегмента RS–Т и положительный зубец Т. Изменения ЭКГ в отведениях от конечностей непостоянны. В связи с преобладанием электрической активности ЛЖ (рис. 7.21) вектор 0,04 с отклоняется влево в сторону положительных электродов отведений I и аVL, где и регистрируется высокий зубец R. Наоборот, в отведениях III и аVF увеличивается амплитуда зубца S, что обусловлено проекцией вектора 0,04 с на отрицательные части осей этих отведений. Иными словами, речь идет о смещении электрической оси сердца влево.
Из приведенных количественных электрокардиографических признаков гипертрофии ЛЖ наиболее популярными являются два признака: 1. Индекс Соколова–Лайона: RV5, 6 + SV1,2 >= 35 мм (у пациентов старше 40 лет) и >= 45 мм (у пациентов моложе 40 лет). Специфичность индекса Соколова–Лайона достигает 100%, хотя чувствительность не превышает 22%. 2. Корнельский вольтажный индекс: RaVL + SV3 > 28 мм у мужчин и RaVL + SV3 > 20 мм у женщин. Чувствительность этого индекса несколько выше (42%), чем индекса Соколова–Лайона, а специфичность составляет 96%. На рис. 7.22 приведена электрокардиограмма больного ГБ с признаками гипертрофии ЛЖ. Признаки коронарной недостаточности у больных ГБ лучше всего выявляются с помощью функциональных нагрузочных проб (при отсутствии противопоказаний) и суточного мониторирования ЭКГ по Холтеру (см. выше). Для выявления рубцовых изменений миокарда, а также нарушений ритма и проводимости показано стандартное ЭКГ-исследование в покое и холтеровское мониторирование ЭКГ.
Рентгенография сердца у больных ГБ позволяет оценить степень дилатации ЛЖ, а у пациентов с сердечной недостаточностью — признаки венозного застоя крови в малом круге кровообращения и легочной артериальной гипертензии (см. главу 2). Рентгенологические признаки дилатации ЛЖ лучше выявляются в прямой, левой передней косой и левой боковой проекциях. Важным рентгенологическим признаком расширения ЛЖ является удлинение нижней дуги левого контура сердца в прямой проекции(рис. 7.23). Верхушка сердца при этом смещается влево или влево и вниз и как бы погружается в тень диафрагмы. При значительном смещении верхушки влево угол между сосудистым пучком и контуром ЛЖ становится менее тупым, а “талия” сердца — более подчеркнутой (рис. 7.23, в).
В левой передней косой проекции задний контур тени сердца, образованный ЛЖ, отклоняется еще более кзади,сужая ретрокардиальное пространство и даже частично перекрывая тень позвоночника (рис. 7.24). Выделяют три степени увеличения ЛЖ, выявляемого в левой передней косой проекции (И. Х. Рабкин). I степень — задний контур ЛЖ доходит до края позвоночника (рис. 7.24, а); II степень — задний контур наслаивается на тень позвоночника (рис. 7.24, б); III степень — задний контур значительно наслаивается на тень позвоночника, перекрывая ее (рис. 7.24, в).
На рис. 7.25 приведена рентгенограмма сердца в прямой проекции больного ГБ с признаками умеренной дилатации гипертрофированного ЛЖ.
Использование метода эхокардиографии у больных ГБ дает возможность:
Cпособы эхокардиографического решения некоторых из перечисленных задач были описаны в предыдущих главах. В данном разделе приводится краткое описание методики выявления признаков гипертрофии ЛЖ. Эхокардиографическая диагностика гипертрофии миокарда ЛЖ основана на компьютерном вычислении массы миокарда ЛЖ (ММЛЖ), наиболее точные значения которой могут быть получены только с помощью двухмерной эхокардиографии. На рис. 7.26 схематически показан один из наиболее приемлемых способов вычисления ММЛЖ, рекомендуемый Американской ассоциацией по эхокардиографии. Из левого парастернального доступа получают изображение продольного и поперечного сечений ЛЖ. Поперечный срез регистрируют на уровне папиллярных мышц. Курсором обводят эндокардиальный и эпикардиальный контуры ЛЖ, что достаточно для последующего автоматического измерения и расчета ряда количественных параметров, необходимых для вычисления ММЛЖ. Определяют: 1) А1 и А2 — площади эпикардиального и эндокардиального контуров левого желудочка; 2) t — толщину миокарда ЛЖ; 3) “а” — длинную полуось ЛЖ; 4) “b” — радиус короткой оси ЛЖ; 5) “d” — короткую полуось ЛЖ. ММЛЖ вычисляется автоматически по формулам, которые используются в современных компьютерных программах для автоматического расчета ММЛЖ.
По данным Schiller N.В. с соавт. верхние границы нормальной ММЛЖ достигают 183 г у мужчин и 141 г у женщин, хотя средние значения этого показателя существенно ниже (135 г и 99 г, соответственно). Превышение этих значений ММЛЖ свидетельствует о наличии гипертрофии миокарда ЛЖ. Более точным является расчет так называемого индекса массы миокарда ЛЖ (отношение ММЛЖ к площади поверхности тела), нормальные значения которого колеблются от 94 г/м2 у женщин до 126 г/м2 у мужчин. До настоящего времени в некоторых диагностических центрах используются устаревшие компьютерные программы ультразвуковой диагностики ММЛЖ (по B. Troy), основанные на линейных измерениях по М-модальным одномерным эхокардиограммам толщины МЖП и задней стенки ЛЖ, а также величины КДР (см. рис. 7.27). ММЛЖ рассчитывается как произведение объема миокарда ЛЖ в см3 (Vm) на удельную плотность сердечной мышцы, равную 1,05 г/см3: ММЛЖ= Vm Χ 1,05 г.
Понятно, что объем миокарда ЛЖ (Vm) равен разности общего диастолического объема ЛЖ (Vобщ.) и КДО, рассчитанного по известной формуле L. Teicholz (см.выше): Vm = Vобщ. –КДО. В свою очередь, общий объем ЛЖ определяют по формуле:
Такой способ вычисления ММЛЖ нередко приводит к ошибочным результатам, поскольку для определения объема миокарда используется принцип возведения в третью степень линейного диастолического размера ЛЖ, определяемого в ограниченном участке. Способ B. Troy, таким образом, не учитывает сложной геометрии ЛЖ. Кроме того, толщина миокарда задней стенки желудочка и МЖП далеко не всегда коррелирует с признаками гипертрофии ЛЖ. Так, при дилатации ЛЖ его стенки истончаются, несмотря на наличие существенно увеличенной массы миокарда. Наоборот, при уменьшении диастолического наполнения ЛЖ толщина миокарда может увеличиваться даже при отсутствии гипертрофии. Таким образом, результаты вычисления ММЛЖ по B. Troy должны оцениваться весьма критически. На рис. 7.28 представлена эхокардиограмма больного ГБ с признаками дилатации ЛЖ.
Офтальмоскопия глазного дна — весьма информативный метод, позволяющий оценить степень изменений сосудов сетчатки. У больных ГБ обычно выявляются следующие изменения. 1. Сужение артериол сетчатки (рис. 7.29). В некоторых случаях, особенно у пожилых, артериолы выглядят как узкие белые поблескивающие полоски (симптом “серебряной проволоки”) или полоски желтоватого цвета (симптом “медной проволоки”). По мере прогрессирования ГБ отмечается все более выраженное (в том числе неравномерное) сужение артериол.
2. Расширение вен сетчаткис прогрессирующим уменьшением отношения диаметра артериол и соответствующих им венул меньше 1 : 2 (т.е. 1 : 3, 1 : 4, 1 : 5 и т.д.). 3. Характерные изменения вен в месте их перекреста с артерией. Последние, будучи спазмированными и уплотненными, сдавливают вену в месте перекреста, усугубляя венозный застой крови. Различают несколько степеней таких изменений (см. рис. 7.29):
4. Гипертоническая ретинопатия, развивающаяся в поздних стадиях ГБ, включает несколько признаков:
Последние три признака обычно возникают на фоне гипертонического криза или у больных со злокачественной формой АГ (см. ниже).
Согласно наиболее распространенной классификации, различают 4 степени поражения сосудов сетчатки и сосудистых осложнений ГБ. I степень — минимальное сужение артериол и неравномерность их просвета. Признаки гипертонической ретинопатии отсутствуют. II степень — выраженное сужение артериол с участками спазма и расширения венул при их перекресте с артериями (симптомы Салюс и Гвиста). Признаки ретинопатии отсутствуют. III степень — на фоне резкого спазма артериол и расширения венул определяются признаки гипертонической ретинопатии:
IV степень — любые из вышеперечисленных признаков + отек диска зрительного нерва.
К числу наиболее значимых осложнений ГБ относятся гипертонические кризы, нарушения мозгового кровообращения (геморрагические или ишемические инсульты), ИМ, нефросклероз (первично сморщенная почка), сердечная недостаточность, расслаивающая аневризма аорты и др.
Гипертонический криз — это внезапное повышение АД, нередко сопровождающееся значительным ухудшением церебрального, коронарного, почечного кровообращения, что существенно повышает риск тяжелых сердечно-сосудистых осложнений: инсульта, ИМ, субарахноидального кровоизлияния, расслоения стенки аорты, отека легких, острой почечной недостаточности (осложненный гипертонический криз). А.Л. Мясников называл гипертонические кризы “квинтэссенцией”, “сгустком” ГБ. Гипертонические кризы могут развиваться на любой стадии заболевания. Они возникают под действием известных неблагоприятных факторов, описанных выше, например в результате выраженного психоэмоционального напряжения, алкогольных эксцессов, неадекватного лечения АГ, прекращения приема антигипертензивных лекарственных препаратов, избыточного потребления соли, влияния метеорологических факторов и т.д. В основе гипертонического криза лежит не только необычно высокий подъем АД, но и срыв местной саморегуляции мозгового, коронарного или почечного кровообращения с развитием гипоперфузии или гиперперфузии органов-мишеней, нарушением проницаемости сосудистой стенки, кровоизлияниями и отеком ткани органа и снижением его функции. Согласно рекомендациям ВОЗ/МОГ гипертонический криз диагностируется при повышении диастолического АД > 120 мм рт. ст. В то же время клиническая практика показывает, что симптоматика криза и острые нарушения функции органов-мишеней могут развиваться и при менее значительном повышении АД.
Общепринятой классификации гипертонических кризов не существует. В последние годы наметилась тенденция делить все случаи гипертонических кризов на две группы:
Неосложненный гипертонический криз Неосложненный гипертонический криз чаще возникает на ранних стадиях заболевания (ГБ I–II стадии) и, несмотря на внезапное и часто значительное повышение АД, характеризуется отсутствием сколько-нибудь выраженного поражения органов-мишеней, например острой гипертонической энцефалопатии или ишемии миокарда. В клинической картине таких кризов преобладают вегетативные расстройства, в частности признаки симпатикотонии, а также симптомы, связанные собственно с внезапным повышением АД. В отечественной литературе такие кризы нередко обозначались как “симпато-адреналовые кризы”, “гипертонические кризы I типа” (по классификации А.Л. Мясникова и Н.А. Ратнер, 1968) или “гиперкинетические кризы” (А.П. Голиков с соавт., 1976). Они связаны, в основном, со значительной активацией САС и выбросом в кровь катехоламинов, преимущественно адреналина. Неосложненные кризы обычно развиваются очень бурно, но относительно непродолжительны (не более 2–3 ч) и довольно легко купируются антигипертензивными средствами. В клинической картине, помимо повышения АД, преобладают возбуждение, беспокойство, страх, тахикардия, одышка. Весьма характерно чувство “внутренней дрожи”, холодный пот, “гусиная” кожа, тремор рук, гиперемия лица. Возможен небольшой субфебрилитет. Нарушение местного мозгового кровотока проявляется головной болью, иногда головокружением, тошнотой, однократной рвотой. Во многих случаях наблюдается преимущественное повышение систолического АД. В анализах крови в течение короткого времени может выявляться нейтрофильный лейкоцитоз, гипергликемия. После купирования такого гипертонического криза нередко появляется полиурия. Осложненный гипертонический криз Осложненный гипертонический криз, как правило, развивается в поздние стадии болезни (ГБ II–III стадии) и характеризуется, помимо значительного повышения АД, развитием гипертонической энцефалопатии или других сердечно-сосудистых осложнений. Осложненный гипертонический криз диагностируется в тех случаях, когда на фоне внезапного повышения АД развиваются следующие патологические состояния:
Чаще встречаются гипертонические кризы, осложненные гипертонической энцефалопией. Они соответствуют кризам, традиционно обозначаемым в отечественной литературе как “гипертонические кризы II типа” (по А.Л. Мясникову и Н.А. Ратнер) или “гипокинетические кризы” (А.П. Голиков с соавт.). Осложненные кризы обычно развиваются постепенно, симптоматика сохраняется в течение нескольких дней (даже после снижения АД). В клинической картине преобладают интенсивные головные боли, головокружение, тошнота и рвота, нарушения сознания (заторможенность, оглушенность, потеря сознания и др.). Нередко к общемозговым симптомам присоединяются признаки очаговой неврологической симптоматики: слабость и гипостезия в конечностях, онемение губ и языка, нарушение речи и т.п. Нередко отмечается брадикардия. В тяжелых случаях к этим симптомам присоединяются признаки левожелудочковой недостаточности (одышка, удушье, положение ортопноэ, влажные хрипы в легких), нестабильной стенокардии (загрудинные боли, изменения ЭКГ) или других сосудистых осложнений, перечисленных выше. Исследование глазного дна, как правило, выявляет признаки тяжелой гипертонической ретинопатии II–III степени (отек сетчатки, “хлопьевидные” экссудаты, отек диска зрительного нерва и др.). Следует помнить, что развитие повторных гипертонических кризов у больного ГБ часто свидетельствует о неадекватности проводимой антигипертензивной терапии.
Злокачественная АГ — это синдром, характеризующийся значительным повышением АД, быстрым прогрессированием органических изменений в органах-мишенях (сердце, головной мозг, почки, аорта) и рефрактерностью к антигипертензивной терапии. Синдром злокачественной АГ развивается примерно у 0,5–1,0% больных эссенциальной АГ, чаще у мужчин в возрасте 40–50 лет. Патогенез синдрома злокачественной АГ остается неясным. Предполагают, что в основе его возникновения лежит быстро прогрессирующий некротизирующий артериолит в органах-мишенях, который проявляется значительным и стойким повышением АД и развитием артериолонекроза вследствие усиленного пропитывания сосудистой стенки белками плазмы. В результате ухудшается кровоснабжение почек, головного мозга, сердца и быстро снижается их функция. Непосредственной причиной развития синдрома злокачественной АГ является, вероятно, выраженная активация почечно-надпочечниковой РААС, развивающаяся на фоне артериолонефросклероза (первично сморщенной почки). В крови больных с синдромом злокачественной АГ обычно обнаруживают повышенную концентрацию альдостерона. Клинические проявления синдрома злокачественной АГ обусловлены значительным повышением АД, нарушением перфузии и функционального состояния головного мозга, сердца, почек, органа зрения и других внутренних органов. Наиболее характерны следующие клинические симптомы. 1. АД значительно повышено (диастолическое АД выше 130–140 мм рт. ст.) и плохо поддается медикаментозной коррекции. 2. Отмечаются почти постоянные интенсивные головные боли, головокружение, тошнота, рвота и др. признаки гипертонической энцефалопатии (см. выше). 3. Быстро прогрессируют нарушения зрения вплоть до полной слепоты (при офтальмоскопии определяется гипертоническая ретинопатия III–IV степени с микротромбозами, кровоизлияниями в сетчатку, отеком диска зрительного нерва, отслойкой сетчатки). 4. Выявляются признаки выраженной эксцентрической гипертрофии миокарда ЛЖ с увеличением массы миокарда и дилатацией ЛЖ (по данным ЭхоКГ). 5. Прогрессируют признаки левожелудочковой или бивентрикулярной недостаточности. 6. Быстро нарастают клинические симптомы ХПН с азотемией сыворотки выше 200 ммоль/л. Прогноз синдрома злокачественной АГ чрезвычайно серьезен. При отсутствии адекватного лечения в течение 1 года умирает около 70–80% больных. Наиболее частой причиной смерти является геморрагический инсульт, ХПН, ХСН и расслаивающая аневризма аорты. Активное современное лечение позволяет снизить в несколько раз летальность больных злокачественной АГ. В результате около половины больных выживают в течение 5 лет.
При формулировании диагноза эссенциальной АГ (гипертонической болезни) следует наиболее полно охарактеризовать все индивидуальные особенности течения заболевания, влияющие на прогноз и определяющие тактику лечения больного. При этом желательно придерживаться следующих рекомендаций (В.И. Маколкин). 1. Хотя оба термина — “эссенциальная АГ” и “гипертоническая болезнь” — равнозначны, в отечественной литературе чаще употребляют традиционный термин “гипертоническая болезнь”, который и следует использовать в практической деятельности. 2. Стадия заболевания (I, II, III) указывается в соответствии с современной классификацией ВОЗ, которая хорошо согласуется с классификацией ГБ, предложенной А.Л. Мясниковым. 3. В диагнозе обязательно указание конкретного поражения органов-мишеней (гипертрофия ЛЖ, ангиопатия глазного дна, гипертоническая энцефалопатия, поражение аорты, почек и т.п.). 4. В диагнозе обязательно следует отразить степень повышения АД, согласно классификации JNC-V1 (1996) и ВОЗ/МОГ (1999). 5. Следует также перечислить основные факторы риска ГБ, имеющиеся у больного (ожирение, гиперлипидемия, гиперинсулинемия и др.). 6. В заключение необходимо привести диагноз сопутствующих заболеваний (ИБС, сахарный диабет и др.). Несмотря на то что такая формулировка диагноза ГБ выглядит громоздкой, только такой подход позволяет составить достаточно точное и объективное представление о степени риска возникновения осложнений ГБ и соответственно объективно обосновать необходимость того или иного лечения больных.
Основной целью лечения больных ГБ является максимальное снижение риска развития осложнений АГ и смертности больных. Это достигается путем длительной пожизненной терапии, направленной на:
Таким образом, достижение оптимального уровня АД — далеко не единственная цель, которую преследует врач, подбирая ту или иную терапию больному ГБ. По современным представлениям, тактика ведения больных ГБ должна разрабатываться с учетом степени индивидуального риска АГ, рассчитанного на основании оценки 4-х основных параметров (см. табл. 7.4):
Методика стратификации степени риска АГ была описана выше. Ниже приведены общие принципы ведения больных ГБ, изложенные в рекомендациях ВОЗ/МОГ (1999). 1. Группа низкого риска (САД 140–159 и/или ДАД 90–99 мм рт. ст.; нет факторов риска, нет поражений органов-мишеней; нет сопутствующих заболеваний): показано немедикаментозное лечение и наблюдение за больным в течение 6–12 мес. 2. Группа среднего риска (при САД 140–159 и/или ДАД 90–99 мм рт. ст.; имеется 1–2 фактора риска, кроме сахарного диабета; нет поражений органов-мишеней, нет сопутствующих заболеваний): показано немедикаментозное лечение и наблюдение за больным в течение 3–6 мес. 3. Группа среднего риска (при САД 160–179 и/или ДАД 100–109 мм рт. ст.; имеется 1–2 фактора риска или они отсутствуют; нет поражений органов-мишеней, нет сопутствующих заболеваний): показано медикаментозное лечение. 4. Группы высокого и очень высокого риска (при наличии поражений органов-мишеней, сопутствующих заболеваний, сахарного диабета или более 3-х ФР, независимо от уровня АД): показано медикаментозное лечение. 5. При изолированной систолической АГ и САД і 160 мм рт. ст. медикаментозное лечение показано при наличии факторов риска (в том числе — возраст больше 65 лет) или поражений органов-мишеней или при наличии сопутствующих заболеваний, сахарного диабета. Согласно приведенным рекомендациям ВОЗ/МОГ, лечение эссенциальной АГ (медикаментозное или/и немедикаментозное) следует проводить у всех больных, уровень АД у которых превышает 140/90 мм рт. ст. В одних случаях (низкий риск возникновения осложнений) вначале это может быть только немедикаментозная терапия, в других (средний, высокий и очень высокий риск) — ее сочетание с приемом индивидуально подобранных антигипертензивных лекарственных средств. В полной мере это относится к лицам с так называемой “мягкой” АГ (исходный уровень АД 140–159/90–99 мм рт. ст.). Напомним, что число пациентов с “мягкой” АГ достигает 60–70% от общего числа больных ГБ. Поэтому достижение оптимального уровня АД у этой группы больных оказывает особенно большое влияние на снижение общего показателя сердечно-сосудистой заболеваемости и смертности пациентов с ГБ. Понятно, что чем выше исходный уровень АД, зарегистрированный до начала лечения, больше число имеющихся у больного неблагоприятных факторов риска и сопутствующих заболеваний, а также органных нарушений (гипертрофия ЛЖ, гипертоническая ретинопатия, гипертоническая энцефалопатия и т.д.), тем активнее должно проводиться лечение ГБ. Следует подчеркнуть, что, в отличие от достаточно широко распространенного мнения, активная антигипертензивная терапия целесообразна также у пациентов пожилого и старческого возраста (при уровне АД > 140/90 мм рт. ст.), в том числе у больных с изолированной систолической АГ. В последние годы убедительно показано, что эффект антигипертензивной терапии у этих больных (снижение числа осложнений АГ и летальных исходов) оказывается даже более значительным, чем у пациентов молодого и среднего возраста и лиц с систоло-диастолической АГ.
В нескольких крупномасштабных клинических исследованиях последних лет убедительно показано, что с помощью регулярной терапии современными антигипертензивными препаратами удается на 40–50% снизить летальность от мозгового инсульта и на 15% — от ИМ. Кроме того, поддержание АД на оптимальном уровне существенно улучшает качество жизни больных ГБ, их трудоспособность и физическую активность в быту.
Немедикаментозное лечение больных ГБ направлено, в первую очередь, на устранение или уменьшение действия некоторых модифицируемых факторов риска, способствующих прогрессированию заболевания и развитию осложнений: снижение избыточной массы тела, ограничение потребления поваренной соли, алкоголя, отказ от курения, диетическая коррекция нарушений липидного и углеводного обменов, повышение физической активности и т.д. Эти мероприятия обязательны у каждого больного ГБ, независимо от уровня АД, количества факторов риска и сопутствующих заболеваний. Примерно у половины больных с мягкой АГ удается достичь оптимального уровня АД только с помощью немедикаментозной коррекции факторов риска. У лиц с более высоким уровнем АД немедикаментозное лечение, проводимое параллельно с приемом антигипертензивных препаратов, позволяет существенно снизить дозы лекарственных препаратов и уменьшить риск возникновения побочных эффектов этих лекарственных средств. Мало того, отказ от проведения немедикаментозных мероприятий, направленных на коррекцию основных факторов риска (модификацию образа жизни больного), является одной из наиболее частых причин рефрактерности больных к терапии антигипертензивными средствами. Снижение избыточной массы тела (МТ) закономерно сопровождается уменьшением системного АД. Методика немедикаментозной коррекции ожирения подробно изложена в главе 4. Коррекция гиперлипидемийпредусматривает, прежде всего, снижение общей калорийности пищи в соответствии с индексом ИМТ (подробнее — см. главу 4) и ограничение простых углеводов и животных жиров. Целесообразно также исключить из пищевого рациона больных ГБ крепкий кофе, чай, шоколад, копчености, продукты, богатые холестерином. При необходимости можно использовать медикаментозную коррекцию гиперлипидемий (см. главу 4). Ограничение потребления соли до 5–6 г в сутки приводит к небольшому снижению АД и способствует повышению чувствительности больных к антигипертензивной терапии. Более значительное ограничение NаCl показано в случаях обострения заболевания или развития осложнений ГБ (гипертонический криз, сердечная недостаточность, злокачественная АГ), а также больным с так называемой объемзависимой АГ. Следует помнить, что чрезмерное длительное ограничение соли (ниже 2,0 г в сутки) может привести к гипонатриемии и компенсаторной активации РАС, что по понятным причинам может иметь неблагоприятные последствия. Кстати, такая же ситуация (гипонатриемия с активацией РАС) может возникнуть при передозировке некоторых диуретиков (см. ниже). Повышение потребления калия и магния, наряду с ограничением поступления ионов Na+, способствует снижению АД. Больным рекомендуется употреблять в пищу больше фруктов, овощей, соков. Следует помнить, что калий содержится в таких продуктах, как печеный картофель, морская капуста, говядина, треска, овсяная крупа, персики, абрикосы, бананы, чернослив, фасоль, урюк, тыква, груши, апельсины и др. В состав магниевой диеты входит фасоль, горох, о
Поиск по сайту: |





 Запомните
При измерении АД по методу Короткова систолическое АД регистрируют при появлении первых тихих тонов над лучевой артерией (I фаза), а диастолическое АД — в момент полного исчезновения звуков Короткова (V фаза). Целесообразно также определять уровень давления в манжете в момент резкого ослабления тонов (IV фаза).
Запомните
При измерении АД по методу Короткова систолическое АД регистрируют при появлении первых тихих тонов над лучевой артерией (I фаза), а диастолическое АД — в момент полного исчезновения звуков Короткова (V фаза). Целесообразно также определять уровень давления в манжете в момент резкого ослабления тонов (IV фаза).