|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Катаболизм компонентов основного вещества
Идет под действием некоторых гидролаз. Например, НЕЙРАМИНИДАЗА отщепляет от гликопротеинов N-ацетилнейраминовую (сиаловую) кислоту, и уже дестабилизированный гликопротеин поглощается макрофагами. Поэтому концентрация сиаловых кислот в крови - характеристика состояния соединительной ткани. При воспалительных процессах эта концентрация намного возрастает. При недостаточности ферментов катаболизма основного вещества развиваются заболевания - мукополисахаридозы, при которых в тканях происходит накопление тех или иных ГАГ. ВОЛОКНА СОЕДИНИТЕЛЬНОЙ ТКАНИ В межклеточном матриксе находятся 2 типа волокнистых структур: КОЛЛАГЕНОВЫЕ и ЭЛАСТИНОВЫЕ ВОЛОКНА. Основным их компонентом является нерастворимый белок КОЛЛАГЕН. КОЛЛАГЕН Коллаген является основным структурным белком межклеточного матрикса. Это фибриллярный белок, отличающийся от других белков рядом особенностей своего состава и структуры. Типичная молекула коллагена состоит из трех полипептидных целей разных типов (α-спиралей), скрученных в виде правойтройной спирали. В свою очередь полипептидные цепи построены из часто повторяющихся фрагментов, имеющих характерную последовательность -Gly-X-Y-. Каждым третьим аминокислотным остатком является глицин. Пролин (Pro) часто встречается в положениях X, положение Υ может быть занято как пролином, так и 4-гидроксипролином (4Нур). Кроме того, молекула коллагена содержит остатки З-гидроксипролина (ЗНур) и 5-гидроксилизина (5Нуl). Присутствие в полипептидной цепи остатков гидроксиаминокислот является характерной особенностью коллагена. Остатки пролина и лизина гидроксилируются посттрансляционно, т. е. после включения в полипептидную цепь. На одном из концов молекула коллагена сшита поперечными связями, образованными боковыми цепями остатков лизина. Количество поперечных связей возрастает по мере старения организма. При формировании вторичной структуры полипептидная цепь коллагена укладывается в более развернутую левозакрученную a-спираль (на один виток приходится 3 аминокислотных остатка); Третичная структура коллагена — это правозакрученная суперспираль из 3 a-цепей, при формировании которой остаток глицина оказывается в ее центре, что способствует образованию линейной молекулы тропоколлагена с последующим включением ее в волокно. Типы коллагена. Известно 19 типов коллагена, которые отличаются друг от друга по первичной структуре пептидных цепей, функциям и локализации в организме. Коллагены входят в состав фибрилл (фибриллообразующие коллагены- I, II, III, V и XI типы), миофибрилл (коллаген VI типа), являются структурным компонентом базальных мембран (коллаген IV типа) и т.д. Фибриллообразующие коллагены (I, II, III, V и XI типы). Основа фибрилл — ступенчато расположенные параллельные ряды молекул тропоколлагена, которые сдвинуты на 1/4 относительно друг друга. Фибриллогенезу предшествует еще одна модификация лизина. Внеклеточный медьсодержащий фермент лизилоксидаза осуществляет окислительное дезаминирование лизина и гидроксилизина с образованием реактивных альдегидов. Для этих реакций необходимо присутствие витаминов РР и В6. Эти группы принимают участие в формировании поперечных ковалентных связей между молекулами тропоколлагена. Преимущественное распределение этих типов коллагена по тканям следующее: I тип — кости, дентин, роговица, сухожилия; II тип — хрящи, межпозвоночные диски, стекловидное тело; III тип — почки, печень, сосуды, лимфатические узлы. Коллагены V и XI типов в разных количествах присутствуют в межклеточном веществе всех тканей, они определяют диаметр коллагеновых фибрилл. Синтез и созревание коллагена (рис.3,4) Синтез и созревание коллагена представляют собой сложный многоэтапный процесс, который начинается в клетке, а завершается во внеклеточном пространстве. Он включает в себя ряд пострансляционных изменений: гидроксилирование пролина и лизина, гликозилирование гидроксилизина, отщепление N- и С-концевых пептидов. Благодаря этим изменениям появляются дополнительные возможности для стабилизации цепей в молекуле тропоколлагена; в образовании водородных связей участвуют не только NH- и СО-группы пептидного остова но и ОН-группы гидроксипролина; гидроксипролин и пролин, являясь «жесткими» молекулами, ограничивают вращение полипептидного стержня. Определенную роль в синтезе коллагена играют белки - шапероны, которые обеспечивают «контроль качества» коллагена: они способствуют правильному синтезу молекул коллагена и их транспорту по секреторным путям, а также «отслеживают» неправильно собранные молекулы коллагена, которые затем разрушаются. СИНТЕЗ КОЛЛАГЕНА Существуют 8 этапов биосинтеза коллагена: 5 внутриклеточных и 3 внеклеточных. 1-Й ЭТАП Протекает на рибосомах, синтезируется молекула-предшественник: препроколлаген. 2-Й ЭТАП С помощью сигнального пептида “пре” транспорт молекулы в канальцы эндоплазматической сети. Здесь отщепляется “пре” - образуется “проколлаген”. 3- Й ЭТАП Аминокислотные остатки лизина и пролина в составе молекулы коллагена подвергаются окислению под действием ферментов пролилгидроксилазы и лизилгидроксилазы.. При недостатке витамина “С” - аскорбиновой кислоты наблюдается цинга, - заболевание, вызванное синтезом дефектного коллагена с пониженной механической прочностью, что вызывает, в частности, разрыхление сосудистой стенки и другие неблагоприятные явления. 4-Й ЭТАП Посттрасляционная модификация - гликозилирование проколлагена под действием фермента гликозилтрансферазы. Этот фермент переносит глюкозу или галактозу на гидроксильные группы оксилизина. 5-Й ЭТАП Заключительный внутриклеточный этап - идет формирование тройной спирали - тропоколлагена (растворимый коллаген). В составе про-последовательности - аминокислота цистеин, который образует дисульфидные связи между цепями. Идет процесс спирализации. 6-Й ЭТАП Секретируется тропоколлаген во внеклеточную среду, где амино- и карбоксипротеиназы отщепляют (про-)-последовательность. 7-Й ЭТАП Ковалентное “сшивание” молекулы тропоколлагена по принципу “конец-в-конец” с образованием нерастворимого коллагена. В этом процессе принимает участие фермент лизилоксидаза (флавометаллопротеин, содержит ФАД и Cu). Происходит окисление и дезаминирование радикала лизина с образованием альдегидной группы. Затем между двумя радикалами лизина возникает альдегидная связь. Лизилоксидаза является Cu-зависимым ферментом, поэтому при недостатке меди в организме происходит уменьшение прочности соединительной ткани из-за значительного повышения количества растворимого коллагена (тропоколлагена). 8-Й ЭТАП Ассоциация молекул нерастворимого коллагена по принципу “бок-в-бок”. Ассоциация фибрилл происходит таким образом, что каждая последующая цепочка сдвинута на 1/4 своей длины относительно предыдущей цепи. Только после многократного сшивания фибрилл коллаген приобретает свою уникальную прочность, становится нерастяжимым волокном.
Рисунок 3 Катаболизм коллагена Нативный коллаген не гидролизуется обычными пептидгидролазами, основной фермент катаболизма коллагена — коллагеназа. Коллаген — медленно обменивающийся белок, о скорости его обмена судят по содержанию оксипролина в крови и моче. Катаболизм коллагена более активен в молодом возрасте (до 20 лет) и при некоторых
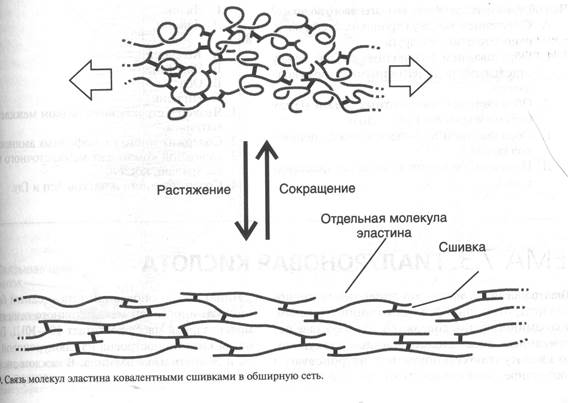
Рисунок 4 заболеваниях (коллагенозы, гиперпаратиреоидизм, некоторые инфекционные заболевания). Эластические волокна 2-й вид волокон - эластические. В основе строения - белок эластин.Эластин еще более гидрофобен, чем коллаген. В нем до 90% гидрофобных аминокислот. Эластин - это основной структурный компонент эластических волокон, которые содержатся в тканях, обладающих значительной эластичностью (кровеносные сосуды, связки, легкие). Свойства эластичности проявляются высокой растяжимостью этих тканей и быстрым восстановлением исходной формы и размера после снятия нагрузки. Эластин — гликопротеин с молекулярной массой 70 кД, который содержит много гидрофобных аминокислот (Гли, Вал, Ала, Лей, Про). В отличие от большинства белков пептидные цепи эластина не приобретают характерную третичную структуру, а сохраняют гибкую случайную конформацию (рис.5).
Рисунок 5 В межклеточном матриксе молекулы эластина образуют волокна, сети, слои, в которых отдельные молекулы связаны множеством сшивок. Наличие гибкой случайной конформации молекул эластина и большого количества поперечных сшивок позволяет эластическим волокнам проявлять свои резиновоподобные свойства.
Поиск по сайту: |