 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
ТЕОРИЯ АКТИВИРОВАННОГО КОМПЛЕКСА
Теория столкновений непригодна для сложных молекул потому, что она предполагает существование молекул в виде идеальных упругих сферических частиц. Однако для сложных молекул, помимо поступательной энергии, должны быть учтены другие виды молекулярной энергии, например, вращательная и колебательная. По теории столкновений невозможно существование реакций, в которых должны столкнуться три и более молекулы. Кроме того, реакции разложения типа АВ = А + В трудно объяснить этой теорией. Для преодоления указанных затруднений Х. Эйринг в 1935г. предложил теорию активированного комплекса. Всякая химическая реакция или любой другой молекулярный процесс, протекающий во времени(диффузия, вязкое течение и т.д.), состоит в непрерывном изменении расстояний между ядрами атомов. При этом конфигурация ядер, отвечающая начальному состоянию, через некоторую промежуточную конфигурацию – активированный комплекс или переходное состояние – превращается в конечную конфигурацию. Предполагается, что активированный комплекс образуется как промежуточное состояние во всех химических реакциях. Он рассматривается, как молекула, которая существует лишь временно и разрушается при определенной скорости. Этот комплекс образуется из таких взаимодействующих молекул, энергия которых достаточна для того, чтобы они смогли близко подойти друг к другу по схеме: реагенты Энергия активации всегда представляет поглощенную энергию, независимо от того, является ли общее изменение ее для реакции положительным (эндотермическая реакция) или отрицательным (экзотермическая реакция). Это схематично показано на рис. 6.
 
    
                 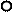       
Рисунок 6. Энергетическая схема образования активированного комплекса.
Активация – сообщение молекулам такого количества энергии, что при их эффективном превращении происходит образование веществ в активированном состоянии. Превращение – образование из веществ, находящихся в активированном состоянии, продуктов реакции. Если система не может перейти через этот энергетический барьер в ней не могут произойти химические превращения. Значит эта система химически неактивна и нуждается в некоторой дополнительной энергии для активации. Количество этой дополнительной энергии зависит от того, какой энергией уже обладает система. Энергия исходной системы не может быть меньше ее нулевой энергии (т.е. при 00К). Для активации любой системы достаточно сообщить ей дополнительную энергию. Эта энергия называется истинной энергией активации. Истинной энергией активации элементарного химического акта называется минимальная энергия, которой должна обладать исходная система сверх совей нулевой энергии (т.е. при 00 К), чтобы в ней могли произойти химические превращения. Разность истинной энергии активации обратной и прямой реакций равна тепловому эффекту реакции при абсолютном нуле.
Поиск по сайту: |
 активированный комплекс
активированный комплекс  продукты. Активированный комплекс имеет промежуточную структуру между реагентами и продуктами. Энергия активации реакции есть дополнительная энергия, которую должны приобрести реагирующие молекулы, чтобы образовать активированный комплекс, необходимый для протекания реакции.
продукты. Активированный комплекс имеет промежуточную структуру между реагентами и продуктами. Энергия активации реакции есть дополнительная энергия, которую должны приобрести реагирующие молекулы, чтобы образовать активированный комплекс, необходимый для протекания реакции.