 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Описание метода и установки.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РФ ВЛАДИМИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ МУРОМСКИЙ ИНСТИТУТ КАФЕДРА: «ФИЗИКА» ДИСЦИПЛИНА: ФИЗИКА ЛАБОРАТОРНАЯ РАБОТА №1.05
«СПЕКТРАЛЬНЫЙ АНАЛИЗ СПЛАВОВ»
Утверждена на методическом семинаре каф. физики Зав. кафедрой ________
Муром 2004 Техника безопасности
1. Режим работы генератора – повторно кратковременный: 5 минут работы, 2 минуты перерыва. При непрерывной работе генератор выходит из строя. 2. Не включать генератор без заземления. 3. Работу со стилоскопом следует проводить в резиновых перчатках и иметь под ногами резиновый коврик. 4. При включенном токе не прикасаться к головке прибора и к электроду стилоскопа. Смена электродов может проводится только при отключенном генераторе. 5. Не оставлять установку под током в перерывах между анализами окончании работы. 6. ЗАПРЕЩАЕТСЯ работать с влажным генератором и стилоскопом после пребывания их под дождем или после отпотевания от температурных изменений. 7. Работа с приборами может производиться как на открытом воздухе под навесом при температуре от -40ºС до +35ºС и относительной влажности до 80%, так и в помещении при тех же условиях. Лабораторная работа № 1.05 «Спектральный анализ сплавов»
Приборы и оборудование: 1. Стилоскоп типа СЛП-1 2. Генератор высокой частоты ПДГ-1 3. Исследуемый электрод (образец)
Введение. Состояние электронов в атомах определяется значением четырех квантовых чисел. 1. n – главное квантовое число, принимающее значение 1, 2, 3,…
m – магнитное квантовое число, связанное с Данному значению Магнитное спиновое квантовое число 2. На основании принципа Паули можно объяснить закономерности в строении электронных оболочек атомов. Будем считать, что электроны движутся вокруг атомного ядра и образуют электронное облако (такое название вполне справедливо из-за волновых свойств электронов). В этом облаке можно выделить электронные слои или электронные оболочки, отличающиеся значением главного квантового числа. Для n =1 соответствует К-оболочка. Для n=2 , В каждой оболочке можно выделить электроны, отличающиеся значением квантового числа l , которые образуют электронные подоболочки. Электроны с l=0 называются S – электронами, с l=1 – p-электронами. l=2 d –электронами, с l=3 f-электронами и т.д. Легко убедиться в том, что данному значению l соответствует 2(2 l+1) электронов и т.д. Для l=0 – 2 электрона. Для l=1 – 6 электронов и т.д. Для данного значения n в атоме не может быть больше 2n Полностью заполненная К-оболочка имеет 2 электрона, L-оболочка- 8 электронов, М-оболочка - 18 электронов и т. д. На основании принципа Паули можно объяснить периодический закон Д.Н. Менделеева, который утверждает, что если расположить химические элементы в порядке возрастания их атомных весов, то их физические и химические свойства будут периодически повторяться. В настоящее время установлено, что элементы в таблице Менделеева расположены в порядке возрастания величины заряда атомного ядра Z, выраженного в элементарных зарядах. Атомы химических элементов нейтральны. Значит, вокруг ядра с зарядом Z движется Z электронов, т.е. порядковый номер элемента в таблице Менделеева показывает также число электронов в атоме химического элемента. Электроны в атомах последовательно занимают такое состояние, чтобы энергия атома была наименьшей в основном состоянии атома. 3. Можно, начиная с атома Z =I (водород), проследить порядок заполнения электронных оболочек. Каждый последующий атом можно получить, увеличивая заряд ядра предыдущего атома на единицу и добавляя к нему один электрон, который должен занять доступное ему согласно принципу Паули, состояние с наименьшей энергией. Можно ожидать, что имеется некоторая периодичность в строении электронных оболочек, в частности их внешних оболочек. 4.В настоящее время установлено, что многие физические и химические свойства веществ определяются строением внешних оболочек атомов, образующих данное вещество. Следовательно, должна наблюдаться периодичность в строении внешних оболочек атомов химических элементов. Это можно видеть из таблиц I , где показано распределение электронов в основных состояниях атомов химических элементов с №1 до №20. Возьмем щелочные металлы Li ,K, Na. Во внешней оболочке этих атомов имеется по одному S – электрону. Эти элементы имеют тождественные химические и оптические свойства. В частности в их спектрах можно выделить одинаковые серии спектральных линий. Однако длины волн отдельных линий даже в одинаковых сериях будут различными. Такое различие связано с различным числом электронов в атомах. Литий имеет 3- электрона, натрий-11 , калий-19. Внешний валентный электрон в различных атомах щелочных металлов будет двигаться в различных потенциальных полях и будет, естественно, обладать разной энергией. С этим связано и различие в длинах волн спектральных линий. В спектре каждого химического элемента можно выделить линии, характерные только для данного элемента. По таким линиям можно обнаружить отдельные химические элементы в смеси веществ (в растворах, сплавах и т.д.), а это есть задача спектрального анализа.
Таблица 1
Описание метода и установки.
Спектральным анализом называется способ определения химического состава вещества по спектру, излучаемому его атомами. Спектральный анализ разделяется на качественный и количественный. Задача качественного анализа – установить наличие в смеси тех или иных элементов по имеющимся в спектрах характерным линиям анализируемых элементов. Задача количественного анализа - установить количественное содержание анализируемых элементов в смеси по интенсивности линий данного элемента - является функцией его концентрации, чем больше содержание данного элемента, тем интенсивнее линии этого элемента в спектре. Количественный расчет концентрации - задача сложная, так как интенсивность спектральной линии зависит не только от концентрации элемента, но и от условий возбуждения спектра и ряда других причин. Количественный анализ низкой точности называют полуколичественным. Источником возбуждения спектра является электрическая дуга. В дуге доминирующую роль играют процессы соударения атомов с электронами, при которых кинетическая энергия электронов переходит в энергию возбуждения атомов. Температура в дуге между металлическими электродами достигает примерно 50000 С. Дуга переменного тока между металлическими электродами не стабильна, она гаснет в момент прохождения тока через ноль и вновь не загорается, так как вследствие большой теплопроводности металлов концы электродов быстро охлаждаются. Чтобы получить стабильную дугу переменного тока между металлическими электродами, к дуговому промежутку, кроме напряжения сети (220 В) с частотой 50 Гц, подводят ток высокочастотный большого напряжения. Такая дуга называется активизированной дугой Свентицкого (рис.1). Напряжение от сети 220 В подводится к трансформатору Тр1,подающему напряжение до 1800 В, от которого заряжается конденсатор С1. В момент пробоя искрового промежутка конденсатор заряжается, и в контуре возникают затухающие колебания с частотой 1,5-10 Гц Трансформатор Тр2 повышает напряжение этих колебаний до 11500В, и это напряжение подается электродам, образующим искровой промежуток. К электродам подается также и напряжение от сети 220B. Блокировочный конденсатор С2 препятствует проникновению высокочастотных колебаний в сеть переменного тока. При правильной нагрузке контура искры проскакивают между электродами дуги в момент, следующий за паузами тока, питающего дугу. Ионизация, обусловленная этими искрами, оказывается достаточной для зажигания дуги после каждого погасания при прохождении тока через нуль. Высокочастотный генератор смонтирован в отдельном корпусе. Генератор ПДГ-1 дает возможность получить дугу и переменного тока и низко валентную искру. Для переключения с дугового режима на искровой имеется на корпусе переключатель. В сеть генератор подключается при помощи провода с вилкой. На корпусе имеется сигнальная лампочка, сигнализирующая о наличии напряжения в сети вторичной обмотки разделительного трансформатора. Работа с генератором без сигнальной лампочки ВОСПРЕЩАЕТСЯ. Для включения генератора в сеть служит магнитный пускатель типа II- 6-III. Включение его осуществляется нажатием кнопки включателя на ручке стилоскопа, соединенного с генератором гибким (проводом) кабелем. Стилоскоп СЛП-I служит для быстрого качественного визуального и полуколичественного анализа всех наиболее распространенных марок легированных сталей и цветных сплавов по их спектрам излучения в основном по элементам: методом спектрального анализа. Оптическая схема стилоскопа (рис.2) тождественна схеме спектроскопа. Свет от дуги II через защитные стекла направляется призмой 3 на конденсор 4, который фиксирует его на щель 5. Объектив 6 фокусирует расходящийся пучок лучей и направляет его на дисперсирующие призмы 7 и 3, где свет разлагается в спектр. Отражаясь от посеребренного большого катета призмы 8, лучи проходят в обратном направлении призмы 6 и 7 , что увеличивает дисперсию прибора. Затем пучок лучей, пройдя объектив 6, превращается в сходящийся и попадает на призму 9, которая направляет его на окуляр 10. Конструктивно стилоскоп состоит из головки 1 с осветительной системой и спектрального аппарата 2 (рис 3). В корпусе головки находятся защитные стекла, призма и конденсор. На конце головки в оправе 3 укрепляют анализируемый электрод, имеющий форму пластинки, и постоянный стержневой или дисковой электрод 4. Головка изолирована от остальной части изолятором 5. Стержень головки 10 служит для поворота призмы 3 (рис 3), что позволяет вводить спектр в поле зрения. В поле зрения окуляра 6 имеется указатель для фиксации спектральных линии. На окулярной части закреплен резиновый глазник 7 для защиты глаз от постороннего света. На корпусе смонтирован барабан 8 со шкалой, вращением которого поворачивают призму 8 (рис. 2), тем самым перемещая спектр в поле зрения окуляра. Для шкалы барабана имеется градуировочная кривая, указывающая длины волн соответствующие различным делениям шкалы. К корпусу прикреплена ручка с кнопкой для включения высокочастотного генератора. Содержание примеси в сплаве определяют сравнением интенсивности спектральных линий примеси с интенсивностью спектральных линий основного металла. При выполнении необходимых расчетов пользуются таблицами (приложенных к прибору). В нашей лабораторной работе нужно произвести качественный и полу количественный анализы медного сплава, взятого в виде латунной пластинки. При анализе медных сплавов почти во всех случаях применяют стандартный медный электрод стержневой или дисковой.
Поиск по сайту: |
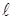 – азимутальное (орбитальное) квантовое число, принимающее значения 0, 1, 2,…(n-1)
– азимутальное (орбитальное) квантовое число, принимающее значения 0, 1, 2,…(n-1)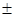 1,
1,  значений m. Четвертое квантовое число определяет внутреннюю степень свободы электрона, его спин и называется спиновым квантовым числом S, принимающим значение +1/2.
значений m. Четвертое квантовое число определяет внутреннюю степень свободы электрона, его спин и называется спиновым квантовым числом S, принимающим значение +1/2. ms равно: (-1/2) или (+1/2). Для электронов справедлив принцип Паули: в состоянии с заданными значениями четырех квантовых чисел n, l, m, ms не может быть больше одного электрона.
ms равно: (-1/2) или (+1/2). Для электронов справедлив принцип Паули: в состоянии с заданными значениями четырех квантовых чисел n, l, m, ms не может быть больше одного электрона. -оболочка. Для n=3-М оболочка и т.д. n=4-N оболочка.
-оболочка. Для n=3-М оболочка и т.д. n=4-N оболочка. электронов.
электронов.
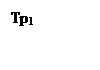
 Рис.1
Рис.1