 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Порядок выполнения работы и обработки результатов измерений ⇐ ПредыдущаяСтр 3 из 3
Опыт 1. Приготовление водного раствора соли NaCl с заданной массовой долей w% из чистого вещества. 1. Получите у преподавателя задание (массовую долю раствора соли). 2. Возьмите взвешенную на технохимических весах данную массу соли (mNaCl = 10 г) и высыпьте её в химический стакан на 250 мл. 3. Рассчитайте массу получаемого раствора, используя формулу (8.4), данные расчета занесите в таблицу 8.2. 4. Рассчитайте объём воды, необходимой для получения раствора с заданной массовой долей, используя формулу (8.5), данные расчета занесите в таблицу 8.2. 5. Отмерьте цилиндром необходимый объём воды и влейте его в стакан с солью. 6. Перемешайте содержимое стакана стеклянной палочкой до полного растворения соли. 7. Перелейте полученный раствор в мерный цилиндр и определите объём раствора, данные занесите в таблицу 8.2. 8. При помощи ареометра определите плотность полученного раствора Таблица 8.2 – Таблица экспериментальных и рассчетных данных
9. По таблице 8.3 определите теоретическое значение плотности раствора с заданной массовой долей Таблица 8.3 – Массовая доля w и плотность r растворов соли NaCl при 20 оС
10. Сравните полученные данные rэкс и rтеор. 11. Рассчитайте молярную СМ и моляльную Сb концентрации растворов. Данные расчётов занесите в таблицу 8.2.
Опыт 2. Приготовление водного раствора соли NaCl с заданной массовой долей w2% из более концентрированного раствора с массовой долей w1%. 1. Получите у преподавателя задание (массовую долю получаемого раствора и объём концентрированного раствора соли). 2. Отмерьте цилиндром заданный объём концентрированного раствора соли и влейте его в химический стакан на 250 мл. 3. Рассчитайте объём воды, необходимой для получения раствора с заданной массовой долей, используя формулу (8.8), плотности растворов r1 и r2 определите по таблице 8.3. 4. Отмерьте цилиндром необходимый объём воды и влейте его в стакан с концентрированным раствором. 5. Тщательно перемешайте содержимое стакана стеклянной палочкой. 6. При помощи ареометра определите плотность полученного раствора 7. Сравните полученное значение с табличным 8. На основании полученных данных сделайте вывод. Контрольные вопросы 1. Дать определение раствора, назвать его составляющие. 2. Охарактеризовать процессы, происходящие при растворении вещества. 3. Дать определение насыщенного и ненасыщенного раствора. 4. Охарактеризовать один из природных растворителей веществ –воду. 5. Дать определение растворимости вещества. Привести примеры различной растворимости веществ. 6. Дать определение величин, характеризующих долевой способ выражения содержания вещества (массовая доля,мольная доля, объёмная доля). 7. Дать определение величин, характеризующих концентрационный способ выражения содержания вещества (молярная концентрация, моляльная концентрация, нормальная концентрация).
Список рекомендуемой литературы 1. Глинка, Н.Л. Общая химия: учеб. пособие для вузов / Н.Л. Глинка; под ред. А.И. Ермакова – 30-е изд. – М.: Интеграл-Пресс, 2004. – 727 с. – § 7.2 2. Евтюхов, К.Н. Концепции современного естествознания: Учебное пособие для студентов экономических и гуманитарных специальностей очной и заочной форм обучения / Евтюхов К.Н. – Брянск: БГИТА, 2011. - §§ 13.1-13.4.
Поиск по сайту: |
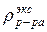 , данные занесите в таблицу 8.2.
, данные занесите в таблицу 8.2. , г
, г
 , мл
, мл
 .
.